
| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法判断 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 邻甲基苯酚可被KMnO4( H +,aq ) 氧化为邻羟基苯甲酸 | |
| B. | 葡萄糖能被新制Cu( OH )2氧化,但不能使溴水褪色 | |
| C. | 苯及其同系物都不能使溴水褪色 | |
| D. | 羧酸不具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、Al3+、Br-、SO42- | B. | Na+、K+、OH-、SiO32- | ||
| C. | Ca2+、K+、Br-、Cl- | D. | Li+、H+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 未洗涤烧杯和玻璃棒 | B. | 转移溶液前溶液未冷却至室温 | ||
| C. | 容量瓶未干燥 | D. | 定容时俯视 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
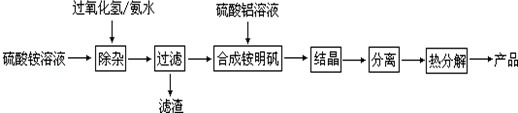
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇与氧气反应生成醛 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 乙醇与浓硫酸加热到140℃ | |
| D. | 乙酸乙酯与稀硫酸共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积.该小组设计的简单实验装置如图所示:该实验的主要操作步骤如下:
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积.该小组设计的简单实验装置如图所示:该实验的主要操作步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| A | 乙酸乙酯(乙醇) | 乙酸 | 加热回流 |
| B | 乙烷(乙烯) | 酸性KMnO4 | 洗气 |
| C | 乙醇(乙酸) | 新制氧化钙 | 蒸馏 |
| D | 苯(溴) | 碘化钾溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3、CO、CO2都是极性分子 | |
| B. | CH4、CCl4都是含有极性键的非极性分子 | |
| C. | NH3、PH3、AsH3的稳定性和沸点随 N、P、As 的核电荷数的变化趋势如图所示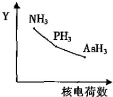 | |
| D. | CS2、H2O、C2H2都是直线型分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com