
【题目】A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(部分产物已略去)。下列说法正确的是( )

A. 若X为KOH溶液,则A可能为Al
B. 若X为Fe,则C可能为Fe(NO3)2溶液
C. 若A、B、C均为焰色反应呈黄色的化合物,则X一定为CO2
D. 若X为O2,则A可为有机物乙醇,也可为非金属单质硫
【答案】B
【解析】
A. 若X为KOH溶液、A为A1时,Al和碱反应只能生成偏铝酸钾,不符合转化关系,A可以为Al3+,故A错误;
B. 若X为Fe,则A和铁反应的量不同,产物不同,且产物可以和铁反应,证明A为氧化性酸,判断A可以为HNO3,B为Fe(NO3)3溶液,则C可能为Fe(NO3)2溶液,故B正确;
C. 若A. B. C均为焰反应呈黄色的化合物,说明含钠元素,转化关系中A可以是NaOH,X可以是二氧化碳或二氧化硫,B为碳酸钠或亚硫酸钠,C为碳酸氢钠或亚硫酸氢钠,故C错误;
D. 若X为O2,A为有机物乙醇,可以实现A→B→C的转化,但不能一步实现A→C;为非金属单质硫时,可以实现A→B→C的转化,但不能实现A→C的转化,故D错误;
答案选B。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】如图所示,在A处通入氯气,关闭B阀时,C处的红布条看不到明显现象;当打开B阀后,C 处的红布条逐渐褪色。有以下几种溶液,则D瓶中盛放的溶液可能是
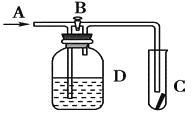
①浓硫酸 ②NaOH溶液 ③H2O ④饱和氯化钠溶液
A.①③B.①②C.②③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某相对分子质量为26的烃A,是一种重要的有机化工原料,以A为原料在不同的反应条件下可以转化为烃B、烃C。B、C的氢核磁共振谱显示都只有一种氢,且B分子中碳碳键的键长有两种。以C为原料通过下列方案可以制备具有光谱高效食品防腐作用的有机物M,M分子的球棍模型如图所示。
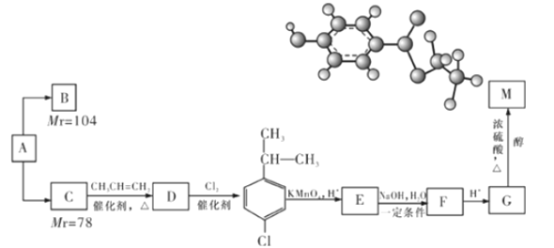
根据上述信息,回答下列问题:
(1)B能使溴的四氯化碳溶液褪色,则B的结构简式为____________,B与等物质的量Br2作用时可能有_________种产物。
(2)C→D的反应类型为______________________。
(3)写出E→F的化学方程式_______________________________。
(4)G分子中的含氧官能团的名称是______________,写出由G反应生成高分子的化学反应方程式___________________________。
(5)M的同分异构体有多种,写出满足以下条件的所有同分异构体的结构简式:
①能发生银镜反应②含有苯环且苯环上一氯取代物有两种③遇FeCl3溶液不显紫色④1mol该有机物与足量的钠反应生成1mol氢气(一个碳原子上同时连接两个—OH的结构不稳定)_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐含有泥沙以及Ca2+、Mg2+、SO42﹣等杂质,其提纯过程一般经过以下流程:

某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液等药品以及必备的实验仪器若干。请回答下列问题:
(1)操作①粗盐样品加水之前,需要将大颗粒粗盐变为细小颗粒或粉末,此时在实验室中需要用到的仪器为__________。
(2)操作②、④过滤后的滤液仍有浑浊,需要进行的操作是___________________。
(3)操作③按abc顺序依次加入过量的试剂。若a为NaOH溶液,则c为________。加入c发生反应的离子方程式为_________________________________________________。
(4)加盐酸调溶液pH的目的是________________________________。
(5)步骤⑥操作名称是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L
B.物质的量浓度为0.5 mol/L的MgCl2溶液中含有NA个Cl-
C.标准状况下,11.2 L H2O含有的分子数为0.5 NA
D.在常温常压下,1.06 g Na2CO3含有的Na+数为0.02 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学需用480 mL 0.5 mol·L-1Na2CO3溶液,在实验室进行配制。
I.(1)该同学用托盘天平应称量________g Na2CO3粉末,使用容量瓶前必须进行的一步操作是______。
(2)下图是该同学配制的一些关键步骤和操作图。
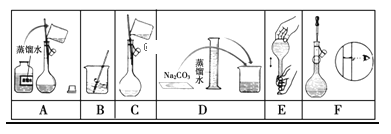
配制过程的先后顺序为(用字母A~F填写)________________。
Ⅱ.若配制1mol/L的稀硫酸溶液500mL
(1)则需要质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为___________mL(计算结果保留一位小数)。如果实验室有10mL 、25mL、50mL量筒,应选用_____________mL规格的量筒最好。
(2)下面操作造成所配稀硫酸溶液浓度偏高的是(_____)
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 溶液呈电中性,胶体带电荷。
B. 配制0.1 mol·L-1CuSO4溶液100 mL,称取1.6g硫酸铜晶体
C. 向饱和Ca(OH)2溶液中加入少量无水CaO固体,恢复原温度,溶液中Ca(OH)2的物质的量浓度不变
D. 制备Fe(OH)3胶体,可向沸水中滴加FeCl3饱和溶液并长时间煮沸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有下列5种离子中的某几种:![]() 。为确认溶液组成进行如下实验:
。为确认溶液组成进行如下实验:
(1)取1L上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀6.63g。向沉淀中加入过量的盐酸,有4.66g沉淀不溶。
(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体2.24L(已换算成标准状况,假定产生的气体全部逸出)。
已知:①![]() ②NH3是一种极易溶于水的碱性气体
②NH3是一种极易溶于水的碱性气体
由此可以得出关于原溶液组成的正确结论是
A.![]()
B.如果上述5种离子都存在,则![]()
C.一定存在![]() ,一定不存在K+
,一定不存在K+
D.一定存在![]() ,可能存在
,可能存在![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式的书写,正确的是
A. NH3·H2O==NH4+ + OH― B. H2SO4==2H+ + SO42―
C. CuCl2== Cu2+ + Cl― D. NaHCO3==Na+ + H+ + CO32―
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com