
【题目】化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应的热化学方程式是( )
2NH3的能量变化如图所示,该反应的热化学方程式是( )

A.N2(g)+3H2(g)2NH3(l) ΔH=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g)2NH3(g) ΔH=2(b-a)kJ·mol-1
C.N2(g)+H2(g)NH3(l) ΔH=(b+c-a)kJ·mol-1
D.N2(g)+H2(g)NH3(g) ΔH=(a+b)kJ·mol-1
【答案】A
【解析】由图示可知:(1)断裂 mol N2(g)和mol H2(g)中的化学键共吸收a kJ的能量,由1 mol N和3 mol H生成1 mol NH3(g)放出b kJ的能量,由1 mol NH3(g)变为1 mol NH3(l)放出c kJ能量;(2)由mol N2(g)和mol H2(g)生成1 mol NH3(g)或1 mol NH3(l)均放出能量。故有①N2(g)+H2(g)![]() NH3(g) ΔH=-(b-a)kJ·mol-1=(a-b)kJ·mol-1或②N2(g)+H2(g)
NH3(g) ΔH=-(b-a)kJ·mol-1=(a-b)kJ·mol-1或②N2(g)+H2(g)![]() NH3(l) ΔH=-(b+c-a)kJ·mol-1=(a-b-c)kJ·mol-1,因此C、D项均错误。将①式乘以2得:N2(g)+3H2(g)
NH3(l) ΔH=-(b+c-a)kJ·mol-1=(a-b-c)kJ·mol-1,因此C、D项均错误。将①式乘以2得:N2(g)+3H2(g)![]() 2NH3(g) ΔH=2(a-b)kJ·mol-1,B项错误;将②式乘以2得:N2(g)+3H2(g)
2NH3(g) ΔH=2(a-b)kJ·mol-1,B项错误;将②式乘以2得:N2(g)+3H2(g)![]() 2NH3(l) ΔH=2(a-b-c)kJ·mol-1,A项正确。
2NH3(l) ΔH=2(a-b-c)kJ·mol-1,A项正确。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如图所示。

(1)写出下列线段内发生反应的离子方程式,DC段________。
(2)原溶液中Mg2+、Al3+的物质的量浓度之比为____。
(3)图中C点表示当加入____ mol NaOH时,Al3+已经________,Mg2+已经______________。
(4)图中线段OA∶AB=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关漂白粉和漂白液的说法正确的是
A. 漂白粉是纯净物,漂白液是混合物 B. 漂白粉的有效成分是Ca(ClO)2
C. 工业上将氯气通入澄清石灰水制取漂白粉 D. 漂白液的有效成分是Na2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:AgOH很不稳定,易分解生成Ag2O(黑色)。溶液X中可能含有下列离子:Ag+,NH4+、Fe3+、SO42-、SO32-、Cl-中的几种离子。为了确定其组成,某同学进行了如下实验:
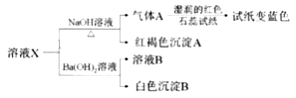
下列说法不正确的是( )
A. 溶液X与NaOH反应生成红褐色沉淀A,可推测该溶液中不存在SO32-
B. 溶液X中一定不含Ag+
C. 溶液X中一定存在NH4+、Fe3+、SO42-
D. 取少量溶液B,加入AgNO3溶液,若有沉淀产生,则有Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。 高铁电池的总反应为:3Zn +2K2FeO4+8H2O![]() 3Zn(OH)2 +2Fe(OH)3+4KOH
3Zn(OH)2 +2Fe(OH)3+4KOH
下列叙述不正确的是
A. 放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
B. 充电时阳极反应为:Fe(OH)3-3e-+5OH-= FeO42-+4H2O
C. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)硅在元素周期表中的位置是_______。
(2)工业生产粗硅的反应有:SiO2+2C![]() Si(粗)+2CO↑,SiO2+3C
Si(粗)+2CO↑,SiO2+3C![]() SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。
SiC+2CO↑。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为 。
(3)工业上可以通过如下图所示的流程制取纯硅:

①若反应I为 Si(粗)+3HCl![]() SiHCl3+H2,
SiHCl3+H2,
则反应II的化学方程式为 。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另 一种物质,写出该反应的化学方程式: 。
③假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应II中H2的利用率为93.75%,则在第二轮次的生产中,补充投入HCl 和H2的物质的量之比是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com