
| ||
| ||
| ||


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
| A、.18 | B、.36 |
| C、34.2 | D、.37.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
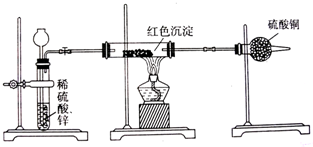
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 元素 | 结构或性质 | ||
| ① | A | 生活中最常见的金属,可被磁铁吸引 | ||
| ② | B | 原子最外层电子数是内层电子数的
| ||
| ③ | C | 形成化合物种类最多的元素之一,其单质为固体 | ||
| ④ | D | 地壳中含量最多的元素 | ||
| ⑤ | E | 与D同主族 | ||
| ⑥ | F | 与E同周期,且最外层电子数等于电子层数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元 素 | 有关信息 |
| A | 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | M层上有3个电子 |
| D | 短周期原子半径最大的主族元素 |
| E | E的氧化物是生活中最常见的液体,D、E同族 |
| F | A与B、F相邻,且A、B、E、F四种元素组成一种离子化合物丙,1mol丙含有10mol原子 |
| G | G、D同周期,G是所在周期元素非金属性最强的 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将样品配制成溶液V1 L,取其中25.00mL用标准KMnO4溶液滴定,消耗标准KMnO4溶液V2 mL |
| B、向样品中加足量H2O2,再加足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为bg |
| C、将样品与足量稀盐酸充分反应后,再加入足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为c g |
| D、将样品与足量稀盐酸充分反应,生成的气体依次通过盛有饱和NaHSO3的洗气瓶、盛有浓H2SO4的洗气瓶、盛有碱石灰的干燥管Ⅰ、盛有碱石灰的干燥管Ⅱ,测定干燥管Ⅰ增重d g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分别由Y、Z组成的单质一定都为原子晶体 |
| B、W与X形成的两种化合物中阴、阳离子的个数比均为1:2 |
| C、Y、Z、R最高价氧化物对应水化物的酸性强弱顺序:R>Z>Y |
| D、X的氢化物比R的氢化物稳定,X的氢化物熔沸点比R的氢化物高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
| B、长江三角洲的形成 |
| C、氯化铝溶液中加入NaOH溶液会产生白色沉淀 |
| D、盐水点豆腐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com