
下列解释事实的方程式不准确的是
A.用浓盐酸检验氨:NH3+HCl=NH4Cl
B.冷的氢氧化钠溶液吸收氯气: Cl2+2OH-= ClO-+Cl-+H2O
C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+
D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
用NA代表阿伏加德罗常数的数值,下列说法正确的是 ( )。
A.标准状况下,22.4 L CHCl3中含有的氯原子的数目为3NA
B.7 g CnH2n中含有的氢原子数目为NA
C.18 g D2O中含有的质子数目为10NA
D.0.5 mol·L-1 Na2CO3溶液中含有的CO32 -的数目为0.5NA
-的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的两个实验装置中,溶液的体积均为200 mL,开始时电解质溶液的浓度均为0.1 mol/L,工作一段时间后,测得导线上均通过0.02 mol电子,若不考虑溶液体积的变化,则下列叙述中正确的是 ( )
A.产生气体的体积:(1) > (2)
 B.电极上析出物质的质量:(1) > (2)
B.电极上析出物质的质量:(1) > (2)
C.溶液pH的变化:(1)增大,(2)减小
D.电极反应式:(1)中阳极:4OH--4e-===2H2O+O2↑,
(2)中负极:2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极实现电解,下列说法正确的是
A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变
B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小
C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2
D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了断裂某些化学键所需的能量:
| 化学键 | H—H | Cl-Cl | I—I | O==O | O—H | H-Cl | H—I |
| 断裂1 mol化学键所吸收的能量(kJ) | 436 | 247 | 151 | x | 463 | 431 | 299 |
请回答下列问题:
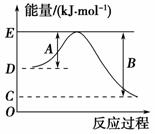
(1)如图表示某反应的能量变化关系图,此反应为________(填 “放热”或“吸热”)反应,其中ΔH=________kJ·mol-1(用含C和D的字母表示)。
(2)若此能量变化关系图表示反应H2(g)+ O2(g)===H2O(g)
O2(g)===H2O(g)
ΔH=-241.8 kJ·mol-1,则B=__________kJ·mol-1,x=
________。
(3)表示Cl2与HI气体反应生成碘蒸气与氯化氢的热化学方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是常见四种有机物的比例模型示意图。下列说法正确的是

A.甲能使酸性高锰酸钾溶液褪色
B.乙可与溴水发生取代反应使溴水褪色
C.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键
D.丁在常温下可与乙酸发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3 = K2O+5Na2O+16N2↑。若1 mol KNO3反应,则下列说法正确的是
A.N2是还原产物
B.KNO3被氧化
C.转移电子的物质的量为5 mol
D.被氧化的N原子的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某酸性溶液可能含有Br-、SO 、H2SO3、NH
、H2SO3、NH 等,分别对该溶液进行如下实验:
等,分别对该溶液进行如下实验:
①加热时放出的气体可使品红溶液褪色;
②加入碱溶液使溶液呈碱性,再加热时放出的气体可使湿润的红色石蕊试纸变蓝;
③加入氯水时,溶液略呈橙红色,再加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀。
对于下列物质不能确定其在原溶液中是否存在的是( )
A.Br- B.SO
C.H2SO3 D.NH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com