
用NA代表阿伏加德罗常数的数值,下列说法正确的是 ( )。
A.标准状况下,22.4 L CHCl3中含有的氯原子的数目为3NA
B.7 g CnH2n中含有的氢原子数目为NA
C.18 g D2O中含有的质子数目为10NA
D.0.5 mol·L-1 Na2CO3溶液中含有的CO32 -的数目为0.5NA
-的数目为0.5NA
科目:高中化学 来源: 题型:
氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
工业合成氨的热化学方程式是 。
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
| T / ℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
①ΔH(填“>”、“<”或“=”) 0。
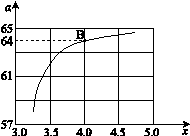
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比) ,右图是氨碳比(x)与CO2平衡转化率(α%)的关系。α随着x增大而增大的原因是 。
,右图是氨碳比(x)与CO2平衡转化率(α%)的关系。α随着x增大而增大的原因是 。
③ 上图中的B点处,NH3的平衡转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
安全是顺利进行实验及避免伤害和事故的保障。下列实验操作都正确但不是从实验安全角度考虑的是( )
|

① ② ③ ④
A.操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B.操作②:使用CCl4萃取溴水中的溴时,振荡后需打开活塞,使漏斗内气体放出
C.操作③:吸收氨气或氯化氢气体并防止倒吸
D.操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为 ( )。
A.3.2 g B.4.0 g C.4.2 g D.4.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在潜水艇中可用过氧化钠作为供氧剂。请选择适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化 钠可作供氧剂。
钠可作供氧剂。

①A是制取CO2的装置。写出A中发生反应的化学方程式:______________________________________。
②B中盛有饱和NaHCO3溶液,其作用是______________________________。
③写出过氧化钠与二氧化碳反应的化学方程式__________________________
_______________________________________________________________。
④D中盛放的试剂是________,其目的是_____________________________。
⑤试管F中收集满气体后,下一步实验操作是___________________________
________________________________________________________________。
(2)①某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗?____ ____,简要说明理由:___________________________________________
____,简要说明理由:___________________________________________
_________________________________________________________________。
②该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(图中铁架台等装置已略去)。

装置B的作用是_______________ ___________________________________,
___________________________________,
D的作用是_______________________________________________________。
③为确认反应产物,该同学设计了以下实验步骤,你认为合理的操作顺序是________(选填序号)。
A.用带火星的细木条靠近干燥管口a,观察细木条是否复燃
B.将C装置中反应后的固体物质溶于适量水配成溶液
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀
生成
查看答案和解析>>
科目:高中化学 来源: 题型:
测定1 mol氧气在标准状况下所占体积的实验操作的步骤如下:
①按下图装配实验装置。

②洗净试管然后充分干燥。
③向500 mL烧瓶里装满水,向500 mL烧杯里加入少量水,把连接烧瓶和烧杯的玻璃管A、橡皮管B和玻璃管C中也装满水,在中间不要留下气泡,然后用弹簧夹把橡皮管B夹紧。
④称得试管的质量为14.45 g,往试管里加入KClO3和MnO2的混合物,再称其质量为15.95 g。
⑤打开弹簧夹,把烧杯举起使烧瓶和烧杯中的水面一致,再关闭弹簧夹,然后把烧杯中的水倒掉。
⑥打开弹簧夹,加热试管的混合物到不再产生气体,即水不再流向烧杯时为止。
⑦反应完毕后把装置冷却到室温。
⑧调节烧杯的高度使烧瓶和烧杯中的水面一致,然后再关闭弹簧 夹。
夹。
⑨用500 mL量筒测量烧杯里水的体积为285.0 mL,把它换算为标准状况下氧气的体积为279.7 mL。
⑩再称量冷却后试管的质量为15.55 g。
(1)在操作⑦中,装置冷却时,玻璃管C的出口一直要在烧杯的水中,不能离开水面,其理由是__________________________________________________
_________________________________________________________________。
(2)简述操作⑧的必要性,即为什么要调节烧杯的高度,使烧瓶和烧杯中的水面一致?__________________________________________________________
______________________________________________________________ ___。
___。
(3)标准状况下,1 mol氧气所占的体积(保留小数后两位)为________L;混合物中MnO2的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O +O2+aOH-===Y+S4O
+O2+aOH-===Y+S4O +2H2O,下列说法中,不正确的是( )
+2H2O,下列说法中,不正确的是( )
A.a=4
B.Y的化学式为Fe2O3
C.S2O 是还原剂
是还原剂
D.每有1 mol O2参加反应,转移的电子为4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是 ( )
A.含有离子键的化合物一定是离子化合物
B.活泼的金属和活泼的非金属原子之间形成的化学键一定是离子键
C.共价化合物中不可能存在离子键
D.某元素原子最外层只有1个电子,它跟卤素可能形成离子键也可能形成共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的方程式不准确的是
A.用浓盐酸检验氨:NH3+HCl=NH4Cl
B.冷的氢氧化钠溶液吸收氯气: Cl2+2OH-= ClO-+Cl-+H2O
C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+
D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com