
【题目】工业上用洗净的废铜屑作原料来制备硝酸铜。为了节约原料和防止污染环境,宜采取的方法( )
A.![]()
B.![]()
C.![]()
D.![]()
【答案】B
【解析】
试题分析: A.Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O、CuSO4+Ba(NO3)2=BaSO4↓+Cu(NO3)2,该过程中生成有毒气体二氧化硫且浪费浓硫酸、硝酸钡,所以不符合条件,故A不选;B.2 Cu+O2
CuSO4+SO2↑+2H2O、CuSO4+Ba(NO3)2=BaSO4↓+Cu(NO3)2,该过程中生成有毒气体二氧化硫且浪费浓硫酸、硝酸钡,所以不符合条件,故A不选;B.2 Cu+O2![]() 2CuO、CuO+2HNO3=Cu(NO3)2+H2O,该反应中没有有毒气体生成,且能节约硝酸,所以符合条件,故B选;C.3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,NO有毒会污染环境,所以不符合条件,故C不选;D.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,二氧化氮有毒而污染环境,所以不符合条件,故D不选;故选B。
2CuO、CuO+2HNO3=Cu(NO3)2+H2O,该反应中没有有毒气体生成,且能节约硝酸,所以符合条件,故B选;C.3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,NO有毒会污染环境,所以不符合条件,故C不选;D.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,二氧化氮有毒而污染环境,所以不符合条件,故D不选;故选B。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】I、某化学兴趣小组利用以下装置模拟合成氨并制备少量氨水

已知:加热(85℃)NH4Cl和NaNO2饱和溶液可以制取N2
B中仪器名称是___________________;
⑵为了完成实验,装置从左到右接口的连接顺序是_____![]() ______;
______;
⑶D中玻璃纤维的作用是_________________;
⑷小组中甲同学认为F装置不太合理,实验中会产生倒吸。乙同学认真分析后认为该装置无需改进,他的理由是________________________;
II、实验探究
⑸该小组同学利用制备的氨水再进行银镜反应实验。经查阅资料,配制的银氨溶液主要成分是[Ag(NH3)2]OH,小组同学对其组成进行了如下实验探究:
①在洁净的小试管中加入2mL 2%的AgNO3溶液,然后边振荡试管边滴加2%的稀氨水溶液,至最初产生的沉淀恰好溶解为止,制得银氨溶液。
②在制得的银氨溶液中加入无水乙醇,溶液变浑浊,过滤,用__________洗涤,得到白色固体;
③将该白色固体用适量蒸馏水溶解,得到无色溶液,用广范pH试纸检验溶液近似呈中性;向溶液中逐滴加入稀盐酸至不再产生沉淀,静置,取上层清液于另一支放有一小片铜的小试管中并微热,发现铜片的表面有气泡产生,遇到空气变成红棕色;另取少量上层清液加过量的NaOH溶液并加热,得到无色刺激性气体。由此确定通过上述方法制备的白色固体主要成分是___________________;
⑹请根据以上探究,设计实验来制备少量纯净的[Ag(NH3)2]OH溶液:取2mL 2%的AgNO3溶液于洁净的小试管中,_________________,即得到[Ag(NH3)2]OH溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中![]() 减小
减小
B.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
C.稀醋酸中加入少量NaOH固体,溶液的导电性增强
D.向醋酸中加入氨水至中性,溶液中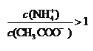
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列有关图象,说法正确的是( )
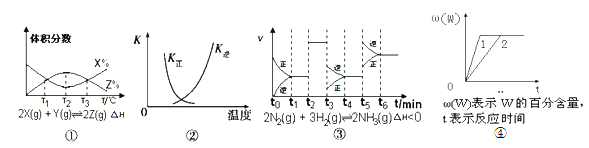
A. 由图①知,反应在T1、T3处达到平衡,且该反应的△H<0
B. 图②中曲线表示反应2SO2(g)+O2(g) ![]() 2SO3(g),ΔH<0的正、逆反应平衡常数K随温度的变化
2SO3(g),ΔH<0的正、逆反应平衡常数K随温度的变化
C. 由图③知,反应在t6时,NH3体积分数最大。
D. 其他条件不变时,图④中曲线表示不同压强对反应aX(g)+bY(s)![]() nW(g)的影响,且P1>P2,n=a+b。
nW(g)的影响,且P1>P2,n=a+b。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体充入2 L的密闭容器中,一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g)。若经2 s后测得C的浓度为0.6 mol ·L-1,下列几种说法正确的是
2C(g)。若经2 s后测得C的浓度为0.6 mol ·L-1,下列几种说法正确的是
①用物质A表示的反应平均速率为0.3 mol ·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol ·L-1·s-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol ·L-1
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,浓度均为0.1mol/L的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
回答下列问题:
(1)下列反应不能发生的是: ;
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+HClO=CO2↑+H2O+ClO-
d.2ClO-+CO2+H2O=CO32-+2HClO
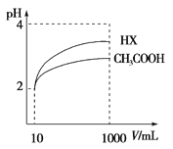
(2)体积为10 mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如右上图,则HX的电离平衡常数________(填“大于”、“等于”或“小于”)醋酸的平衡常数,写出HX的电离方程式 。
(3)某温度下,纯水中c (H+)=2.0×10-7 mol·L1, 0.9mol·L-1NaOH溶液与0.1mol·L-1HCl溶液等体积混合后(不考虑溶液体积变化),溶液的pH= 。
(4)等浓度等体积的CH3COONa和NaCN混合后,所得混合溶液中各离子浓度的大小关系是: 。
(5)某二元酸H2B在水中的电离方程式为H2B = H+ + HB— ;HB—![]() H++ B2—,则NaHB溶液显 (填“酸性”、“中性”或“碱性”)。
H++ B2—,则NaHB溶液显 (填“酸性”、“中性”或“碱性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8,下列说法不正确的是 ( )
A. 与W相邻的同主族元素可制成重要的半导体材料
B. X单质不可能置换出W单质
C. 元素原子半径从大到小的顺序是X、Y、Z
D. W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是HZO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 的说法正确的是( )
的说法正确的是( )
A.所有碳原子有可能都在同一平面上
B.最多只可能有9个碳原子在同一平面上
C.有7个碳原子可能在同一直线上
D.至少有6个碳原子在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是指直径从几纳米至几十纳米的材料,目前已广泛应用于催化剂及军事技术中,如果将纳米材料分散到液体分散剂中,所得混合物
A.不能透过滤纸 B.一定是浊液
C.一定是溶液 D.有丁达尔效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com