
【题目】(1)若反应2NO(g)+O2(g)![]() 2NO2的平衡常数为K1,2NO2(g)
2NO2的平衡常数为K1,2NO2(g)![]() N2O4(g)的平衡常数为K2,则反应2NO(g)+O2(g)
N2O4(g)的平衡常数为K2,则反应2NO(g)+O2(g)![]() N2O4(g)的平衡常数K=___。
N2O4(g)的平衡常数K=___。
(2)25℃、101KPa时,1Kg乙醇充分燃烧后放出的热量为29714kJ,则乙醇的燃烧热△H=__。
(3)反应mA+nB![]() pC在某温度下达到平衡。
pC在某温度下达到平衡。
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关是___。
②若C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向___方向移动。
③如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为__态。
【答案】K=K1×K2 △H=-1366.8kJ/mol m+n>P 逆 气
【解析】
根据影响化学平衡因素结合速率大小分析判断反应前后的体积变化;
(2)反应前后系数相同,改变压强平衡移动说明反应物中含有固体或纯液体;
(3)固体和纯液体对平衡无影响。
(1)若反应2NO(g)+O2(g)![]() 2NO2的平衡常数为K1=c2(NO2)/c2(NO)c(O2),2NO2(g)
2NO2的平衡常数为K1=c2(NO2)/c2(NO)c(O2),2NO2(g)![]() N2O4(g)的平衡常数为K2=c(N2O4)/c2(NO2),则反应2NO(g)+O2(g)
N2O4(g)的平衡常数为K2=c(N2O4)/c2(NO2),则反应2NO(g)+O2(g)![]() N2O4(g)的平衡常数K=c(N2O4)/c2(NO)c(O2)=K1×K2;答案:K=K1×K2;
N2O4(g)的平衡常数K=c(N2O4)/c2(NO)c(O2)=K1×K2;答案:K=K1×K2;
(2)25℃、101KPa时,1Kg乙醇充分燃烧后放出的热量为29714kJ,则1mol乙醇的燃烧放出的热量为29714kJ/(1000![]() )= 1366.8KJ。燃烧热是指1mol可燃物完全燃烧释放的热量,所以1mol乙醇的燃烧放出热量为1366.8kJ, 则乙醇的燃烧热△H=-1366.8KJ/mol;
)= 1366.8KJ。燃烧热是指1mol可燃物完全燃烧释放的热量,所以1mol乙醇的燃烧放出热量为1366.8kJ, 则乙醇的燃烧热△H=-1366.8KJ/mol;
(3) ①反应mA+nB![]() pC ,若A、B、C都是气体,减压后正反应速率小于逆反应速率,证明逆向反应是气体体积增大的反应,得到m+n>P ,因此,本题正确答案是m+n>P;
pC ,若A、B、C都是气体,减压后正反应速率小于逆反应速率,证明逆向反应是气体体积增大的反应,得到m+n>P ,因此,本题正确答案是m+n>P;
(2)若反应mA+nB![]() pC,C为气体,且m+n=P,在加压时化学平衡发生移动,说明AB中至少有一种是固体或纯液体,加压平衡逆向进行,
pC,C为气体,且m+n=P,在加压时化学平衡发生移动,说明AB中至少有一种是固体或纯液体,加压平衡逆向进行,
因此,本题正确答案是:逆;
(3)若反应mA+nB![]() pC,如果在体系中增加或减少B的量,平衡均不发生移动,证明B一定是固体或纯液体,不是气体;
pC,如果在体系中增加或减少B的量,平衡均不发生移动,证明B一定是固体或纯液体,不是气体;
因此,本题正确答案是:气。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某原电池构造如图所示,下列叙述正确的是( )

A. 在外电路中,电子由银电极流向铜电极
B. 取出盐桥后,电流表的指针仍发生偏转
C. 外电路中每通过0.1 mol电子,铜的质量理论上减小6.4 g
D. 原电池的总反应式为Cu+2AgNO3===2Ag+Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A. 甲烷的燃烧热△H=﹣890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3kJ/mol
B. 一定条件下,将0.5 molN2和1.5molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g)△H=﹣38.6kJ/mol
2NH3(g)△H=﹣38.6kJ/mol
C. 已知2C(s)+2O2(g) ═2CO2(g);△H1;2C(s)+O2(g)=2CO(g) △H2 则△H1>△H2
D. 在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3+5O2=4NO+6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mo1,则此反应的平均速率Vx为( )
A. VO2=0.01mo1L-1s-1B. VNO=0.008mo1L-1s-1
C. VH2O=0.002mo1L-1s-1D. VNH3=0.002mo1L-1s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)密闭容器中mA(g)+nB(g)![]() pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图。则:
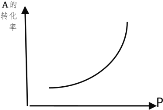
①增大压强,A的转化率___平衡向___移动,达到平衡后,混合物中C的浓度___。
②上述化学方程式中的系数m、n、p的正确关系是____。
③当降低温度时,C的浓度减小,正反应是___热反应。
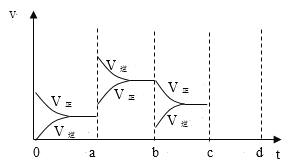
(2)如图表示在密闭容器中反应:2SO2(g)+O2(g)![]() 2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是___;b-c过程中改变的条件可能是____;若增大压强时,反应速度变化情况画在c-d处。___
2SO3(g)△H<0,达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a-b过程中改变的条件可能是___;b-c过程中改变的条件可能是____;若增大压强时,反应速度变化情况画在c-d处。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2SO2(g) + O2(g)![]() 2SO3(g) △H<0
2SO3(g) △H<0
①增加O2的浓度,平衡___移动,SO2的浓度___,SO3的物质的量___。
②增大压强,平衡___移动, SO2的浓度____,SO3的浓度___。
③升高温度,平衡____移动,SO2的浓度___,SO3的浓度____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电化学的叙述正确的是( )
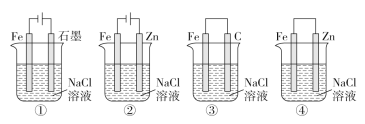
A. 图①两极均有气泡产生,滴加酚酞溶液时石墨一极变红
B. 图②装置中Fe电极参与反应发生腐蚀
C. 图③可以模拟钢铁的吸氧腐蚀,碳棒一极的电极反应式:O2+2H2O+4e-=4OH-
D. 上述4个装置中,图①、②中Fe腐蚀速率较快,图③中Fe腐蚀速率较慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】荣获2019年诺贝尔化学奖的吉野彰是最早开发具有商业价值的锂离子电池的日本科学家,他设计的可充电电池的工作原理示意图如图所示。该可充电电池的放电反应为LixCn+Li(1-x)CoO2=LiCoO2+nC。NA表示阿伏伽德罗常数的值。下列说法错误的是( )
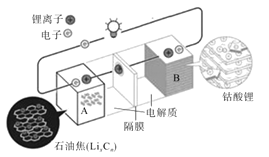
A.该电池用于电动汽车可有效减少光化学烟雾污染
B.充电时,正极反应为LiCoO2-xe-=Li(1-x)CoO2+xLi+
C.放电时,Li+由A极移向B极
D.若初始两电极质量相等,当转移2NA个电子时,两电极质量差为14g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种金属混合粉末15g,与足量的盐酸反应时生成11.2L H2(标况下),符合上述情况的金属混合物是( )
A. Mg、Fe B. Zn、Ag C. Fe、Zn D. Mg、Al
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com