
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入1.00mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如下图所示,试回答:
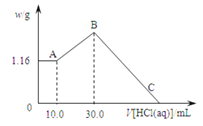
(1)A点的沉淀物的化学式为________________,
(2)原混合物中MgCl2的物质的量是__________mol,NaOH的物质的量是__________mol
(3)C点HCl溶液的体积为____________mL。
(4)写出A→B的离子方程式:_______________________________
【答案】 Mg(OH)2 0.02 0.13 130.0 AlO2-+H++H2O=Al(OH)3↓
【解析】(1)向所得悬浊液中逐滴加入1.00mol/L盐酸溶液时,0-A时没有沉淀生成,说明溶液中NaOH过量,溶液中铝离子完全转化为偏铝酸根离子,溶液中存在的沉淀为Mg(OH)2;(2)A点沉淀是氢氧化镁,物质的量是1.16g÷58g/mol=0.02mol,根据Mg原子守恒得n(MgCl2)=0.02mol;A-B段,盐酸和偏铝酸钠反应生成氢氧化铝沉淀,离子反应方程式为AlO2-+H++H2O=Al(OH)3↓,根据HCl的体积知,n(AlO2-)=n(HCl)=1mol/L×(0.03-0.01)L=0.02mol,根据铝原子守恒得n(AlCl3)=n(AlO2-)=0.02mol,由Na+离子和Cl-离子守恒得,原混合物中n(NaOH)=n(NaCl)=n(Cl-)=2n(MgCl2)+3n(AlCl3)+n(HCl)=0.02mol×2+0.02mol×3+0.03L×1mol/L=0.13mol;(3)C点溶液为MgCl2、AlCl3和NaCl混合液,C点所加盐酸用于中和原混合物中的NaOH,此时所加盐酸物质的量:n(HCl)=n(NaOH)=0.13mol;C点所表示盐酸的体积为:V=0.13mol÷1mol/L=0.13L=130mL;(4)A-B段,盐酸和偏铝酸钠反应生成氢氧化铝沉淀,离子反应方程式为AlO2-+H++H2O=Al(OH)3↓。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.高级脂肪酸甘油酯属于有机高分子化合物
B.紫外线、高温、酒精可杀菌消毒的原理是蛋白质变性
C.塑料、合成纤维、合成橡胶称为三大合成高分子材料
D.维生素C又称抗坏血酸,新鲜蔬菜中富含维生素C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血红蛋白中含有Fe2+ , 如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+转变成Fe3+ , 生成高铁血红蛋白而丧失与O2结合的能力,服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有()。
A.酸性
B.碱性
C.氧化性
D.还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于0.1mol/L H2SO4溶液的叙述错误的是( )
A.1L该溶液中含有H2SO4的质量为9.8g
B.0.5L该溶液中氢离子的物质的量浓度为0.2mol/L
C.从1L该溶液中取出100mL,则取出溶液中H2SO4的物质的量浓度为0.01mol/L
D.取该溶液10mL,加水稀释至100mL后H2SO4的物质的量浓度为0.01mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某反应aA(g)+bB(g)cC(g)△H=Q 在密闭容器中进行,在不同温度(T1和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w
A.与反应时间(t)的关系如图所示,下列判断正确的是( ) 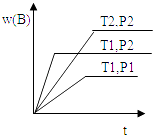
B.T1<T2 , P1<P2 , a+b>c,Q>0
C.T1>T2 , P1<P2 , a+b<c,Q>0
D.T1<T2 , P1>P2 , a+b<c,Q>0
E.T1<T2 , P1>P2 , a+b>c,Q<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】屠呦呦受“青蒿一握,以水二斤渍,绞取汁”启发,改用乙醚从青蒿中提取出抗疟疾药物青蒿素。青蒿素的提取过程不包含的操作是
A. 过滤B. 灼烧C. 蒸馏D. 萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的二氧化锰与40 mL 10 mol/L浓盐酸反应产生的氯气同0.1 mol二氧化锰与足量的浓盐酸反应产生的氯气相比( )
A. 前者产生的Cl2多 B. 后者产生的Cl2多
C. 一样多 D. 无法比较
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com