
【题目】人体血红蛋白中含有Fe2+ , 如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+转变成Fe3+ , 生成高铁血红蛋白而丧失与O2结合的能力,服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有()。
A.酸性
B.碱性
C.氧化性
D.还原性
科目:高中化学 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段.如图是硫元素的常见化合价与部分物质类别的对应关系:
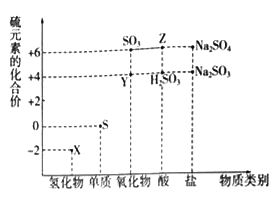
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______(填化学式).
(2)将X与Y混合,可生成淡黄色固体.该反应中氧化剂与还原剂的物质的量之比为_______.
(3)检验物质Y的方法是_______________________________.
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______.
(5)Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______(填代号).
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)已知Na2SO3能被K2Cr207氧化为Na2SO4则24mL 0.05molL﹣1的Na2SO3溶液与 20mL 0.02molL﹣1的溶液恰好反应时,Cr元素在还原产物中的化合价为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题日益成为制约国际社会经济发展的瓶颈.甲醇是一种可再生能源,具有广泛的开发和应用前景,因此甲醇被称为21世纪的新型燃料.
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图.
请回答下列问题: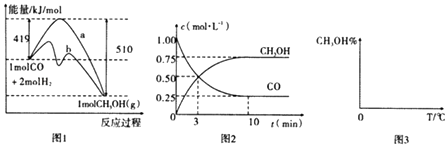
(1)在“图1”中,曲线(填“a”或“b”)表示使用了催化剂;该反应属于(填“吸热”或“放热”)反应.
(2)根据“图2”判断,下列说法不正确的是 .
A.起始充入的CO为1mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1mol CO和2mol H2 , 再次达到平衡时 ![]() 会增大
会增大
(3)从反应开始到建立平衡,v(H2)=;该温度下CO(g)+2H2(g)CH3OH(g)的化学平衡常数为 . 若保持其他条件不变,向平衡体系中再充入0.5mol CO、1molH2、1.5molCH3OH,此反应进行的方向为(填“正反应方向”或“逆反应方向)”.
(4)请在“图3”中画出平衡时甲醇蒸气百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出p1、p2 , 且p1>p2).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组在实验室用铜和硫酸为原料多种方法制取硫酸铜.制备方法如下:Ⅰ.方法一:
(1)浓硫酸试剂瓶上适合贴上的标签是(填序号).
(2)甲同学取6.4 g铜片和10 mL 18 molL﹣1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色沉淀.甲同学为了验证其中白色沉淀主要成分.设计下列实验:实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌.
实验现象:;
实验结论:所得白色固体的化学式为 .
(3)乙还观察到加热过程中,起初液面以上出现大量白色烟雾,在试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失.淡黄色固体消失的原因是(用化学反应方程式回答) . 直到最后反应完毕,发现试管中还有铜片剩余.乙根据自己所学的化学知识,认为试管中还有硫酸剩余.他这样认为的理由是 .
(4)Ⅱ.方法二:丙同学认为甲设计的实验方案不好,他自己设计的思路是:2Cu+O2 ![]() 2CuO,CuO+H2SO4═CuSO4+H2O.对比甲的方案,你认为丙同学的优点是① , ② .
2CuO,CuO+H2SO4═CuSO4+H2O.对比甲的方案,你认为丙同学的优点是① , ② .
(5)方法三:丁同学取一铜片和稀硫酸放在试管中,再向其中滴入双氧水,发现溶液逐渐呈蓝色.写出反应的化学反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下将2mol A和2mol B两种气体混合于2L密闭容器中,发生如下反应:3A(g)+B(g)2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,请填写下面空白:
(1)用B表示的平均反应速率为 , A的转化率为 .
(2)如果缩小容器容积(温度不变),则平衡体系中混合气体的密度 , 混合气体平均相对分子质量(填“增大”、“减少”或“不变”).
(3)若开始时只加C和D各 ![]() mol,要使平衡时各物质的物质的量原平衡相等,则还应加入mol B物质.
mol,要使平衡时各物质的物质的量原平衡相等,则还应加入mol B物质.
(4)若向原平衡体系再投入1mol A和1mol B,平衡(填“右移、左移或不移”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题
(1)KAl(SO4)2的电离方程式_______________________。
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是______________、_________________ (填微粒符号)。
(3)实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取_______________ml该浓盐酸。
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L(标况) SO2时,转移的电子是__________mol。
(5)下列四个图像中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。
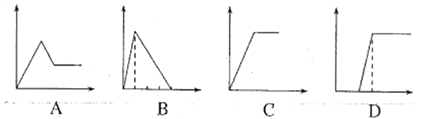
溶液 | 加入的物质 | 序号 |
①AlCl3溶液 | 通入过量的NH3 | ___ |
②Na2CO3和NaOH的溶液 | 滴入过量的盐酸 | ___ |
③NaAlO2溶液 | 滴加稀硫酸至过量 | ___ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应A(g)+3B(s)2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是( )
A.υ(A)=0.5mol/(Lmin)
B.υ(B)=1.2mol/(Ls)
C.υ(C)=0.1mol/(Ls)
D.υ(D)=0.4mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入1.00mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如下图所示,试回答:
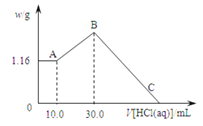
(1)A点的沉淀物的化学式为________________,
(2)原混合物中MgCl2的物质的量是__________mol,NaOH的物质的量是__________mol
(3)C点HCl溶液的体积为____________mL。
(4)写出A→B的离子方程式:_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面关于金属钠的描述不正确的是( )
A. 钠是电和热的良导体
B. 将Na投入盐酸中,Na先与水反应,生成的NaOH再与HCl反应
C. 钠的化学性质很活泼,在自然界里不能以游离态存在
D. 钠和钾的合金在室温下呈液态,可做原子反应堆的导热剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com