
| 选项 | 离子或物质 | 条件 |
| A | Na+、K+、Cl-、SO42- | c(Na+)+c(K+)=c(SO42-)+ c(Cl-) |
| B | Fe3+、SO32-、Cl- | 加入NaOH溶液,产生红褐色沉淀 |
| C | Ba+、HCO3-、Cl-、H+ | 加入氨水产生沉淀 |
| D | SO2、O2、NO2 | 通入足量NaOH溶液后,可能会没有任何气体剩余 |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源:不详 题型:单选题
| A.甲基橙呈红色的溶液中:I-、Cl-、NO3-、Na+ |
| B.石蕊呈蓝色的溶液中:Na+、AlO2-、NO3-、HCO3- |
| C.含大量Al3+的溶液中:K+、Na+、NO3-、ClO- |
| D.含大量OH一的溶液中:CO32-、Cl-、F-、K+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
| B.等体积的pH都为3的酸HA和HB分别与足量的Mg反应,HA放出的H2多,说明酸性:HA>HB |
| C.常温下,弱酸酸式盐NaHA溶液的pH=6,说明HA?的电离程度大于其水解程度 |
| D.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓度均为0.1mol?L—1的CH3COOH和CH3COONa溶液等体积混合所得的溶液中: c(CH3COOH)+c(CH3COO—)=0.2mol?L-1 |
| B.0.1mol?L-1NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2(CO32-) |
| C.0.2mol?L-1HCl溶液与等体积0.1mol?L-1NaOH溶液混合后,溶液的pH=1 |
| D.0.1mol?L-1氨水中滴入0.1mol?L-1盐酸至溶液呈中性时,混合溶液中:c(NH4+)=c(Cl—) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.滴人甲基橙显红色的溶液中:NH4+、Ba2+、AlO—2、CI— |
B.Kw/c( H+) =0.l mol/L的溶液:Na+、K+、Si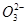 、HC 、HC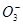 |
C.含有较多S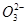 '的溶液:H+、Ca2+、Fe3+、N '的溶液:H+、Ca2+、Fe3+、N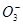 |
D.澄清透明溶液中:K+、M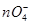 、H3O+、SO42― 、H3O+、SO42― |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
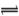 X2—+H+。回答下列问题:
X2—+H+。回答下列问题: (2)在25℃下,向浓度均为0.1 mol·L—1的FeCl3和AlCl3混合溶液中逐滴加入氨水,先生成 (填化学式)沉淀。已知25℃时Ksp[Fe(OH)3]=2.6×10—39 mol4·L—4,KsP[Al(OH)3]=1.3×10—33 mol4·L—4。
(2)在25℃下,向浓度均为0.1 mol·L—1的FeCl3和AlCl3混合溶液中逐滴加入氨水,先生成 (填化学式)沉淀。已知25℃时Ksp[Fe(OH)3]=2.6×10—39 mol4·L—4,KsP[Al(OH)3]=1.3×10—33 mol4·L—4。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
 SO42-+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72-转移__________mol e-。
SO42-+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72-转移__________mol e-。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
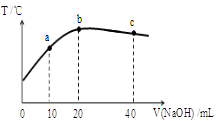
| A.醋酸的电离平衡常数:b点>a点 |
| B.由水电离出的c(OH—):b点>c点 |
| C.从a点到b点,混合溶液中可能存在:c(CH3COO—)= c(Na+) |
| D.b点到c点,混合溶液中一直存在:c(Na+)>c(CH3COO—)>c(OH—)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解精炼铜时,转移1mol电子,阳极上溶解的铜原子数必为0.5NA |
| B.常温下,4.4gCO2和N2O混合物中所含有的原子数为0.3×6.02×1023 |
| C.等体积0.2mol·L-1HCl溶液与0.05mol·L-1Ba(OH)2溶液混合后,溶液的pH=1 |
| D.溶液中由水电离出的c(H+)=1×10-12mol/L,SO42-、NO3-、Fe2+、Mg2+能大量共存 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com