
下列过程中不涉及氧化还原反应的是
| A.由植物油制备人造黄油 |
| B.用氯化铁溶液腐蚀印刷线路板 |
| C.用牺牲阳极的阴极保护法防止金属被腐蚀 |
| D.在蛋白质溶液中加入饱和硫酸铵溶液,析出白色固体 |
科目:高中化学 来源: 题型:单选题
水是生命之源,也是化学反应中的主角。请回答下列问题:
I.水是一种电解质,发生电离会产生电子总数相同的两种微粒,其电离方程式为 。
Ⅱ.在许多反应中H2O扮演不同的“角色”。请结合所学知识,写出有关反应的化学方程式或离子方程式。
(1)H2O参与置换反应,符合X+W→Y+V:
已知X和Y分别是短周期主族元素形成的两种单质, W、V是化合物。
①W是水,作还原剂,该反应的化学方程为 ;
②V是水,化学方程式为 。
(2)水在氧化还原反应既不是氧化剂也不是还原剂:
A、B是中学化学常见的两种由短周期元素组成的有色气体,它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,写出A、B与水反应的化学方程式:
①A + H2O ;
②B + H2O ;
(3)某物质化学式为NH5,常温下是固态,能与水剧烈反应放出两种气体。在NH5中的各原子均具有稀有气体的稳定结构,则下列对NH5与水的反应描述正确的是 (填选项)。
A.NH5与水反应时,NH5是氧化剂
B.NH5与水反应时,NH5既是氧化剂又是还原剂
C.NH5与水反应时,NH5是还原剂
D.NH5与NH3溶于水后溶液均呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知:①向盛有稀H2SO4试管中加入Fe粉,Fe粉完全溶解得浅绿色溶液;
②向实验①浅绿色溶液中滴加NaOH溶液,生成白色沉淀并立即变为红褐色;
③向实验②红褐色沉淀中滴加溶有淀粉的HI溶液,红褐色沉淀溶解得蓝色溶液。
下列判断正确的是
| A.上述实验中,共涉及四个氧化还原反应 |
| B.实验可证明还原性:H+>Fe2+>OH->I- |
| C.实验②可证明溶解度:Fe(OH)3>Fe(OH)2 |
| D.实验③中,反应的离子方程式是:2Fe(OH)3+2I-+6H+=2Fe2++I2+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
反应①和②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2。下列说法正确的是
| A.两个反应中均为硫元素被氧化 |
| B.碘元素在反应①中被还原,在反应②中被氧化 |
| C.氧化性:MnO2>SO42->IO3->I2 |
| D.反应①、②中生成等量的I2时转移电子数比为1︰5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
三氟化氮(NF3)是一种无色无味的气体,它是氨和氟(F2)在一定条件下直接反应得到:4NH3+3F2=NF3+3NH4F,下列有关NF3的叙述正确的是( )
| A.NF3的氧化性比F2强 |
| B.NF3的还原性比NH3强 |
| C.NF3中的原子最外层均达8电子 |
| D.该反应过程转移了6 mol电子。 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
制备食用碘盐(KIO3)原理之一为:I2 +2KClO3 Cl2 +2KIO3,下列说法正确的是
Cl2 +2KIO3,下列说法正确的是
| A.KClO3和KIO3均属于离子化合物,只含有离子键 |
| B.反应过程中I2置换出Cl2,由此可推断非金属性I>Cl |
| C.为防止反应的尾气造成大气污染,可以用饱和食盐水吸收尾气 |
| D.制备KIO3的反应中I2被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知P单质在KOH溶液中的变化是:4P+3KOH+3H2O=3KH2PO2+PH3↑,下列说法正确的是
| A.产物PH3分子中所有的原子可能共平面 |
| B.该反应中P做还原剂,H2O做氧化剂 |
| C.相关元素的第一电离能的大小顺序:S>P>Si |
| D.该反应每发生0.3摩尔电子转移,PH3分子中就有0.3摩尔P-H键形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(14分)镍是一种十分重要的有色金属,但粗镍中一般含有Fe、Cu及难与酸、碱溶液反应的不溶性杂质而影响使用。现对粗镍进行提纯,具体的反应流程如下:
已知:
①2Ni2O3(黑色)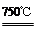 4NiO(暗绿色) + O2↑
4NiO(暗绿色) + O2↑
②
| 物质 | CuS | Cu(OH)2 | Ni(OH)2 | NiS |
| Ksp | 8.8×10-36 | 2.2×10-20 | 5.48×10-16 | 3.2×10-19 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com