
制备食用碘盐(KIO3)原理之一为:I2 +2KClO3 Cl2 +2KIO3,下列说法正确的是
Cl2 +2KIO3,下列说法正确的是
| A.KClO3和KIO3均属于离子化合物,只含有离子键 |
| B.反应过程中I2置换出Cl2,由此可推断非金属性I>Cl |
| C.为防止反应的尾气造成大气污染,可以用饱和食盐水吸收尾气 |
| D.制备KIO3的反应中I2被氧化 |
科目:高中化学 来源: 题型:单选题
向仅含Fe2+、I-、Br-的溶液中通入适量氯气,溶液中这种离子的物质的量随消耗氯气物质的量的变化如图所示。下列说法中正确的是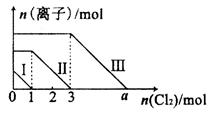
| A.线段III代表Fe2+的变化情况 |
| B.线段I代表Br-的变化情况 |
| C.a值等于6 |
D.原混合溶液中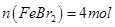 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应:
3NF3+5H2O→2NO+HNO3+9HF。下列有关该反应的说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.NF3是极性分子,在潮湿空气中泄漏会看到红棕色气体 |
| C.若生成1 mol HNO3,则转移2NA个电子 |
| D.每消耗0.2mol氧化剂,可收集到5.418L气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列过程中不涉及氧化还原反应的是
| A.由植物油制备人造黄油 |
| B.用氯化铁溶液腐蚀印刷线路板 |
| C.用牺牲阳极的阴极保护法防止金属被腐蚀 |
| D.在蛋白质溶液中加入饱和硫酸铵溶液,析出白色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在熔融KOH中大气中的氧可将铬铁矿FeCr2O4中Fe和Cr的化合价都转化为+6价,氧化 1 mol FeCr2O4在理论上需要多少摩尔氧气
| A.2mol | B.2.5mol | C.3mol | D.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学在日常生活中具有广泛的应用,下列应用中不涉及氧化还原反应原理的是
| A.用明矾[KAl(SO4)2·12H2O]净水 | B.海水中提取溴 |
| C.交警用CrO3检验司机是否酒后驾驶 | D.医务室用双氧水消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将1.95g锌粉加入到200mL的0.100 mol·L-1MO2+溶液中,恰好完全反应,则还原产物可能是( )
| A.M | B.M2+ | C.M3+ | D.MO2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知BrFn与水按3:5物质的量比反应,生成HF、HBrO3、O2和Br2,且O2和Br2物质的量相等.请回答:
(1)n= (2)氧化产物是 (3)1mol水可还原 mol BrFn?
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氢气还原氧化铜所得的红色固体可能是铜与氧化亚铜的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和Cu。
(1)现有8.4克氧化铜被氢气完全还原后,得到红色固体6.96克,其中含单质铜与氧化亚铜的物质的量之比是 ;
(2)若将6.96克上述混合物与足量的浓硝酸充分反应:
①生成标准状况下1.568升的气体(不考虑NO2的溶解,也不考虑NO2与N2O4的转化),则该气体的成分是 ,其物质的量之比是 ;
②把得到的溶液小心蒸发浓缩,把析出的晶体过滤,得晶体20.328g。经分析,原溶液中的Cu2+有20%残留在母液中,所得晶体的化学式为 。
(3)Cu、Cu2O和CuO组成的混合物,加入100mL 0.6mol/L HNO3溶液恰好使混合物完全溶解,同时收集到224mL NO气体(标准状况)。如原混合物中Cu的物质的量为X,求其中Cu2O、CuO的物质的量及X的取值范围(写出解题过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com