
【题目】新型超高能材料是国家核心军事力量制高点的重要标志,高性能炸药BNCP的结构如图,回答下列问题:
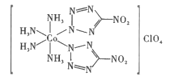
(1)BNCP中Co3+的基态价层电子轨道表示式是__,Co3+的配位数是__,阴离子ClO4-的中心原子杂化类型是__。
(2)1mol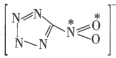 配体中的σ键的数目是__,已知该配体是平面结构,图中标记的N原子与O原子之间的σ键是由N原子的__杂化轨道与O原子的__轨道重叠形成的。
配体中的σ键的数目是__,已知该配体是平面结构,图中标记的N原子与O原子之间的σ键是由N原子的__杂化轨道与O原子的__轨道重叠形成的。
(3)比较NO2+、NO2、NO2-的键角大小:__,与NO2-互为等电子体的单质是___。
(4)比较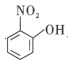 、
、![]() 的沸点并说明理由:__。
的沸点并说明理由:__。
(5)比较H2O与OF2的极性大小并说明理由:__。
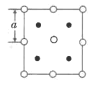
(6)2018年南京理工大学胡炳成团队合成全国首个全氮阴离子,全氮阴离子的盐AgN5的晶体结构中:N5-采取面心立方最密堆积,Ag+填在正四面体空隙中,从晶胞上方的俯视投影图如图。每个晶胞中含有的N5-的数目是__。Ag+与N5-最近的距离是__(用a表示)。
【答案】![]() 6 sp3 8NA sp2 2p NO2+>NO2>NO2- O3
6 sp3 8NA sp2 2p NO2+>NO2>NO2- O3 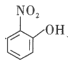 <
<![]() H2O的极性大于OF2,H2O和OF2都是V形结构,H和O的电负性的差值大于O和F之间的电负性差值,则H2O的极性更大 4
H2O的极性大于OF2,H2O和OF2都是V形结构,H和O的电负性的差值大于O和F之间的电负性差值,则H2O的极性更大 4 ![]() a
a
【解析】
(1)根据价层电子轨道排布方式写出轨道表示式,由结构图可知Co3+的配位数,根据价层电子对互斥理论的杂化轨道计算公式得到ClO4-的杂化方式;
(2)每两个原子之间形成1个σ鍵,因为是平面结构,所以是N的sp2杂化轨道与O的2p轨道重叠形成σ键;
(3)NO2+是直线型结构,键角为180°,NO2和NO2-是sp2杂化V型结构,键角约为120°,其中NO2的N原子的其中一个杂化轨道上含一个单电子,NO2-的N原子杂化轨道上含一对电子,则排斥力更大,键角更小;
(4)苯环上羟基位置不同会形成不同种类的氢键,从而影响物质的沸点;
(5) H2O与OF2分子结构相似,比较O与H和F的电负性差值的相对大小进行判断;
(6)由图计算每个晶胞中含有的N5-的数目;该结构类似四方ZnS的结构,因此可以求算品胞中的离子数与阴阳离子的最近距离。
(1)Co为27号元素,Co3+核外有24个电子,基态价层轨道表示式为![]() ,由结构图可知Co3+的配位数为6,根据价层电子对互斥理论的杂化轨道计算公式得到ClO4-的杂化方式为sp3杂化;
,由结构图可知Co3+的配位数为6,根据价层电子对互斥理论的杂化轨道计算公式得到ClO4-的杂化方式为sp3杂化;
(2)每两个原子之间形成1个σ鍵,由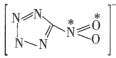 结构图可知,1mol配体中的σ键有8mol,即数目为8NA,因为是平面结构,所以是N的sp2杂化轨道与O的2p轨道重叠形成σ键;
结构图可知,1mol配体中的σ键有8mol,即数目为8NA,因为是平面结构,所以是N的sp2杂化轨道与O的2p轨道重叠形成σ键;
(3)NO2+是直线型结构,键角为180°,NO2和NO2-是sp2杂化V型结构,键角约为120°,其中NO2的N原子的其中一个杂化轨道上含一个单电子,NO2-的N原子杂化轨道上含一对电子,则排斥力更大,键角更小,所以三者键角大小关系为:NO2+>NO2>NO2-;1个NO2-有3个原子,核外有24个电子,与NO2-互为等电子体的单质是O3;
(4) 存在分子内氢键,而
存在分子内氢键,而![]() 存在分子间氢键,沸点更高;
存在分子间氢键,沸点更高;
(5)H2O的极性大于OF2,H2O和OF2都是V形结构,H和O的电负性的差值大于O和F之间的电负性差值,则H2O的极性更大;
(6)由图计算每个晶胞中含有的N5-的数目为4![]() +4
+4![]() +1=4;该结构类似四方ZnS的结构,因此可以求算品胞中的Ag+与N5-最近的距离是
+1=4;该结构类似四方ZnS的结构,因此可以求算品胞中的Ag+与N5-最近的距离是![]() =
=![]() a。
a。


科目:高中化学 来源: 题型:
【题目】某学习小组为了探究碳与浓H2SO4反应的产物,将浓H2SO4和木炭反应产生的气体进行以下实验:
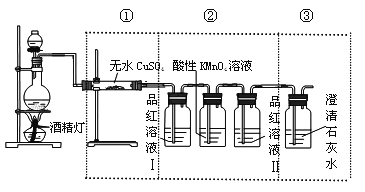
(1)气体通过无水硫酸铜,固体变蓝。说明气体中含有__________;
(2)气体通入品红溶液,溶液褪色;微热,溶液恢复红色。说明气体中含有__________(填“SO2”或“CO2”);
(3)气体通入足量的澄清石灰水,产生白色沉淀。该小组认为气体中含有CO2,你认为该结论:__________(填“正确”或“不正确)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铅蓄电池的工作原理为Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l),现用如图1装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:
2PbSO4(s)+2H2O(l),现用如图1装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时,铁电极的质量减少11.2g。请回答下列问题:
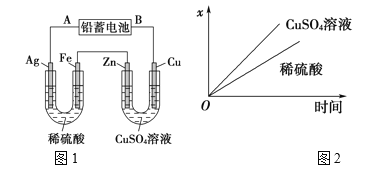
(1)A是铅蓄电池的________极,铅蓄电池正极反应式为:______。
(2)Ag电极的电极反应式是______,该电极的电极产物共________g。
(3)Cu电极的电极反应式是________,CuSO4溶液的浓度_______(填“减小”“增大”或“不变”)。
(4)如图2表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示_______。
a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X与其他元素均不在同周期,W的M层电子数是K层的2.5倍,ZX2是一种储氢材料,液态Y的简单氢化物可用作制冷剂。下列叙述错误的是( )
A.非金属性:Y>W
B.等物质的量的W4与CH4共价键数目不同
C.X、Y的单质在催化剂作用下化合的过程可以表示为:![]()
D.Z的单质在空气中燃烧会生成Z3Y2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B和C为常见气体,A是所有气体中密度最小的气体;B是黄绿色气体;C能使湿润的红色石蕊试纸变蓝。D是目前用量最大,用途最广的金属。请回答下列问题:
(1)A是________(填化学式)
(2)实验室制取C时,常用________(填“向下”或“向上”)排空气法收集;
(3)B与D的单质在点燃条件下反应的化学方程式为______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3溶液中存在水解平衡:CO32-+H2O![]() HCO3-+OH-。下列说法错误的是( )
HCO3-+OH-。下列说法错误的是( )
A.加水稀释,溶液中所有离子的浓度都减小B.通入CO2,溶液pH减小
C.加入NaOH固体,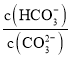 减小D.升高温度,平衡常数增大
减小D.升高温度,平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶解氧(指溶解在水体中氧气分子)是衡量水质的一个重要指标。为测定某水样中溶解氧含量(ρ=![]() )设计了如下实验方案。实验步骤如下:
)设计了如下实验方案。实验步骤如下:
步骤1:水样的采集与固定
用水样瓶准确量取100mL的待测水样(不能留有气泡),并用针筒向水样下方快速注入2.0mLMnSO4溶液和3.0mL碱性KI溶液,盖好瓶盖,上下颠倒摇匀,此时生成Mn2+在碱性条件下被水中的氧气氧化为MnOOH棕色沉淀,静置至澄清。
步骤2:碘的游离
向水样瓶中加入3.0mL浓硫酸,使I-在酸性条件下被MnOOH氧化为I2,同时MnOOH被还原Mn2+,待沉淀完全溶解后,将它们全部转移到250mL锥形瓶中。
步骤3:碘的滴定
向锥形瓶中加入少量淀粉溶液,再滴加0.005mol·L-1的Na2S2O3标准溶液,恰好完全反应时,消耗Na2S2O3标准溶液的体积为16mL。(已知:I2+2S2O32-=2I-+S4O62-)
(1)MnOOH中Mn元素的化合价是___。
(2)写出步骤2中所发生反应的离子方程式___。
(3)若待测水样中留有气泡,则测定结果将___。(填“偏大”、“偏小”或“无影响”)
(4)计算该水样中溶解氧的含量ρ(以mg·L-1表示),并写出计算过程:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛在航天、潜海和医疗方面应用广泛。以钛铁矿[主要成分为钛酸亚铁(FeTiO3),含少量Fe2O3]为原料制备钛的工艺流程如图所示。
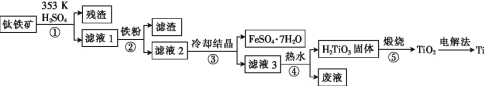
(1)步骤②、③、④中,均需进行的操作是____(填操作名称)。
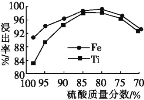
(2)滤液1中钛元素以TiO2+形式存在,步骤①中生成TiO2+的化学方程式为____,硫酸质量分数对钛、铁浸出率的影响如图所示,据此判断,酸浸时所加硫酸的质量分数应为____(填范围)。
(3)请结合离子方程式解释步骤④中加热水的原因:____。
(4)电解法制备Ti的装置是以石墨为阳极,TiO2为阴极,熔融CaO为电解质。Ti在___(填“阳极”或“阴极”)生成,____(填“能”或“不能”)将熔融CaO换成石灰乳。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。下列判断正确的是

A. e、f两管中的试剂可以分别是浓氨水和NaOH固体
B. 玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
C. c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
D. Y形管乙中产生的为氧化性气体,将BaSO3氧化为BaSO4沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com