
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g) 经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g) 经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50 s的平均速率为v (PCl3) = 0.0032 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时,c(PCl3) = 0.11 mol·L-1,则反应的ΔH < 0
C.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,达到平衡前v (正) < v (逆)
D.相同温度下,起始时向容器中充入2.0 mol PCl5,达到平衡时PCl5的转化率小于20%
【答案】D
【解析】
A由表中数据可知50s内:△n(PCl3)=0.16mol,v(PCl3)= =0.0016mol·L-1·s-1,A错误;
=0.0016mol·L-1·s-1,A错误;
B.由表中数据可知,平衡时n(PCl3)=0.20mol,保持其他条件不变,升高温度,再次平衡时c(PCl3)=0.11mol·L-1,则n′(PCl3)=0.11mol/L2L=0.22mol,说明升温平衡向正向移动,所以正反应为吸热反应,反应的ΔH>0,B错误;
C.对于该反应,根据表中数据可有:

所以平衡常数K=![]() =0.025;相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,则起始时PCl5、PCl3和Cl2的浓度分别为0.5mol·L-1、0.10mol·L-1和0.10mol·L-1,浓度商Qc=
=0.025;相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,则起始时PCl5、PCl3和Cl2的浓度分别为0.5mol·L-1、0.10mol·L-1和0.10mol·L-1,浓度商Qc=![]() =0.02,Qc<K,说明平衡向正反应方向移动,v(正)>v(逆),C错误;
=0.02,Qc<K,说明平衡向正反应方向移动,v(正)>v(逆),C错误;
D.相同温度下,起始时向容器中充入2.0molPCl5,与原平衡相比,压强增大,平衡向逆反应方向移动,平衡时PCl5的转化率较原平衡低,D正确。
答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】人造空气(氧气与氦气的混合气)可用于减轻某些病痛或供深水潜水员使用。标准状况下,5.6 L“人造空气”的质量是2.4 g,其中氧气与氦气的质量比是( )
A. 1∶1 B. 2∶1 C. 1∶4 D. 2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 广泛存在于天然气等燃气及废水中,热分解或氧化
广泛存在于天然气等燃气及废水中,热分解或氧化![]() 有利于环境保护并回收硫资源。
有利于环境保护并回收硫资源。
(1)Binoist等进行了![]() 热分解实验:
热分解实验:![]() ,开始时,
,开始时,![]() 与
与![]() 的体积比为1:19.在压强为
的体积比为1:19.在压强为![]() 下测得在三种不同温度下
下测得在三种不同温度下![]() 的转化率如图1所示.
的转化率如图1所示.
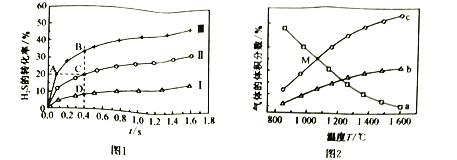
![]() 分解反应的
分解反应的![]() ______________(填“>”或“<”)0,A、B、C、D四点中:
______________(填“>”或“<”)0,A、B、C、D四点中:![]() 最大的是__________________,
最大的是__________________,![]() 最大的是___________,容器中
最大的是___________,容器中![]() 的分压由大到小的关系是__________________。
的分压由大到小的关系是__________________。
(2)当![]() 与
与![]() 混合,在
混合,在![]() 及不同温度下反应达平衡时
及不同温度下反应达平衡时![]() 及
及![]() 的体积分数如图2所示。图中b表示的物质是___________,M点时,反应
的体积分数如图2所示。图中b表示的物质是___________,M点时,反应![]() 的平衡常数
的平衡常数![]() ____________________
____________________![]() (
(![]() 为以分压表示的平衡常数,保留两位小数)
为以分压表示的平衡常数,保留两位小数)
(3)用氯气除去废水中![]() 的反应为
的反应为![]() ,该反应的可能机理如下:
,该反应的可能机理如下:
a.![]() 慢 b.
慢 b.![]() 快
快
![]() 快
快 ![]() 慢
慢
![]() 快
快 ![]() 快
快
c.![]() 慢 d.
慢 d.![]() 快
快
![]() 快
快 ![]() 慢
慢
①机理a的中间体为______________________。
②已知![]() ,
,![]() 为正反应速率,k为速率常数,上述机理中与该速率方程一致的是_________________________(填字母)。
为正反应速率,k为速率常数,上述机理中与该速率方程一致的是_________________________(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。
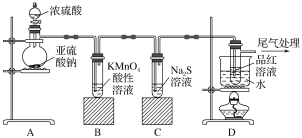
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是________,其中发生反应的化学方程式为_____。
(2)实验过程中,装置B、C中发生的现象分别是_____、 ____,这些现象分别说明SO2具有的性质是____和____。
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_________。
(4)尾气可采用________溶液吸收。(写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求用系统命法写出下列物质名称或结构简式
(1)用系统命法命名
①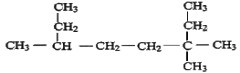 _________。
_________。
② 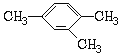 _________________。
_________________。
(2)顺-2-丁烯的结构简式为:____________。
(3)3-甲基-1-丁烯的结构简式为:_____________。
(4)2,2,3,3-四甲基戊烷的结构简式为:____________
(5)分子式为C5H10、核磁共振氢谱中只有一个峰的烃的结构简式_______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是第四周期ⅤA族元素,可以形成As2O3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________。该反应需要在加压下进行,原因是________。
(3)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:AsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。
AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是__________(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)不再变化
d. c(I)=y mol·L1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
(1)基态O原子核外电子排布式为_______,基态Fe2+核外未成对电子数为_______,基态P原子核外占据最高能级的电子云轮廓图为_________形;
(2)比较大小(填“大于”、“小于”或“等于”):
①沸点:NH3_____PH3 ;②第一电离能:I1(P)_____I1(O)。
(3)PO43的空间构型是______,P原子的杂化形式为______,在1molPO43中含σ键______个。
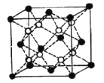
(4)Li2O的晶胞如图所示(其中白球代表Li,黑球代表O)。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为______g·cm3(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com