
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源:不详 题型:填空题
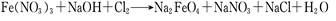
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 将反应后得到黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| Ⅱ | 向实验I中得到的溶液滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
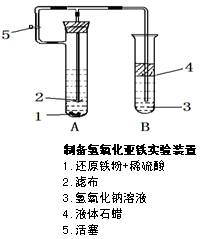
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
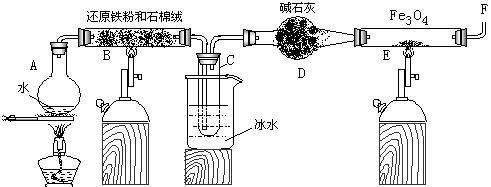
 Fe3O4 +4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释
Fe3O4 +4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Cu+SO2
2Cu+SO2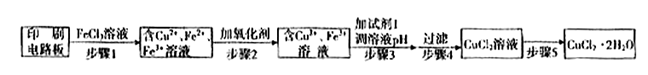 ①证明步骤I所加FeCl3溶液过量的方法是 。
①证明步骤I所加FeCl3溶液过量的方法是 。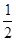 O2(g)==H2O(l) △H3=-286kJ/mol
O2(g)==H2O(l) △H3=-286kJ/mol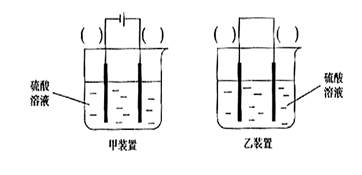
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 的量浓度为 .
的量浓度为 .查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu和SO2 | B.Cu和S | C.CuO和SO2 | D.Cu2O和S |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.把硝酸亚铁溶液与稀盐酸混合,因不符合复分解反应进行到底的条件,所以它们不能发生化学反应 |
| B.分液实验操作时,下层液体从下端放出,上层液体从上口倒出 |
| C.氢氧化钠固体应保存在带有橡胶塞的广口瓶里 |
| D.凡是有元素化合价升降的化学反应都是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com