
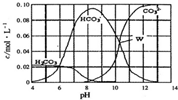
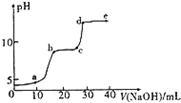
 25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1L 的溶液,溶液中部分微粒与pH的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1L 的溶液,溶液中部分微粒与pH的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )| A. | W点所示的溶液中:c(Na+)+c(H+)=4c(CO32-)+c(OH-)+c(Cl-) | |
| B. | pH=4的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1 mol/L | |
| C. | pH=8的溶液中:c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-) | |
| D. | pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)>c(H2CO3) |
分析 A.根据电荷守恒判断,阴离子漏掉了碳酸氢根离子;
B.pH=4时有二氧化碳气体生成,根据物料守恒判断,碳元素守恒;
C.先判断溶液中的溶质,根据图象可知pH=8时,溶液中碳酸氢钠的浓度远远大于碳酸钠的浓度,这说明反应中恰好是生成碳酸氢钠,则根据物料守恒和电荷守恒计算判断;
D.先根据图象判断溶液中的溶质,再确定其浓度关系,根据图象可知pH=11时,溶液碳酸钠的浓度远远大于碳酸氢钠,这说明碳酸钠是过量的.
解答 解:A.根据电荷守恒可知,溶液中离子浓度应该满足:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)+c(HCO3-),故A错误;
B.根据图象可知,pH=4时有CO2生成,根据物料守恒可知c(H2CO3)+c(HCO3-)+c(CO32-)<0.1 mol•L-1,故B错误;
C.根据图象可知pH=8时,溶液中碳酸氢钠的浓度远远大于碳酸钠的浓度,这说明反应中恰好是生成碳酸氢钠,则根据物料守恒可知:c(H2CO3)+c(HCO3-)+c(CO32-)=c(Cl-)=$\frac{1}{2}$c(Na+),再结合电荷守恒c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)+c(HCO3-)可得:c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-),故C正确;
D.根据图象可知pH=11时,溶液碳酸钠的浓度远远大于碳酸氢钠,这说明碳酸钠是过量的,则c(Na+)>c(CO32-)>c(Cl-)>c(HCO3-)>c(H2CO3),故D错误;
故选C.
点评 本题考查碳酸钠和盐酸反应中离子浓度大小比较,该题是高考中的常见题型,属于综合性试题的考查,对学生的思维能力提出了较高的要求,侧重对学生能力的培养,意在培养学生的逻辑推理能力和创新思维能力.该题的关键是在明确反应原理的基础上利用好几种守恒关系,即电荷守恒、物料守恒以及质子守恒,然后结合图象和题意灵活运用即可,题目难度中等.


科目:高中化学 来源: 题型:推断题
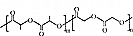 )制成的外科手术缝线在人体内可降解,省去了缝合皮肤后拆线的麻烦,合成PLGA的一种路线如图:
)制成的外科手术缝线在人体内可降解,省去了缝合皮肤后拆线的麻烦,合成PLGA的一种路线如图: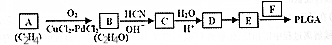
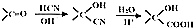
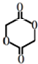 ;
;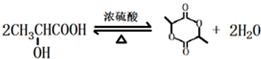 ;
;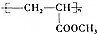 的合成线路:
的合成线路: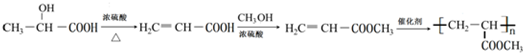 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某研究性学习小组拟探究在含Mg2+、Al3+的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程.
某研究性学习小组拟探究在含Mg2+、Al3+的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程.| 较大量存在的含金属元素的离子 | 检验方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3+H3O+═NH${\;}_{4}^{+}$+H2O:NH3结合H+的能力比H2O强 | |
| B. | Al2O3+2NaOH═2NaAlO2+H2O:Al2O3是两性氧化物 | |
| C. | HClO+SO2+H2O═HCl+H2SO4:酸性 HClO>H2SO4 | |
| D. | 已知C(s,石墨)=C(s,金刚石)△H=+1.9 kJ/mol:金刚石比石墨稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁胶体中加入HI溶液:Fe(OH)3+3H+═Fe3++2H2O | |
| B. | 用氨水溶解氢氧化铜沉淀:Cu2++4NH3•H2O═[Cu(NH3)4]2++4H2O | |
| C. | 用稀硝酸除去试管内壁银:3Ag+4H++NO3-═3Ag++NO↑+2H2O | |
| D. | 向NaOH溶液中通入过量的CO2:CO2+2OH-═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
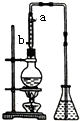 市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\underset{\stackrel{{H}^{+}}{→}}{\;}$n(C2H4O).
市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\underset{\stackrel{{H}^{+}}{→}}{\;}$n(C2H4O).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
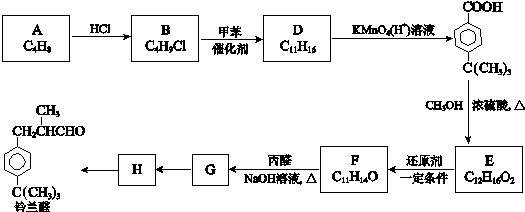
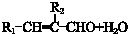
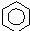 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$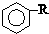 +HCl
+HCl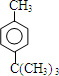 .
.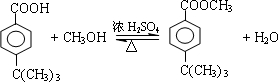 .
. .
. .
. .
.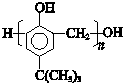 ,合成路线是(不需写化学方程式)
,合成路线是(不需写化学方程式)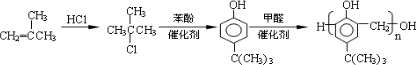 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔬菜表面洒少许福尔马林,可保鲜和消毒 | |
| B. | 推广使用可降解塑料及布质购物袋,以减少“白色污染” | |
| C. | 绿色食品就是不使用化肥农药,不含任何化学物质的食品 | |
| D. | 推广使用煤液化技术可减少二氧化碳温室气体的排放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com