
����Ŀ����ѧ�ϳ���ȼ�շ�ȷ���л������ɣ�����ͼ��ʾװ������ȼ�շ�ȷ���������ĺ������������ʽ�ij���װ�ã����ַ������ڵ�¯����ʱ�ô�������������Ʒ�����ݲ��������ȷ���л������ɣ� 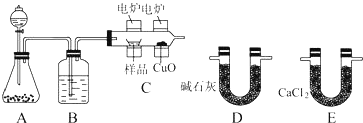
����������⣺
��1��A�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2��Bװ�õ������� �� ȼ�չ�C��CuO��������
��3������������������������ȼ�չ�C��װ��D��E������˳���ǣ�C���� ��
��4����Ӧ������Aװ����ƿ�ڵ�ʣ�������з�������壬��Ҫ���е�ʵ������� ��
��5��ȷ��ȡ 1.8g ���ĺ���������X����Ʒ�������ȼ�պ�D���������� 2.64g��E���������� 1.08g������л����ʵ��ʽ�� �� ʵ����X�������ܶ���ͬ��ͬѹ�������ܶȵ�45������X�ķ���ʽΪ �� 1mol X�ֱ�������Na��NaHCO3��Ӧ�ų�����������ͬ�����µ������Ϊ1��1��X���ܵĽṹ��ʽΪ ��
���𰸡�
��1��2H2O2 ![]() 2H2O+O2������2Na2O2+2H2O=4NaOH+O2����
2H2O+O2������2Na2O2+2H2O=4NaOH+O2����
��2�����������е�ˮ�������������������ʹ�л��ﲻ��ȫȼ�յIJ���ȫ��ת��ΪCO2��H2O
��3��E��D
��4�����ˡ������ᾧ������Na2O2��H2O��Ӧ��O2���Ӧ����
��5��CH2O��C3H6O3��CH3CH��OH����COOH��HO��CH2CH2��COOH
���������⣺��1��AΪ�����Һ�巴Ӧ�Ʊ�������װ�ã����ù�������Ͷ������̣�Ҳ���ù������ƺ�ˮ��Ӧ�Ʊ�������ʽΪ2H2O2 ![]() 2H2O+O2������2Na2O2+2H2O=4NaOH+O2���������Դ��ǣ�2H2O2
2H2O+O2������2Na2O2+2H2O=4NaOH+O2���������Դ��ǣ�2H2O2 ![]() 2H2O+O2������2Na2O2+2H2O=4NaOH+O2��������2�������Ϸ�����֪B�������������е�ˮ�������������������CuO��������ʹ�л�������������CO2��H2O�����Դ��ǣ����������е�ˮ������������������� ʹ�л��ﲻ��ȫȼ�յIJ���ȫ��ת��ΪCO2��H2O����3���л���ȼ������ˮ�Ͷ�����̼��Ӧ�����Ȼ�������ˮ��Ȼ�����ü�ʯ�����ն�����̼�����Դ��ǣ�E��D����4�����ö������̺��������Ʊ������������Ϊ�������̣�������ˮ�����ù��˵ķ������룬���ù������ƺ�ˮ�Ʊ������������������ƣ����������ᾧ�ķ����Ʊ������Դ��ǣ����ˡ������ᾧ������Na2O2��H2O��Ӧ��O2���Ӧ��������5��D����������2.64g��˵��������2.64g��n��CO2��=
2H2O+O2������2Na2O2+2H2O=4NaOH+O2��������2�������Ϸ�����֪B�������������е�ˮ�������������������CuO��������ʹ�л�������������CO2��H2O�����Դ��ǣ����������е�ˮ������������������� ʹ�л��ﲻ��ȫȼ�յIJ���ȫ��ת��ΪCO2��H2O����3���л���ȼ������ˮ�Ͷ�����̼��Ӧ�����Ȼ�������ˮ��Ȼ�����ü�ʯ�����ն�����̼�����Դ��ǣ�E��D����4�����ö������̺��������Ʊ������������Ϊ�������̣�������ˮ�����ù��˵ķ������룬���ù������ƺ�ˮ�Ʊ������������������ƣ����������ᾧ�ķ����Ʊ������Դ��ǣ����ˡ������ᾧ������Na2O2��H2O��Ӧ��O2���Ӧ��������5��D����������2.64g��˵��������2.64g��n��CO2��= ![]() =0.06mol��m��C��=0.06mol��12g/mol=0.72g�� E����������1.08g��˵��������1.08g��ˮ��n��H2O��=
=0.06mol��m��C��=0.06mol��12g/mol=0.72g�� E����������1.08g��˵��������1.08g��ˮ��n��H2O��= ![]() =0.06mol��m��H��=0.06mol��2��1g/mol=0.12g��
=0.06mol��m��H��=0.06mol��2��1g/mol=0.12g��
�Ӷ����Ƴ�����Ԫ�ص�����Ϊ��1.8g��0.72g��0.12g=0.96g��n��O��= ![]() =0.06mol��
=0.06mol��
N��C����N��H����N��O��=0.06mol��0.12mol��0.06mol=1��2��1���ʸ��л����ʵ��ʽΪCH2O��ʽ��Ϊ30�����л������Է�������Ϊ��45��2=90�������ʽΪ CnH2nOn �� 30n=90�����n=3���ʷ���ʽΪ��C3H6O3���� 1molX�ֱ�������Na��NaHCO3��Ӧ�ų�����������ͬ�����µ������Ϊ1��1����һ���ǻ���һ���Ȼ����ʸ��л���ṹ��ʽΪ��CH3CH��OH����COOH��HO��CH2CH2��COOH�����Դ��ǣ�CH2O��C3H6O3��CH3CH��OH����COOH��HO��CH2CH2��COOH��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A�Ľṹ��ͼ��ʾ������˵����ȷ���ǣ� �� 
A.һ�������£�1 mol A����3 mol NaOH��Ӧ
B.һ�������£�1 mol A�ܺ�5 mol���������ӳɷ�Ӧ
C.һ�������º�Ũ��ˮ��Ӧʱ��1 mol A������3 mol Br2
D.A����̼��������Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���÷���ʽC7H8O����ʾ��ij�������б��������Һ�FeCl3��Һ������Ӧ����Һ����ɫ�����ֻ������ͬ���칹���У� ��
A.2��
B.3��
C.4��
D.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ����ȡ9gֱ����������ˮ���ⶨ����ˮ��İٷ��ʣ���������£� 
��1������ʵ����������ӵ��Լ�ΪA �� B �� C ��
��2�������ⶨ�����У�ֻ��A��Һ������B��Һ�Ƿ���У������� ��
��3��������2.16g��������ʱ�����۵�ˮ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������
��1��ijʵ��С��ͬѧ��������ʵ�飬�Լ��黯ѧ��Ӧ�е������仯��ʵ���з��֣���Ӧ����е��¶����ߣ����е��¶Ƚ��ͣ��ɴ��ж�����������ķ�Ӧ���ȷ�Ӧ��Ba��OH��28H2O��NH4Cl�ķ�Ӧ���ȷ�Ӧ����Ӧ��������١��ڡ����������仯����ͼ2��ʾ�� 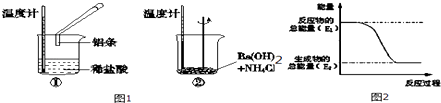
��2��Ϊ����֤Fe3+��Cu2+������ǿ��������װ���ܴﵽʵ��Ŀ����������ţ��� 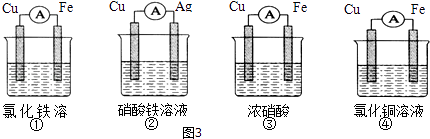
��3����CH4��Ƴ�ȼ�ϵ�أ��������ʸ��ߣ�װ����ͼ4��ʾ��a��bΪ���̼���������缫���ͨ���飨��A��B������缫��ӦʽΪ �� 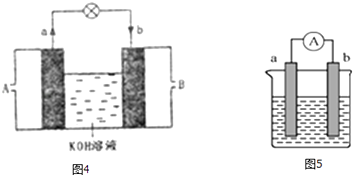
��4����ͼ5��ij��ѧ��ȤС��̽����ͬ�����»�ѧ��ת��Ϊ���ܵ�װ�ã���ش��������⣺ �ٵ��缫aΪAl���缫bΪCu���������ҺΪϡ����ʱ��д����ԭ��������ĵ缫��ӦʽΪ ��
�ڵ��缫aΪAl���缫bΪMg���������ҺΪ����������Һʱ����ԭ��ص�����Ϊ����ԭ��صĸ�����ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һδ֪����ɫ��Һ��ֻ���ܺ������������е������֣�������ˮ���������H+��OH������H+��NH4+��K+��Mg2+��Cu2+��Al3+��NO3����CO32����SO42�� �� ��ȡ����100mL��Һ��������ʵ�飺 �ٵ�һ�ݼ�����AgNO3��Һ���а�ɫ����������
�ڵڶ��ݼ�����BaCl2��Һ���а�ɫ������������ϴ�ӡ������������Ϊ6.99g��
�۵�������εμ�NaOH��Һ����ó�����NaOH��Һ�������ϵ��ͼ��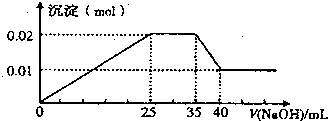
��������ʵ�飬�����Ʋⲻ��ȷ���ǣ� ��
A.ԭ��Һһ��������H+��Cu2+��CO32��
B.����ȷ��ԭ��Һ�Ƿ���K+��NO3��
C.ʵ�����ӵ�NaOH��Ũ��Ϊ2molL��1
D.ԭ��Һȷ����Mg2+��Al3+��NH4+ �� ��n��Mg2+����n��Al3+����n��NH4+��=1��1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��Ϊ��ѧ��ѧ�����Ĵ����A�ǵ��ʣ�����֮������ͼ�ķ�Ӧ��ϵ�� 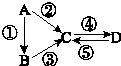
��1����A�ǵ���ɫ���壬C��D�������C������������Ҫ���ʣ���CҲ����㷺����;��д�����е�2����;�� ��
��2����B����̬�⻯�C��D���������һ���ɹ⻯ѧ������Ⱦ��B��C��һ�������·�Ӧ���ɵ�A�Ǵ�������Ҫ�ɷ֣�д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3����A��̫���ܵ���õĹ�����ϣ�B������������ά��C��DΪ���Σ���D�dz����г��õ����ʣ���C�ĵ��뷽��ʽд���ܷ�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʷֱ�μӵ��������ɫ�����ϣ�����ʹ����ɫ����
A. ���Ƶ���ˮ B. Һ��
C. ���������Һ D. ����ʹ������ƵĻ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��XeO3��һ�ֲ��ȶ������ʣ�����ǿ�����ԣ�
��1����ƽ��Ӧ�����ӷ���ʽ��
XeO3+Mn2++H2O��MnO4��+Xe��+H+
��2����Ӧ����Ϊ���������ݲ������� ��
��3����������Ԫ���� ��
��4����������XeO3Ͷ��30mL 0.1molL��1 Mn2+��ˮ��Һ�У��պ���ȫ��Ӧ��
�ٴ�ʱת�Ƶ�������Ϊ ��
�ڽ���Ӧ�����Һϡ����90mL��������Һ��pH= ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com