
【题目】实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热.图是实验室利用此反应制备氯气并进行一系列相关实验的装置(夹持设备已略). 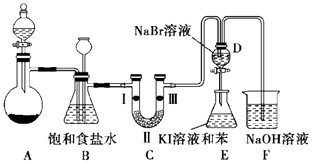
(1)上述反应中是氧化剂,是还原剂,若反应中氧化产物比还原产物多 1mol,则转移的电子数目为 .
(2)装置B的作用是 , 实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象: .
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入(选“a”“b”或“c”)
a | b | c | |
Ⅰ | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E 的目的是为了比较Cl2、Br2、I2的氧化性强弱. 已知Br2 的水溶液因浓度不同而呈现橙色或红棕色,I2难溶于水而易溶苯,且 I2 的苯溶液为紫红色.当向D中缓缓通入足量Cl2时,可以看到无色溶液逐渐变为红棕色,说明 Cl2的氧化性大于 Br2 , 请写出D中对应的离子方程式并用双线桥法表示出电子转移情况: . 打开活塞,将 D中的少量溶液加入E中,振荡E,观察到E中溶液分为两层,上层(苯层)为紫红色.该现象( 填“能”或“不能”)说明Br2的氧化性大于I2 .
(5)装置F的作用是除去污染性的物质(Cl2、Br2 等),已知Cl2与NaOH反应时产物中可能有NaCl、NaClO、NaClO3 , 且 ![]() 值与温度高低有关. 若烧杯中装有500mL0.2mol/L 的NaOH溶液,则最多可吸收标况下的Cl2的体积为L(忽略Cl2溶于水).
值与温度高低有关. 若烧杯中装有500mL0.2mol/L 的NaOH溶液,则最多可吸收标况下的Cl2的体积为L(忽略Cl2溶于水).
【答案】
(1)KClO3;HCl;2.5NA
(2)除杂和安全瓶;锥形瓶中的液面下降,长颈漏斗中的液面上升
(3)c
(4) ;不能
;不能
(5)1.12
【解析】解:(1)因HCl中Cl元素的化合价升高,则HCl为该反应中的还原剂,KClO3中的Cl的化合价降低被还原,KClO3是氧化剂,氧化产物比还原产物物质的量之比为5:1,若反应中氧化产物比还原产物多 1mol,则氧化产物为1.25mol,还原产物为0.25mol,所以转移的电子数目为2.5NA , 所以答案是:KClO3;HCl;2.5NA;(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,发生堵塞时B中的,压强增大,锥形瓶中液面下降,长颈漏斗中液面上升;
所以答案是:除杂和安全瓶;锥形瓶中的液面下降,长颈漏斗中的液面上升;(3)装置C的实验目的是验证氯气是否具有漂白性,验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性,选项中ab的Ⅱ中都是干燥剂,再通入湿润的有色布条不能验证氯气的漂白性,所以C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,
所以答案是:c;(4)D中氯气与溴化钠反应生成氯化钠和溴单质,对应的离子方程式并用双线桥法表示出电子转移情况:  ;打开活塞,将装置D中含溴单质的少量溶液加入焓碘化钾和苯的装置E中,溴单质和碘化钾反应生成碘单质,碘单质溶于苯呈紫红色,振荡;观察到的现象是:E中溶液分为两层,上层(苯层)为紫红色;氯气具有强氧化性,过量的氯气能够将碘离子氧化成碘单质,所以该现象不能说明溴的非金属性强于碘;
;打开活塞,将装置D中含溴单质的少量溶液加入焓碘化钾和苯的装置E中,溴单质和碘化钾反应生成碘单质,碘单质溶于苯呈紫红色,振荡;观察到的现象是:E中溶液分为两层,上层(苯层)为紫红色;氯气具有强氧化性,过量的氯气能够将碘离子氧化成碘单质,所以该现象不能说明溴的非金属性强于碘;
所以答案是:  ;不能;(5)已知Cl2与NaOH反应时产物中可能有NaCl、NaClO、NaClO3 , 由原子守恒可知,n(Cl2)=
;不能;(5)已知Cl2与NaOH反应时产物中可能有NaCl、NaClO、NaClO3 , 由原子守恒可知,n(Cl2)= ![]() n(NaOH)=0.5L×0.2mol/L×
n(NaOH)=0.5L×0.2mol/L× ![]() =0.05mol,则标况下的Cl2的体积为1.12L;
=0.05mol,则标况下的Cl2的体积为1.12L;
所以答案是:1.12.
【考点精析】本题主要考查了氯气的化学性质和氯气的实验室制法的相关知识点,需要掌握氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应;实验室制法:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】下列离子能大量共存的是( )
A. 无色酚酞试液呈红色的溶液中:Na+ 、K+、SO42-、CO32-
B. 无色透明的溶液中:Cu2+、K+、SO42-、NO3-
C. 含有大量Ba(NO3)2的溶液中:Mg2+、NH4+、SO42-、Cl-
D. 紫色石蕊试液呈红色的溶液中:Ca2+、K+、HCO3-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.把100mL 3molL﹣1的H2SO4跟100mL H2O混合,硫酸的物质的量浓度改变为1.5molL﹣1
B.把200mL 3molL﹣1的BaCl2溶液跟100mL 3molL﹣1的KCl溶液混合后,溶液中的C(Cl﹣)仍然是3molL﹣1
C.把100g20%的NaCl溶液跟100g H2O混合后,NaCl溶液的质量分数是10%
D.把100mL 20%的NaOH溶液跟100mL H2O混合后,NaOH溶液的质量分数是10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5 L 1 mol/L FeCl3溶液与0.2 L 1 mol/L KCl溶液中的Cl-的物质的量浓度之比为( )
A. 5:2 B. 3:1 C. 15:2 D. 5:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1mol·L-1KI溶液:Na+、K+、ClO-、OH-
B.0.1mol·L-1Fe2(SO4)3溶液:Cu2+、NH4+、NO3-、SO42-
C.PH=7的溶液中:Al3+、Cl-、Na+、NO3-
D.25℃时,水电离出的c(H+)=1×l0l3mol/L的溶液中:K+、Ba2+、NO3、S2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下在三个体积为1.0L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g),下列说法正确的是( )
CH3OCH3(g)+H2O(g),下列说法正确的是( )
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A. 该反应的正向为吸热反应
B. 达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C. 容器I中反应达到平衡所需时间比容器Ⅲ中的长
D. 若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制500 mL 0.0500 mol·L-1的Na2CO3溶液,不需要的仪器是
A. 500 mL容量瓶 B. 锥形瓶 C. 烧杯 D. 胶头滴管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅、磷、硫、氯都是第三周期的非金属元素,它们在工农业生产中都有重要的用途。
(1) 基态硅原子的电子排布图为_________________________________________________;硫的基态原子能量最高的电子云在空间有________________个伸展方向,原子轨道呈________________形。
(2)硅、磷、硫的第一电离能由大到小的顺序为________________。
(3)单质磷与Cl2反应,可以生产PC13和PC15。其中各原子均满足8电子稳定结构的化合物中,P原子的杂化轨道类型为________________,其分子的空间构型为________________。
(4)H3PO4为三元中强酸,与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+。基态Fe3+核外电子排布式为__________;PO43-作为___________为Fe3+提供________________。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,下图为其晶胞,硼原子与磷原子最近的距离为a cm。 用Mg/mol表示磷化硼的摩尔质量,NA表示阿伏加德罗常数的值,则磷化硼晶体的密度为_________g/cm3。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com