
【题目】关于基本营养物质的说法不正确的是( )。
A.所有蛋白质均可通过遇浓硝酸变黄色来鉴别
B.我国居民传统膳食结构中能量的主要来源是糖类
C.人体血糖含量指的是血液中含葡萄糖的多少
D.油脂在碱性条件下的水解产物可以用来制取肥皂
科目:高中化学 来源: 题型:
【题目】苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:
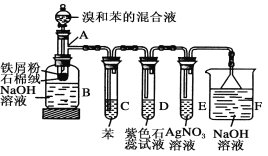
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式):______________________________.
(2)B中NaOH溶液的作用是______________________________.
(3)试管C中苯的作用是_________________________________.
(4)反应开始后,观察D和E两试管,看到的现象为______________,此现象可以验证苯和液溴的反应为____________(填反应类型).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:

下列说法不正确的是( )
A. 溶解烧渣选用足量硫酸,试剂X选用铁粉
B. 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2
C. 从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D. 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关从海带中提取碘的实验原理和装置能达到实验目的的是

A. 用装置甲灼烧碎海带
B. 用装置乙过滤海带灰的浸泡液
C. 用装置丙制备用于氧化浸泡液中I的Cl2
D. 用装置丁吸收氧化浸泡液中I后的Cl2尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知三氯化铁的熔点为306 ℃,沸点为315 ℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验。
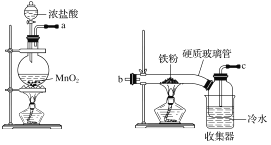
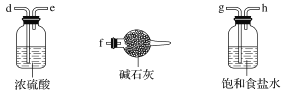
(1)装置的连接顺序为a→_____________________。
(2)饱和食盐水的作用是________。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
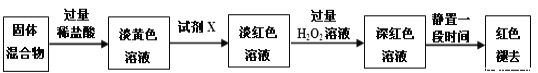
①淡黄色溶液中加入试剂X生成淡红色溶液的离子方程式为_____________。
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是_________________。
(4)已知红色褪去的同时有气体生成,经检验为O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同物质的量浓度的FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
实验①说明______________________________________________;
实验②的目的是___________________________;
得出结论:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯(难溶于水,密度比水大的油状液体)的反应原理,下列关于硝基苯的制备和纯化的装置不正确的是
![]()
A. 浓硫酸与浓硝酸混合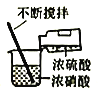
B. 制备硝基苯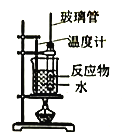
C. 用氢氧化钠溶液分离硝基苯中混有的酸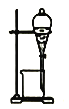
D. 分离硝基苯中混有的苯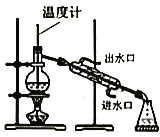
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作或现象描述正确的是( )

A. 实验室用图1装置制备Cl2
B. 加热后图2中溶液颜色恢复红色
C. 用图3装置除去Cl2中含有的少量HCl
D. 实验室用图4装置制取少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是一种重要的化工原料,其绿色化制备是重要的课题。某课外小组设计如下方案用锰酸钾制备高锰酸钾。
I. 锰酸钾制备。将二氧化锰、氯酸钾和氢氧化钾固体放入铁坩埚熔融制锰酸钾。
(1)搅拌时用___________(填“铁棒”或“玻璃棒”)。
(2)若要制得锰酸钾59.1g,至少需要氯酸钾___________g。
II. 高锰酸钾制备。制备高锰酸钾的装置如下图所示(加热与夹持装置省略)。
用I制得的锰酸钾加少量蒸馏水溶解,得墨绿色溶液,倒入三颈瓶中。打开甲装置分液漏斗活塞加入稀硫酸,加热,生成乙酸蒸气,通入乙装置,水浴加热,搅拌,锰酸钾在酸性条件反应生成高锰酸钾和二氧化锰。

(3)用离子方程式表示甲装置中存在的化学平衡___________(任写一个)。
(4)乙装置中发生反应的化学方程式:______________________。
(5)丙装置中氢氧化钠溶液的作用是______________________。
(6)甲装置容易发生倒吸,改进的措施是______________________。
(7)判断乙装置中锰酸钾完全反应的实验方法是;用玻璃棒蘸取溶液滴到滤纸上,若观察到______________________, 表示锰酸钾已完全反应。
III.高锰酸钾产品的纯度分析。
(8)将乙中所得溶液过滤,把滤液倒入蒸发皿中,浓缩,冷却,抽滤,洗涤,干燥得KMnO4产品。请设计实验证明产品中含有少量MnO2:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸 | CH3COOH | H2CO3 |
电离平衡常数(常温) | Ka=1.8×10-5 | Ka1=4.3×10-7; Ka2=5.6×10-11 |
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则c(CH3COOH)/c(CH3COO-)=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com