
| A、6:3:2 |
| B、1:2:3 |
| C、2:3:6 |
| D、2:6:3 |


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
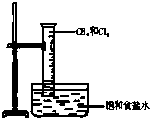 如图所示,将等物质的量的Cl2和CH4 充入一容积为 25mL的量筒,并将量筒倒置在盛有饱和食盐水的水槽中,用日光散射,可观察到的现象是;
如图所示,将等物质的量的Cl2和CH4 充入一容积为 25mL的量筒,并将量筒倒置在盛有饱和食盐水的水槽中,用日光散射,可观察到的现象是;查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同位素:1H2、2H2、3H2 |
| B、化合物:重水、双氧水、矿泉水 |
| C、非电解质:Cl2、BaSO4、C2H5OH |
| D、分子晶体:I2、SO3、固态氩 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液的物质的量浓度为1mol?L-1 |
| B、配制100 mL该溶液需用5.85g NaCl |
| C、0.5 L该溶液含有58.5g NaCl |
| D、量取100 mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 酸 | H2CO3 | CH3COOH | NaHSO4 | HCl |
| 碱 | Mg(OH)Cl | CH3CH2OH | Fe(OH)3 | NaOH |
| 盐 | CuSO4?5H2O | BaSO4 | NaH2PO4 | Na2S |
| 氧化物 | H2O | KClO3 | CuO | H2O2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
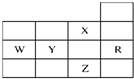
| A、W元素最高价含氧酸酸性强于Y元素最高价含氧酸酸性 |
| B、Z的阴离子电子层结构与R原子的相同 |
| C、p能级未成对电子数最多的是Z元素 |
| D、X元素是电负性最大的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡时,v正(O2)=v逆(O2)必成立 |
| B、关系式5v正(O2)=4v正(NO)总成立 |
| C、用上述四种物质NH3、O2、NO、H2O表示的正反应速率的数值中,v正(H2O)最小 |
| D、若投入4 mol NH3和5 mol O2,通过控制外界条件,必能生成4 mol NO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径的大小顺序:r(Y)>r(Z)>r(W) |
| B、元素Z、W形成的常见化合物中,阴、阳离子个数比相同 |
| C、元素Y 的简单气态氢化物的热稳定性比Z的强 |
| D、X、Y、Z三种元素形成的化合物只能是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、Cl-离子的结构示意图:如图A |
| B、H2O2的结构式:H-O-O-H |
| C、乙烯的结构简式:CH2CH2 |
| D、CCl4分子的球棍模型:如图B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com