
【题目】一名同学把4.48 L(已折算成标准状况下)某有机物蒸气在O2中充分燃烧,然后让产物依次通过装有无水CuSO4的干燥管、盛有浓H2SO4的洗气瓶和盛有含0.8 mol Ca(OH)2的澄清石灰水的烧杯,如图所示:
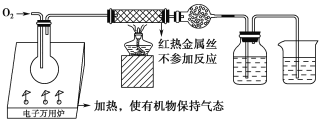
实验结束后发现无水CuSO4变蓝,干燥管和洗气瓶共增重18 g,澄清石灰水变浑浊后又恰好变澄清。请根据实验回答下列问题:
(1)O2要过量的原因是:________________。
(2)若该有机物只含C、H两种元素,且不含任何官能团,也不含脂环,则该有机物的分子式为________,它可能属于________(填序号)。
A.烷烃 B.苯的同系物 C.芳香烃 D.烃的衍生物
该物质可能的结构简式为_____________________。
(3)若该有机物分子中含有一个氧原子,则它可能是哪几类物质?请各举一例,填写在下表中:
物质种类 | 实例(写结构简式) |
_________ | _________ |
_________ | _________ |
_________ | _________ |
【答案】把有机物蒸气完全带入反应装置;保证有机物完全燃烧;从反应装置中把H2O(g)和CO2完全赶出C8H10BC![]() 、
、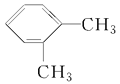 、
、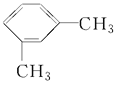 、
、![]() 醇类
醇类![]() 酚类
酚类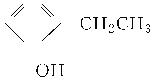 醚类
醚类![]()
【解析】
(1)试验过程中,为了把有机物蒸气完全带入反应装置,保证有机物完全燃烧,从反应装置中把H2O(g)和CO2完全赶出,所以通入的氧气需要足量,故答案为:把有机物蒸气完全带入反应装置;保证有机物完全燃烧;从反应装置中把H2O(g)和CO2完全赶出;
(2)标准状况下4.48L气体的物质的量为:![]() =0.2mol,无水CuSO4变蓝,干燥管和洗气瓶共增重18g,说明18g为水的质量,则水的物质的量为:
=0.2mol,无水CuSO4变蓝,干燥管和洗气瓶共增重18g,说明18g为水的质量,则水的物质的量为:![]() =1mol,该有机物分子中含有H原子数为:
=1mol,该有机物分子中含有H原子数为:![]() =10,含0.8mol Ca(OH)2的澄清石灰水变浑浊又变澄清,说明二氧化碳与氢氧化钙反应生成碳酸氢钙,则生成二氧化碳的物质的量为:0.8mol×2=1.6mol,该有机物分子中含有C原子数为:
=10,含0.8mol Ca(OH)2的澄清石灰水变浑浊又变澄清,说明二氧化碳与氢氧化钙反应生成碳酸氢钙,则生成二氧化碳的物质的量为:0.8mol×2=1.6mol,该有机物分子中含有C原子数为:![]() =8,该有机物只含C、H元素,则该有机物分子式为:C8H10,该有机物不含任何官能团,但含苯环,则该有机物属于苯的同系物、芳香烃,结构简式可能为
=8,该有机物只含C、H元素,则该有机物分子式为:C8H10,该有机物不含任何官能团,但含苯环,则该有机物属于苯的同系物、芳香烃,结构简式可能为![]() 、
、 、
、 、
、![]() ,故答案为:C8H10;BC;
,故答案为:C8H10;BC;![]() 、
、 、
、 、
、![]() ;
;
(3)若该有机物分子中含有一个氧原子,则分子式为C8H10O,可能为醇,如苯乙醇,可能为酚,如乙基苯酚,可能为醚,如苯甲醚等,如表所示: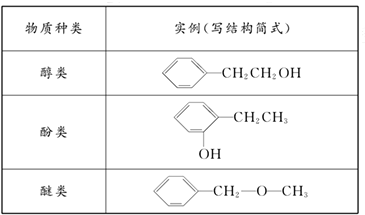 ,故答案为:醇类;
,故答案为:醇类;![]() ;酚类;
;酚类;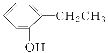 ;醚类;
;醚类;![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列实验操作和实验结论均正确的是
实验操作 | 实验结论 | |
A | 先加少量氯水,再滴加KSCN溶液,出现血红色 | 证明某溶液中存在Fe2+ |
B | 向AgCl悬浊液中加入NaI溶液时出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
C | 向碳酸钙中滴加盐酸,有气泡产生 | 证明氯的非金属性大于碳 |
D | 将MgCl2溶液在氯化氢的气流中蒸发、结晶、过滤 | 制备氯化镁晶体 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素 R、X、Y、Z、E的原子序数依次增加,它们的结构和部分信息如下表所示:
元素代号 | 部分信息 |
R | 基态R原子核外有三个能级,每个能级上电子数相同 |
X | X的双原子单质δ键和π键数目之比为1∶2 |
Y | 短周期主族元素中,原子半径最大 |
Z | Z的最高正化合价与最低负化合价之和等于4 |
E | 基态E3+的外围电子排布式是3d5 |
回答问题:
(1)E元素在周期表中的位置是________,其基态原子中电子占据的最高能层是__________________。
(2)元素 X的氢化物M,分子内含18个电子,M的结构式为_____,每个中心原子的价层电子对数是_________________。
(3)在R、X、Z的含氧酸根离子中,互为等电子体的离子组是_________________。
(4)Z元素的两种氧化物对应的水化物中,酸性较强的________,其原因是_________________。
(5)(ZX)4在常压下,高于130℃时(ZX)4分解为相应的单质,这一变化破坏的作用力是________________;它为热色性固体,具有色温效应,低于-30℃时为淡黄色,高于100℃时为深红色.
在淡黄色→橙黄色→深红色的转化中,破坏的作用力是_________________。
(6)常温条件下,E的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为__________,若E原子的半径为r,则单质E的原子空间利用率为________________。(列出计算式即可)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3·5H2O),又名大苏打、海波,主要用于照相业作定影剂、作鞣革时重铬酸盐的还原剂,易溶于水,遇酸易分解。其工艺制备流程如下:
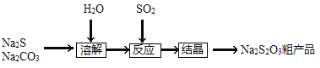
某化学兴趣小组同学模拟该流程设计了如下实验装置:
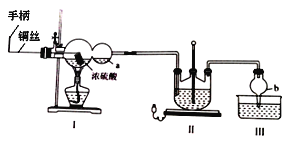
回答下列问题:
(1)双球管a处的液体可用来检验I中的反应是否发生,选用的试剂是______(填字母)
a、品红溶液 b、NaOH溶液 c、稀硫酸
若要停止I中的化学反应,除停止加热外,还要采取的操作是___________________。
(2)加热I,使反应完全,发现浸入液面下的铜丝变黑,甲同学对黑色生成物提出如下假设:①可能是Cu2O;②可能是CuO;③可能是CuS;④CuS和CuO的混合物。乙同学提出假设①一定不成立,该同学的依据是____________________________________;丙同学做了如下实验来验证黑色物质的组成:

基于上述假设分析,原黑色物质的组成为____________________(填化学式)。
(3)II中发生反应的化学方程式为_____________________,实验中通入的SO2不能过量,可能的原因是______________________________________________________。
(4)丁同学提出上述实验装置的设计存在不足,建议在I上_____________;在I、II之间增加_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用核磁共振技术测定有机物分子的三维结构的研究曾获得诺贝尔化学奖。在有机物分子中,不同位置的氢原子的核磁共振氢谱中给出的峰值(信号)也不同。根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
例如:乙醚的结构式为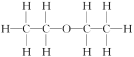 ,其核磁共振氢谱中有2个峰(信号)(参见下图)。
,其核磁共振氢谱中有2个峰(信号)(参见下图)。
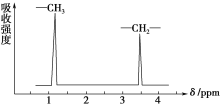
CH3CH2OCH2CH3的核磁共振氢谱
(1)下列分子中,其核磁共振氢谱中只有一种峰(信号)的物质是________。
A.CH3CH3 B.CH3COOH C.CH3COOCH3 D.CH3COCH3
(2)化合物A和B的分子式都是C2H4Br,A的核磁共振氢谱如图所示,则A的结构简式为________,请预测B的核磁共振氢谱上有________个峰(信号)。
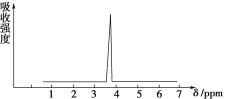
A的核磁共振氢谱示意图
(3)用核磁共振氢谱的方法来研究C2H6O的结构,请简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物TPE具有聚集诱导发光特性,在光电材料领域应用前景广阔,其结构简式如下图所示。下列有关该有机物说法正确的是
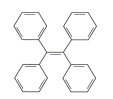
A. 分子式为C26H22 B. 属于苯的同系物
C. 一氯代物有3种 D. 能溶于水和酒精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验所述的变化过程与氧化还原反应无关的是
A | B | C | D | |
实验 | NaOH 溶液滴入FeSO4 溶液中 | 石蕊溶液滴入氯水中 | 向 K2Cr2O7 溶液 中滴加浓硫酸 | CO2 通入 Na2O2 |
现象 | 产生白色沉淀,最 终变为红褐色 | 溶液变红,随后迅速褪色 | 溶液黄色变浅, 橙色加深 | 固体逐渐变白 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com