
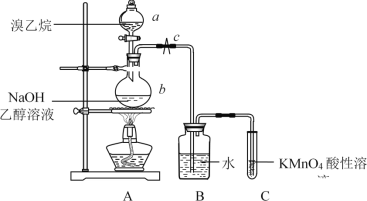
【题目】己知溴乙烷(C2H5Br)是无色液体,沸点38.4℃,密度比水大,难溶于水,可溶于多种有机溶剂。在溴乙烷与NaOH乙醇溶液的消去反应中可以观察到有气体生成。有人设计了如图所示的装置,用KMnO4酸性溶液是否褪色来检验生成的气体是否是乙烯。
请回答下列问题:
(1)仪器a的名称为__________。
(2)实验前应检测装置A的气密性。方法如下:关闭止水夹c,由仪器a向仪器b中加水,若______________________________,则证明装置A不漏气。
(3)仪器b中发生反应的化学方程式为______________________________。
(4)反应开始一段时间后,在装置B底部析出了较多的油状液体,若想减少油状液体的析出,可对装置A作何改进?__________________________________________________
(5)装置A中产生的气体通入装置C之前要先通过装置B,装置B的作用为__________________。
(6)检验乙烯除用KMnO4酸性溶液外还可选用的试剂有__________,此时,是否还有必要将气体先通过装置B?__________(填“是”或“否”)。
【答案】分液漏斗 分液漏斗中液面始终高于圆底烧瓶中的液面(或分液漏斗中液体不能顺利流下) CH3CH2Br+NaOH![]() CH2=CH2↑+NaBr+H2O 将伸出烧瓶外的导管换成长导管 除去挥发出来的乙醇 溴水或溴的四氯化碳溶液 否
CH2=CH2↑+NaBr+H2O 将伸出烧瓶外的导管换成长导管 除去挥发出来的乙醇 溴水或溴的四氯化碳溶液 否
【解析】
(1)根据仪器构造及用途作答;
(2)根据分液漏斗的构造利用液封法检查装置的气密性;
(3)溴乙烷与NaOH醇溶液发生消去反应;
(4)油状液体为溴乙烷蒸气液化的结果;
(5)乙醇易溶于水,据此解答;
(6)根据乙烯的不饱和性,能与Br2发生加成反应作答。
(1)仪器a的名称为分液漏斗,
故答案为:分液漏斗;
(2)关闭止水夹c,由仪器a向仪器b中加水,若分液漏斗中液面始终高于圆底烧瓶中的液面,而不下落,则证明装置A不漏气,
故答案为:分液漏斗中液面始终高于圆底烧瓶中的液面(或分液漏斗中液体不能顺利流下);
(3)卤代烃在碱性醇溶液加热条件下发生了消去反应,生成不饱和烯烃,反应为![]() 故答案为:
故答案为:![]() ;
;
(4)若出现了较多的油状液体,则说明溴乙烷蒸气冷却液化的较多,为减少油状液体的析出,可采取将伸出烧瓶外的导管换成长导管的措施,
故答案为:将伸出烧瓶外的导管换成长导管;
(5)B中的水用于吸收挥发出来的乙醇,目的是防止乙醇和高锰酸钾反应,干扰实验,
故答案为:除去挥发出来的乙醇;
(6)检验乙烯除用KMnO4酸性溶液外还可选用的试剂为溴水或溴的四氯化碳溶液;乙烯也能使溴水或者溴的四氯化碳溶液褪色,因装置B中盛装的是水,目的是防止乙醇和高锰酸钾反应,而溴与乙醇不反应,所以无须用装置B,
故答案为:溴水或溴的四氯化碳溶液;否。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】向一定量的FeO,Fe,Fe3O4的混合物中加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现. 若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是()
A.11.2 gB.5.6 gC.2.8 gD.1.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() (连二亚硫酸钠)是易溶于水,不溶于甲醇的白色固体,在空气中极易被氧化,是一种还原性漂白剂。制取
(连二亚硫酸钠)是易溶于水,不溶于甲醇的白色固体,在空气中极易被氧化,是一种还原性漂白剂。制取![]() 的方法很多,
的方法很多,
(1)在碱性溶液中用![]() 还原
还原![]() 法制备
法制备![]() 的反应原理为:
的反应原理为:![]() (未配平)反应装置如图所示:
(未配平)反应装置如图所示:
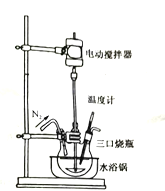
①实验开始及整个过程中均需通入![]() ,其目的是__________________________________。
,其目的是__________________________________。
②制备过程中温度需控制在10~45℃,采用水浴加热的主要优点是______________________。
③为使![]() 尽可能完全被还原,加入三口烧瓶中的反应液,应控制
尽可能完全被还原,加入三口烧瓶中的反应液,应控制![]() ______________。
______________。
(2)用![]() 还原
还原![]() 制备
制备![]() 的装置(夹持加热仪器略)如下:
的装置(夹持加热仪器略)如下:
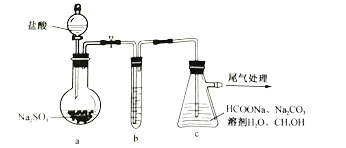
①装置a烧瓶中发生反应的化学方程式为_________________________________。
②装置b用于净化![]() ,适宜的试剂是______________________________。
,适宜的试剂是______________________________。
③装置c在70~83℃生成![]() 并析出,同时逸出
并析出,同时逸出![]() ,该反应的化学方程式为________________________,加入
,该反应的化学方程式为________________________,加入![]() 的目的是________________________;利用反应后的浊液分离提纯
的目的是________________________;利用反应后的浊液分离提纯![]() 需经过的操作为_____________________________________________________。
需经过的操作为_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.某盐是一种重要的化工原料,在印染、制革、木材和农业等领域有重要用途,其溶液可能含有NH4+、Al3+、SO42-、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
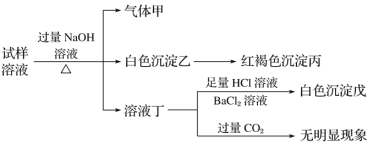
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A.试样中肯定有NH4+、SO42-和Fe2+
B.试样中一定没有Al3+
C.若气体甲在标准状况下体积为0.448 L,沉淀丙和沉淀戊分别为1.07 g和4.66 g,则可判断溶液中还有Cl-
D.该盐工业上可以用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液。下列说法不正确的是
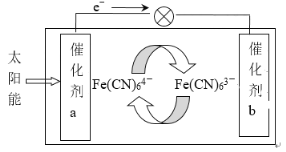
A.K+ 移向催化剂b
B.催化剂a表面发生的化学反应:Fe(CN)64--e-= Fe(CN)63-
C.Fe(CN)63- 在催化剂b表面被氧化
D.电解池溶液中的Fe(CN)64- 和Fe(CN)63- 浓度基本保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,4-环己二醇可通过下列路线合成(某些反应的反应物和反应条件未列出):
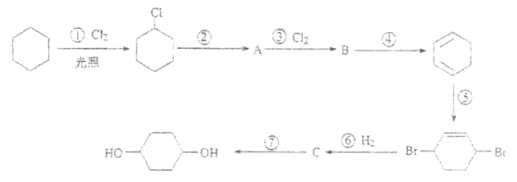
(1)写出反应④、⑦的化学方程式:
④__________________________________;
⑦__________________________________。
(2)上述七个反应中属于加成反应的有____________(填反应序号),A中所含有的官能团名称为____________。
(3)反应⑤中可能产生一定量的副产物,其可能的结构简式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,某有机物和过量Na反应得到V1 L氢气,另一份等量的该有机物和足量的NaHCO3溶液反应得到V2 L二氧化碳,若V1=V2≠0,则该有机物可能是( )
A.HOOCCOOHB.CH3CHOHCOOHC.HOCH2CH2OHD.CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如下实验方法分离KNO3和Ba(NO3)2两种固体混合物并测定其含量:
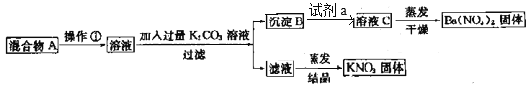
(1)操作①的名称是____________,试剂a是____________(填化学式)。
(2)加入K2CO3溶液所发生反应的离子方程式是__________。
(3)按此实验方案分离得到的KNO3,经分析含有杂质K2CO3,除去K2CO3的操作为___________
(4)过滤后洗涤沉淀B的实验操作为________________。
(5)实验前称量混合物A的质量为m g,称量经洗涤干燥后的沉淀B的质量为w g,则混合物中Ba(NO3)2质量分数为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴元素由于其良好的物理化学性质,被广泛应用于生产生活中。从含钴废料(含CoO、Co2O3、单质Al、Li等)中制取粗CoCl2·6H2O的流程如下所示。
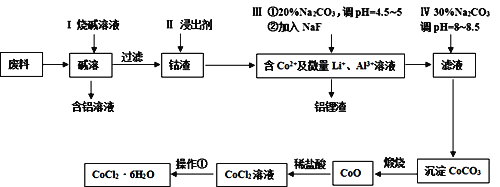
请回答下列问题:
(1)步骤I中主要发生的化学反应方程式为______。
(2)已知Co2O3具有强氧化性,若步骤II中浸出剂为盐酸,造成的后果是_______。
(3)步骤Ⅲ中①的目的是除去Al3+,写出该步反应的离子方程式______。
(4)若在实验室煅烧CoCO3,所需的硅酸盐质仪器除酒精灯和玻璃棒外,还有______、______(填仪器名称)。
(5)操作①是在HCl氛围中进行的,其步骤是______、_____、过滤、洗涤、干燥。洗涤过程中可以用工业酒精代替水,其优点是_____。
(6)某同学用标准硝酸银溶液滴定未知浓度的CoCl2溶液,下列可作为指示剂的是____(填选项,忽略亚钴离子的颜色干扰)
A.KCl B.KSCN C.K2CrO4 D.K2S
已知几种物质在20℃时的颜色及Ksp值如下表
化学式 | AgCl | AgSCN | Ag2S | Ag2CrO4 |
颜色 | 白色 | 浅黄色 | 黑色 | 红色 |
Ksp | 2.0×10-10 | 1.0×10-12 | 2.0×10-48 | 2.0×10-12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com