
【题目】化学用语是学习化学的工具和基础。下列有关化学用语的使用正确的是
A.食醋呈酸性的原因是:CH3COOH+H2O=CH3COO-+H3O+
B.纯碱溶液呈碱性的原因是:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
C.用铁作阳极,电解饱和食盐水的离子方程式:Fe+2H2O![]() Fe(OH)2+H2↑
Fe(OH)2+H2↑
D.表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);![]() H=-571.6KJ·mol—1
H=-571.6KJ·mol—1
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】下图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是

A. 两条曲线间任意点均有c(H+)×c(OH-)=Kw
B. M区域内任意点均有c(H+)<c(OH-)
C. 图中T1<T2
D. XZ线上任意点均有pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 25℃、101 kPa下:① 2 Na(s) + 1/2 O2(g) = Na2O(s) △H1 = - 414 kJ / mol
② 2 Na(s) + O2(g) = Na2O2(s) △H2 = - 511 kJ / mol
下列说法正确的是
A. ①和②产物的阴阳离子个数比不相等
B. ①和②生成等物质的量的产物,转移电子数不同
C. 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D. 25℃、101 kPa下,Na2O2(s) + 2 Na(s) = 2 Na2O(s) △H = -317 kJ / mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸和一水合氨是中学化学中常见的弱电解质。
(1)常温下,某研究性学习小组设计了如下方案证明醋酸为弱电解质,你认为方案可行的是__(填序号)
①配制一定量的0.10mol/LCH3COOH溶液,然后测溶液的pH,若pH大于1,则证明醋酸为弱电解质
②用醋酸溶液和盐酸做导电性实验,若醋酸溶液导电性弱,则证明醋酸为弱电解质
③将pH=2的CH3COOH溶液加水稀释100倍后,若pH>4,则证明醋酸为弱电解质
(2)若25℃时,0.10mol/L的CH3COOH的电离度为1%,则该溶液的pH=___,由醋酸电离出的c(H+)约为水电离出的c(H+)的___倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
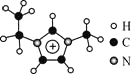
(1)碳原子价层电子的轨道表达式为__________,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_________形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_______;NO3-与NO2-中O-N-O的键角:NO3-____ NO2-(填“<”、“>”“=”)。
(3)EMIM+离子与金属阳离子形成的离子化合物常温下呈液态的原因是____________。
(4)EMIM+离子中,碳原子的杂化轨道类型为___________。分子中的大π键可用符号πnm表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,则EMIM+离子中的大π键应表示为________。
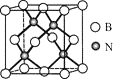
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于_______晶体,其中硼原子的配位数为_______。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率为________(列出化简后的计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度下,纯水中c(H+)=2×10﹣7 molL﹣1,则此时温度____填(“高于”、“低于”或“等于”)25°C,此温度下水的离子积为____。若温度不变,滴入稀盐酸使c(H+)=5×10﹣4 molL﹣1,则此时c(OH﹣)=____。由水电离产生的c(H+)为____
(2)25℃,有pH=12的氢氧化钠溶液100mL,要使它的pH降为11.应加蒸馏水的体积为_____mL;若加pH=10的氢氧化钠溶液,应加_____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的三个容积相同的容器①②③中进行如下反应:3A(g)+B(g) ![]() 2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )
2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )
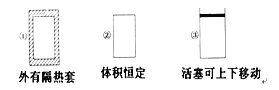
A. ③②①B. ③①②C. ①②③D. ②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为四个常用的电化学装置,关于它们的叙述正确的是
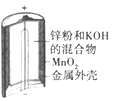
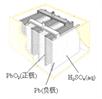
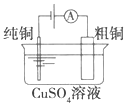
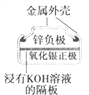
(a)碱性锌锰电池 (b)铅-硫酸蓄电池 (c)电解精炼铜 (d)银锌纽扣电池
A. 图(a)所示电池中,MnO2的作用是催化剂
B. 图(b)所示电池放电过程中,硫酸浓度不断增大
C. 图(c)所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图(d)所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为探究AgCl沉淀的溶解和转化,设计实验方案并记录如下
Ⅰ.将等体积等浓度的AgNO3溶液和NaCl溶液混合得到浊液W,过滤,得到滤液X和白色沉淀Y
Ⅱ.向滤液X中滴加几滴饱和Na2S溶液 出现浑浊
Ⅲ.取少量白色沉淀Y,滴加几滴饱和Na2S溶液 沉淀变为黑色
Ⅳ.取少量白色沉淀Y,滴加几滴浓氨水 沉淀逐渐溶解
(1)步骤Ⅰ的浊液W中存在的沉淀溶解平衡为_______________;
(2)由步骤Ⅱ的浑浊可推测,滤液X中除了含有Na+、NO3﹣,还含有的离子有_______________;
(3)能说明步骤Ⅲ中沉淀变黑的离子方程式为____________.沉淀转化的主要原因是_____________;
(4)已知:Ag++2NH3H2O===Ag(NH3)2++2H2O,用平衡移动原理解释步骤Ⅳ中加入浓氨水沉淀逐渐溶解的原因______________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com