
| 1000ρω |
| M |
| 0.448L |
| 22.4L/mol |
| 1mol |
| 1mol |
| n(Na2CO3) |
| 0.02mol |
| 4.96g-2.12g |
| 4.96g |
| 1000ρω |
| M |
| 1000ρω |
| M |
| 1.02×1000×0.0480 |
| 36.5 |
| 1000ρω |
| M |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | M | N | Q | Z |
| 反应前质量(g) | 19.7 | 8.7 | 31.6 | 0.4 |
| 反应后质量(g) | 待测 | 17.4 | 0 | 3.6 |
| A、物质Q一定是化合物,物质Z可能是单质 |
| B、反应后密闭容器中M的质量为29.7g |
| C、反应过程中,物质N与物质Z变化的质量比为87:36 |
| D、若物质M与物质Q的摩尔质量之比为197:158,则反应中M与Q的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
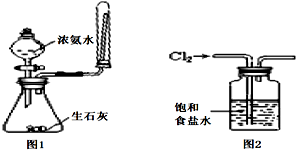 下列操作或实验仪器的使用正确的是(填写字母):
下列操作或实验仪器的使用正确的是(填写字母):查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com