
【题目】下列说法正确的是
A.地下钢铁管道用导线连接锌块可以减缓管道的腐蚀
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.一定条件下,反应N2+3H2![]() 2NH3达到平衡时,3v正(H2)=2v逆(NH3)
2NH3达到平衡时,3v正(H2)=2v逆(NH3)
D.反应2NO(g)+2CO(g)===N2(g)+2CO2(g)常温下可自发进行,该反应为放热反应
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】铁及其化合物在生活中有广泛应用。
(1)Fe3+基态核外电子排布式为______。
(2)实验室用KSCN溶液、苯酚检验Fe3+。
①1mol苯酚分子中含有σ键的数目为______。
②类卤素离子![]() 可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸
可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸![]() 和异硫氰酸
和异硫氰酸![]() ,这两种酸中沸点较高的是______
,这两种酸中沸点较高的是______
(3)氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为______。
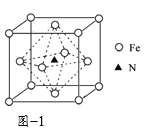
(4)某铁的化合物结构简式如图2所示
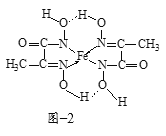
①上述化合物中所含有的非金属元素的电负性由大到小的顺序为______(用元素符号表示)。
②上述化合物中氮原子的杂化方式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH值得盐酸和醋酸溶液分别加水稀释。pH值随溶液体积变化变化如图所示。据图判断正确的是()
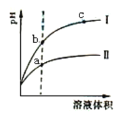
A.Ⅱ为盐酸稀释时pH值变化曲线
B.b点酸的总浓度小于a点酸的总浓度
C.两种酸的物质的量浓度一定相等
D.a点Kw的数值比b点Kw的数值大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W(分子式C3H6O3)能与NaHCO3反应产生CO2,也能与Na反应生成H2,且1 mol W与足量Na反应能生成1 mol H2,分子中核磁共振氢谱为四组峰,峰面积之比为3∶1∶1∶1。
(1)W的结构简式是______________。
(2)W在不同条件下可脱水形成不同物质。若两分子W反应形成环酯,写出反应方程式:_________________。
(3)W的某种同分异构体具有下列性质:
能发生的银镜反应;1 mol该物质能跟金属钠反应产生1 mol H2。
则该同分异构体的结构简式为____________(已知同一个碳原子上不能连接2个羟基)。
(4)W的工业合成路线如图所示:
乙烯![]() A
A![]() B
B![]() C
C![]() D
D![]()
![]() W
W
已知:Ⅰ.A、B、C、D与W分子中含有相同碳原子数;
Ⅱ.RCH2COOH![]()
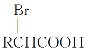
①写出A的名称:__________。
②B与新制Cu(OH)2悬浊液反应的化学方程式是: _______________。
③D与NaOH水溶液反应的化学方程式为:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以绿矾(主要成分FeSO4·7H2O,部分Fe2+已被氧化为Fe3+)为原料,生产铁红(Fe2O3)的工艺流程如下:
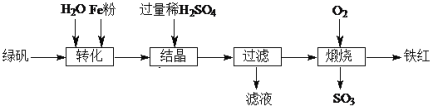
(1)“转化”过程中,加入Fe粉时发生反应的离子方程式为____;为提高该反应速率可采取的措施有:____、____。
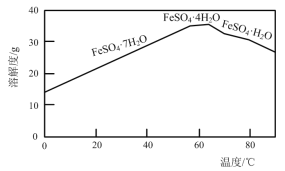
(2)“结晶”时,控制温度在75℃左右进行(相关物质的溶解度见下图),从溶液中析出的晶体是____(填化学式)。
(3)“滤液”的主要成分为FeSO4、____(填化学式)。利用该滤液将工业废水中的Cr2O72—还原为Cr3+,然后投加石灰乳,使Cr3+转化为Cr(OH)3,理论上完全反应消耗的n(FeSO4)∶n(Cr2O72—) =____。
(4)“煅烧”时生成铁红的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质![]() 部分条件未标出
部分条件未标出![]() :
:
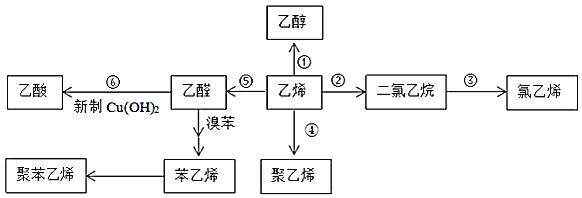
(1)乙醇能与乙酸反应生成有果香味的物质,其名称为______,该反应类型是______;
(2)反应![]() 的化学方程式是______,实验现象是______;
的化学方程式是______,实验现象是______;
(3)反应![]() 用KOH的乙醇溶液处理二氯乙烷制氯乙烯的方程式为:______;
用KOH的乙醇溶液处理二氯乙烷制氯乙烯的方程式为:______;
(4)苯乙烯中所含官能团的名称______;
(5)苯乙烯合成聚苯乙烯的化学方程式是______;
(6)以乙醇和苯乙烯为原料合成有机物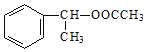 ,写出合成路线图______。
,写出合成路线图______。![]() 合成路线常用的表示方法为:A
合成路线常用的表示方法为:A![]() B目标产物
B目标产物![]() 目标产物
目标产物![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种新型液硫二次电池,其工作原理如图所示。下列说法错误的是

A. 放电时,电池左侧为负极,发生氧化反应
B. 充电时,电解质溶液中K+经交换膜向右侧移动
C. 放电时,电池右侧的电极反应为I3-+2e-=3I-
D. 充电时,电池的总反应为S22-+3I-![]() 2S2-+I3-
2S2-+I3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中,除稀有气体外几乎所有元素都能与氢形成氢化物。
(1)氨气属于共价型氢化物,工业常用氨气和醋酸二氨合铜[Cu(NH3)2]Ac的混合液来吸收CO(醋酸根离子简写为Ac-)。反应方程式为:[Cu(NH3)2]Ac+CO+NH3=[Cu(NH3)3CO]Ac
①氨水溶液中各元素原子的第一电离能从大到小排列顺序为___________。
②醋酸分子(CH3COOH)中的两个碳原子的杂化方式分别是_________________。
③生成物[Cu(NH3)3CO]Ac中所含化学键类型有_________(填序号)。
A.离子键b.金属键c.共价键d.配位键
(2)某离子化合物XY2,晶胞结构如图所示,其中6个Y原子用数字1~6标注。
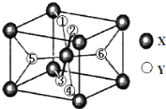
已知1、2、3、4号Y原子在晶胞上、下面上,则5、6号Y原子均在晶胞_________(填“侧面”或“内部”)。
②根据以上信息可以推知,XY2晶体的熔沸点______(填“>”、“=”或“<”)固态氨的熔沸点。
③若该晶胞的边长为anm,密度为ρg/cm3,XY2的摩尔质量为Mg/mol,则阿伏加德罗常数为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来在中国汽车的销量大幅增长的同时也带来了严重的空气污染。汽车尾气处理装置中,气体在催化剂表面吸附与解吸的过程如图所示,下列说法正确的是![]()
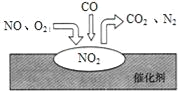
A.汽车尾气的主要污染成分包括CO、NO和![]()
B.催化转化总反应为![]()
C.NO和![]() 必须在催化剂表面才能反应
必须在催化剂表面才能反应
D.反应中NO为还原剂,![]() 为还原产物
为还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com