
����Ŀ�������仯���������ǵ����������
(1)����β����NO���ɹ��̵������仯ʾ��ͼ���£�

�������£�1mol N2��1molO2��ȫ��Ӧ����NO����_______________(���������������ų���)________kJ������
(2)һ���¶��£������Ϊ0.5 L�ĺ����ܱ������У�������̬������X��Y֮�䷴Ӧ�����и����ʵ����ʵ�����ʱ��Ĺ�ϵ��ͼ��ʾ��

�ٸ÷�Ӧ�Ļ�ѧ��Ӧ����ʽ��______________________��
����0��3 min�ڣ���Y��ʾ�ķ�Ӧ����Ϊ____________��
������������˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����________(����ĸ)��
a��������ѹǿ���ٷ����仯
b��X������������ٷ����仯
c��������ԭ���������ٷ����仯
d����ͬʱ��������nmolY��ͬʱ����2nmol X
�ܷ�Ӧ�ﵽƽ����������¶ȣ�����(��)______����(��)________��(��������������С������������)��
(3)��Ӧ A(g)+3B(g)�T2C(g)+3D(g)�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��
���� (A)=0.015mol (Ls)��1 ���� (B)=0.09mol (Ls)��1
���� (C)=2.4mol (Lmin )��1 ���� (D)=0.045mol (Ls)��1
�÷�Ӧ�����ֲ�ͬ����������ɴ�С��˳��Ϊ(��������)________��
���𰸡����� 183 2XY 0.2mol/(L��min) ab ��С ��С ��>��>��=��
��������
(1)���ϼ����յ����������ڳɼ��ų���������Ϊ���ȷ�Ӧ����֮Ϊ���ȷ�Ӧ��
(2) �ٷ�Ӧ������ʵ������٣�����������ʵ��������࣬�������ʵ����ı仯�жϼ�����֮��Ĺ�ϵ��
�ڸ���![]() ����������Y��ʾ��ƽ����Ӧ���ʣ�
����������Y��ʾ��ƽ����Ӧ���ʣ�
�۸���ƽ���־�ж��Ƿ�ﵽƽ��״̬��
�ܽ����¶ȷ�Ӧ����һ����С��
(3)���ݷ�Ӧ����֮�ȵ��ڻ�ѧ������֮���жϡ�
(1)����ͼʾ���ϼ����յ���������945 kJ +498 kJ =1443kJ���ɼ��ų���������Ϊ2mol��630 kJ/mol=1260 kJ���ų�������С�����յ�����������1mol N2��1molO2��ȫ��Ӧ����NO��������1443kJ-1260kJ=183kJ��������
(2) ����ͼ���֪�� Y�����ʵ��������࣬X�����ʵ������٣���XΪ��Ӧ�YΪ���������ȵ�ʱ����X��Y�����ʵ����仯֮��Ϊ0.6:0.3=2:1�����Է�Ӧ����ʽӦΪ��2XY��
�ڸ���![]() 0.2mol/(L��min)��
0.2mol/(L��min)��
��a��2XY��Ӧǰ���������ʵ����DZ������ں�����������ѹǿ�DZ�������ѹǿ���ٷ����仯һ��ƽ�⣬��ѡa��
b��X������������ٷ����仯��˵��X��Ũ�Ȳ��ٱ仯��һ���ﵽƽ��״̬����ѡb��
c�����������غ㣬ԭ�������Ǻ�����������ԭ���������ٷ����仯����һ��ƽ�⣬�ʲ�ѡc��
d����ͬʱ��������nmolY��ͬʱ����2nmol X�������淴Ӧ���ʣ������Ƴ����淴Ӧ������ȣ���һ��ƽ�⣬��ѡd��
�ܽ����¶ȷ�Ӧ���ʼ�С�����Է�Ӧ�ﵽƽ����������¶ȣ����(��)��С����(��)��С��
(3) �٦� (A) ��1=0.015mol (Ls)��1��1=0.015mol (Ls)��1��
�ڦ� (B) ��3=0.09mol (Ls)��1��3=0.03mol (Ls)��1
�ۦ� (C) ��2=2.4mol (Lmin )��1��2=1.2mol (Lmin )��1=0.02 mol (Ls)��1
�ܦ� (D) ��3=0.045mol (Ls)��1��3=0.015mol (Ls)��1�������ɴ�С��˳��Ϊ��>��>��=�ܡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС��Ϊȷ��ij��״�л���A�Ľṹ�����ʣ��������ô�ͳʵ����ֶ����ִ��������ϵķ�������̽�����������̽�����̣�
����ʵ��ʽ��ȷ��
��1��ȡ��ƷA����ȼ�շ��ⶨ������ȼ�պ�ֻ����CO2��H2O��ij��ȼ�պ�����õ���0.125 mol CO2��2.7g H2O���ݴ˵ó��Ľ�����_______��
��2����һʵ���У�ȡ3.4 g��״A��3.36 L(��״���£���ͬ)��������ȫȼ�գ����߾�ǡ����ȫ��Ӧ������2.8 L CO2��Һ̬ˮ��ͨ������ȷ��A��ʵ��ʽ��__________
�����ṹʽȷ��(���ⶨA����Է�������������140)
��3��ȡ������Ʒ�ۻ����������������ų���˵��A�����к���_______����
��4�����к˴Ź�����ֻ�����������壬�������Ϊ8:4������������ף��������Ҵ�һ��������ͬһ�����������ա�ͼ�����£�

��A�Ľṹ��ʽΪ_______��
��������̽��
��5��A��Ũ�������ϼ��ȷ�����Ӧ�Ļ�ѧ����ʽΪ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ȵ�����ԭ�ӣ�����֮��Ĺ�ϵ�ǣ� ��
A.������һ�����B.����Ϊͬλ��
C.һ����ͬ��ԭ��D.�ֱ���ɵĵ��ʣ���������һ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��A~G��Ϊ��ѧ��ѧ�г��������ʣ�����֮��������ת����ϵ������A����Ȼ������Ҫ�ɷ֣�B��һ����ʹ������ľ����ȼ�����壬C��һ����ʹ����ʯ��ʯ����ǵ����壬E��һ�ֵ���ɫ��ĩ״���塣����Ӧ������ijЩ��������ȥ��
��ش����⣺

��1��A�ĵ���ʽΪ_______________________________��
��2��E�Ļ�ѧʽΪ_______________________________��
��3��д��Cת��ΪF�Ļ�ѧ����ʽ_________________________________________��
��4��д��G��Һ��ͨ�����C�����ӷ���ʽ_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A��B�����ݻ�Ϊ5L���ܱ����������������·�Ӧ��3A(g) +B(g) ![]() 2C(g)��2D��g������Ӧ���е�10sĩ�����A�����ʵ���Ϊ1.8mol��B�����ʵ���Ϊ0.6mol��C�����ʵ���Ϊ0.8mol����
2C(g)��2D��g������Ӧ���е�10sĩ�����A�����ʵ���Ϊ1.8mol��B�����ʵ���Ϊ0.6mol��C�����ʵ���Ϊ0.8mol����
��1������C����ʾ�ĸ÷�Ӧ������__________________��
��2����ӦǰA�����ʵ���Ũ��____________________��
��3����Ӧ10s����B���ʵ�ת����_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤±�ص��������Ե����ǿ����ijС������ͼ��ʾװ�ý���ʵ��(�������Ѽ���)��4��5��6��պ����Ӧ��Һ�İ�ֽ��U���Ϸ����������1.���۵⻯����Һ��2.NaBr��Һ������������ͷ���е��ɼеIJ����ܣ�

ʵ����̣�
��. �رյ��ɼ�b��������a���μ�Ũ���ᡣ
��. ��4��5��6��ֽ������ɫ�仯���ɼ�b��
��. ����������պ��NaBr��Һ�����ű�ɺ���ɫ��رյ��ɼ�b��
��.����
(1)����a��_______________��
(2)U���в�������ɫ���壬�����ʽ��_______________��
(3)��֤������������ǿ�ڵ��ʵ��������_______________��
(4)Ϊ��֤���������ǿ�ڵ⣬���̢��IJ�����������_______________��
(5)���̢�ʵ���Ŀ����_______________��
(6)�ȡ��塢�ⵥ�ʵ�������������ԭ��(��ԭ�ӽṹ�ĽǶȽ���)_________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ú�����Դ��õIJ���������ͼ��ʾ������˵����ȷ����
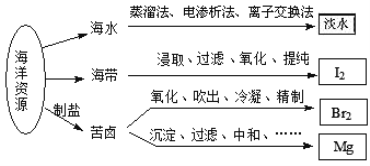
A. �Ӻ�ˮ�л�ȡ��ˮ����ʷ��õķ��������ӽ�����
B. ʵ�����дӺ����л��I2����Ҫ�õ�����Ҫ������������©�����ձ�����Һ©����
C. ��Na2CO3��Һ���մӿ�±�д����ĵ�����ʱ�������Ļ�ѧ��Ӧ������3Br2+3Na2CO3�T5NaBr+ NaBrO3+3CO2��3Br2+6Na2CO3+3H2O�T5NaBr+NaBrO3+6NaHCO3
D. �ñ��ǡ�����ȴӿ�±����ȡþʱ��������Ӧ�������л��ϡ��ֽ⡢�û����ֽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ͼ��ʾת����ϵ(X����±��)��˵���������

A. ��H3<0
B. ��H1=��H2+��H3
C. ��Cl��Br��I��˳��H2��������
D. ��H1ԽС��HXԽ�ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����(����)
A. ����£�11.2L���������Ϊ0.5 NAB. 0.5molC3H8������C��H���ۼ�����Ϊ2NA
C. 11.2Lһ�ȼ�������������Ϊ0.5NAD. 30g��������к��еĹ��õ��Ӷ�Ϊ7NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com