
【题目】下面是以秸秆(含多糖类物质)为原料合成聚酯类高分子化合物的路线:

已知:
请回答下列问题:
食物中的纤维素虽然不能为人体直接提供能量,但能促进肠道蠕动,黏附并带出有害物质,俗称人体内的“清道夫”。从纤维素的化学成分看,它是一种____(填序号)。
a.单糖 b.多糖 c.氨基酸 d.脂肪
A中官能团的名称为____、____。
A生成B的反应条件为____。
B、C的结构简式分别为____、____。
写出E→F的化学反应方程式______。
【答案】b 羧基 碳碳双键 浓硫酸、加热 H3COOCCH=CHCH=CHCOOCH3 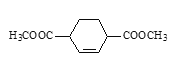
【解析】
食物中的纤维素属于多糖,由合成路线图看出A中官能团为:羧基和碳碳双键,A和乙醇发生酯化反应,条件是浓硫酸、加热,生成的B是酯,由路线图和已知可看出B、C的结构简式,E和1,4-丁二醇是在催化剂作用下发生的缩聚反应。
食物中的纤维素属于多糖,故答案为多糖;
本题答案为:b.
由合成路线图看出A中官能团为:羧基和碳碳双键;
本题答案为:羧基 、碳碳双键。
A和乙醇在浓硫酸、加热的条件下,发生酯化反应;
本题答案为:浓硫酸、加热。
由路线图和已知可看出B为A和乙醇酯化反应生成的酯,B的结构简式为H3COOCCH=CHCH=CHCOOCH3;由题中信息可知,B和乙烯发生加成反应得到C,C的结构简式为![]() ;
;
本题答案为:H3COOCCH=CHCH=CHCOOCH3、![]() 。
。
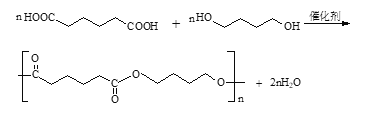
E是二元羧酸,所以E和1,4-丁二醇是在催化剂作用下发生的缩聚反应的化学方程式为: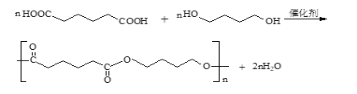 ;
;
本题答案为: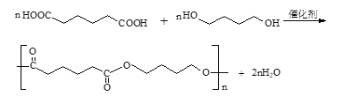 。
。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】恒温恒容下,将2mol气体A和2mol气体B通入体积为2L的密闭容器中,发生如下反应:2A(g)+B(g)![]() xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2molB,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2molB,并测得C的浓度为1.2mol/L。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为__。
(2)x=__。
(3)下列各项可作为该反应达到平衡状态的标志是__(填字母)。
A.气体密度不再变化
B.压强不再变化
C.A的消耗速率与B的消耗速率之比为2:1
D.气体平均相对分子质量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氢氧燃料电池放电时化学能全部转化为电能
B. 反应4Fe(s)+3O2(g)![]() 2Fe2O3(s)常温下可自发进行,该反应为吸热反应
2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了缓解温室效应,科学家提出了多种回收和利用CO2的方案。
方案I:利用FeO吸收CO2获得H2
i.6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △Hl=-76.0kJ/mol
ⅱ.C(s)+2H2O(g)==CO2(g)+2H2(g) △H2=+113.4kJ/mol (1)3FeO(s)+H2O(g)=Fe3O4(s)+H2(g) △H3=__________。
(2)在反应i中,每放出38.0kJ热量,有______gFeO被氧化。
方案II:利用CO2制备CH4
300℃时,向2L恒容密闭容器中充入2mol CO2和8molH2,发生反应CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示。
CH4(g)+2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示。

(3) ①从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)=________。
②300℃时,反应的平衡常数K=________。
③保持温度不变,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度_______(填字母)。
A.等于0.8mol/L B.等于1.6mol/L
C.0.8 mol/L <c(CH4)<1.6 mol/L D.大于1.6 mol/L
(4)300℃时,如果该容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O(g),则v正____v逆(填“>”“<”或“=”)。
(5)已知:200℃时.该反应的平衡常数K=61.8L2·mol-2。则△H4___0(填“>”“<”或“=”)。
方案Ⅲ:用碱溶液吸收CO2
利用100mL3mol/LNaOH溶液吸收4.48LCO2(标准状况),得到吸收液。
(6)该吸收液中离子浓度的大小排序为____________。将该吸收液蒸干,灼烧至恒重,所得固体的成分是_______(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是( )
A. 用过量氨水吸收工业尾气中的SO2:2NH3H2O+SO2=2NH4++SO32-+H2O
B. 氯化钠与浓硫酸混合加热:H2SO4+2Cl-![]() SO2↑+Cl2↑+H2O
SO2↑+Cl2↑+H2O
C. 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O
D. 明矾溶液中滴入Ba(OH)2溶液使SO42-,恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图的说法不正确的是( )

A. 1mol固态碘与![]() 化合生成2molHI气体时,需要吸收5kJ的能量
化合生成2molHI气体时,需要吸收5kJ的能量
B. 2molHI气体分解生成1mol碘蒸气与![]() 时需要吸收12kJ的能量
时需要吸收12kJ的能量
C. 1mol固态碘变为1mol碘蒸气时需要吸收17kJ的能量
D. 碘蒸气与![]() 生成HI气体的反应是吸热反应
生成HI气体的反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对CH4与Cl2的反应(如图所示)叙述不正确的是
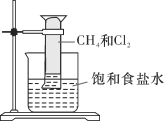
A. 该反应的生成物有四种
B. 该反应属于取代反应
C. 该反应的条件是光照
D. 该反应的现象是量筒内气体颜色变浅,器壁上有油状液滴,量筒内液面上升并产生白雾,溶液中有晶体析出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com