
【题目】莽草酸是合成治疗禽流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如右下:
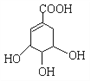
(1)A分子中官能团的名称是________________。
(2)A的分子式是_____________________。
(3)1mol A与氢氧化钠溶液完全反应,需要消耗NaOH的物质的量是_____________。
(4)A在浓硫酸作用下加热可得到 B(B的结构简式为![]() ),B的同分异构体中既含有酚羟基又含有酯基的共有__ 种,写出其中一种同分异构体的结构简式__________
),B的同分异构体中既含有酚羟基又含有酯基的共有__ 种,写出其中一种同分异构体的结构简式__________
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】如图1是细胞中化合物含量的扇形图,图2是有活性的细胞中元素含量的柱形图,下列说法不正确的是( )

A. 若图1表示细胞鲜重,则A、B化合物依次是H2O、蛋白质
B. 若图2表示组成人体细胞的元素含量,则a、b、c依次是O、C、H
C. 地壳与活细胞中含量最多的元素都是a,因此说明生物界与非生物界具有统一性
D. 若图1表示细胞完全脱水后化合物的含量,则A化合物具有多样性,其中含的元素为C、H、O、N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关离子浓度之间的关系不正确的是
A. 将CO2通入0.1mol/LNa2CO3溶液至中性,溶液中:2c(CO32-)+c(HCO3-)=0.lmol/L
B. 浓度均为0.1mol/L的CH3COOH与CH3COONa溶液等体积混合后,pH=5,则混合溶液中:c(CH3COO-)-c(CH3COOH)=2×(10-5-10-9)mol/L
C. 将0.2mol/LNaHCO3溶液与0.1mol/LKOH溶液等体积混合:3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
D. 已知Ka(CH3COOH)=Kb(NH3·H2O)=1.8×10-5,则常温下0.1mol/LCH3COONH4中:c(CH3COO-): c(NH3·H2O)=180
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是 ( )
A. 元素电负性越大的原子,吸引电子的能力越强
B. 在![]() 和
和![]() 中都存在配位键
中都存在配位键
C. SO2、SO3都是极性分子
D. 原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.5 mol CH4的质量是________,在标准状况下的体积为________。
(2)3.1 g Na2X含有Na+ 0.1 mol,则Na2X的摩尔质量为________,X的相对原子质量为________。
(3)0.6 mol的氧气与0.4 mol臭氧(O3)质量之比为________,分子个数之比为________,氧原子个数之比为________。
(4)8.5 g氢氧根离子含有的电子数目为________。
(5)14 g C2H4与C4H8的混合物所含质子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各氧化还原反应中,水既不作氧化剂,也不作还原剂的是( )。
A. 2F2+2H2O==4HF+O2 B. C+H2O![]() CO+H2
CO+H2
C. 2Na+2H2O==2NaOH+H2↑ D. Cl2+H2O==HCl+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列有关叙述正确的是( )
A. 100g质量分数为46%的酒精溶液中含氧原子总数为4NA
B. 电解精炼铜,当外电路转移NA 个电子时,阳极质量减少32g
C. 1L0.1mol·L-1CH3COOH溶液中含H+的数目为0.1NA
D. 常温下,将1molFe加入足量硝酸中,生成H2的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:

已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)请写出一种能提高“酸浸”速率的措施:________________。
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式:_______________。
(3)“调pH”时pH的调控范围为_____________,试用化学反应原理的相关知识解释滤渣Ⅱ的生成:______________________________________________________。
(4)写出“沉镍”时发生反应的离子方程式:__________________________________,证明Ni2+已经沉淀完全的实验步骤及现象是___________________________________,当Ca2+沉淀完全时,溶液中c(F-)>____________mol·L-1(写出计算式即可)。
(5)操作a的内容是_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是四种常见有机物的比例模型示意图,下列说法正确的是
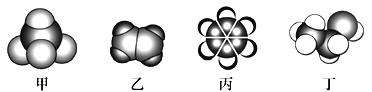
A. 甲能发生氧化反应
B. 乙通入溴的四氯化碳溶液,最后得到无色溶液不能和液溴反应
C. 煤干馏得到的煤焦油可以分离出丙,丙是无色无味的液态烃
D. 丁发生催化氧化得到的产物不能与金属钠反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com