
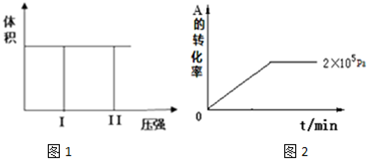
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol?L-1 | 0.08 | 0.20 | 0.44 |
| 1 |
| 2.5 |
| 1 |
| 2 |
| [C]p |
| [A]m |
| [C]p |
| [A]m |
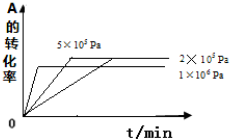 ,故答案为:
,故答案为: .
.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
 )在一定条件下经聚合生成塑料(
)在一定条件下经聚合生成塑料( ),用这种新型塑料制成的餐具,在乳酸菌的作用下,60天内分解成无害物质,最终不会对环境造成污染.在合成该塑料的聚合反应中生成的另一种产物是( )
),用这种新型塑料制成的餐具,在乳酸菌的作用下,60天内分解成无害物质,最终不会对环境造成污染.在合成该塑料的聚合反应中生成的另一种产物是( )| A、H2O |
| B、CO2 |
| C、O2 |
| D、H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
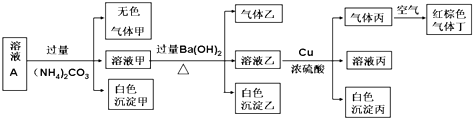
| A、沉淀乙一定有BaCO3,可能有BaSO4 |
| B、实验消耗Cu 14.4g,则生成气体丁的体积为3.36L |
| C、该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子 |
| D、生成的甲、乙、丙气体均为无色的易溶于水气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO32-、HCO3- |
| B、HSO3-、CO32- |
| C、SO32-、CO32- |
| D、HSO3-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)△H<0
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)△H<0查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴水中有下列平衡:Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B、反应 CO+NO2?CO2+NO (△H<0),达平衡后,提高温度体系颜色变深 |
| C、对于 2 HI?H2+I2 达平衡后,缩小体积可使体系颜色变深 |
| D、合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸钠(固体) |
| B、水 |
| C、硫酸钾溶液 |
| D、硫酸铵(固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯碱工业电解饱和食盐水时,阳极电极反应式为 2Cl--2e-=Cl2↑ |
| B、精炼铜时,与电源正极相连的是纯铜,电极反应式为 Cu-2e-=Cu2+ |
| C、氢氧燃料电池的负极反应式 O2+2H2O+4e-=4OH- |
| D、钢铁发生电化腐蚀的正极反应式 Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用
镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用139 57 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com