
| A、若溶液中加入NaOH溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,说明原溶液中含有NH4+ |
| B、若溶液中加入BaCl2溶液有白色沉淀生成,再加稀盐酸沉淀不溶解,说明原溶液中含有SO42- |
| C、若溶液中加入CaCl2溶液有白色沉淀生成,再加稀盐酸沉淀溶解并产生无色无味的气体,说明原溶液中含有CO32- |
| D、若溶液中加稀硝酸酸化后再加入AgNO3溶液有白色沉淀生成,说明原溶液中含有Cl- |


科目:高中化学 来源: 题型:
| A、胶体区别于其它分散系的本质特征是具有丁达尔现象 |
| B、根据化合物中含氢数目的多少,把化合物分为一元酸、二元酸、三元酸等 |
| C、碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 |
| D、强电解质溶液的导电能力一定强于弱电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
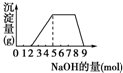 某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随加入的溶液中NaOH的物质的量的变化如图所示:[已知:Mg2++2OH-═Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓,且Mg(OH)2、Fe(OH)3难溶于水;NH4++OH-═NH3?H2O]由此可知,该溶液中肯定含有的离子是
某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随加入的溶液中NaOH的物质的量的变化如图所示:[已知:Mg2++2OH-═Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓,且Mg(OH)2、Fe(OH)3难溶于水;NH4++OH-═NH3?H2O]由此可知,该溶液中肯定含有的离子是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
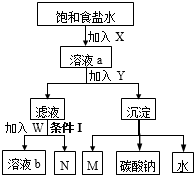
| A、X和M是同种物质 |
| B、W是氯化钠固体和X |
| C、溶液b和N能循环利用 |
| D、条件Ⅰ是加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com