Ti��Fe��Cr��Mn�Ⱦ�Ϊ����Ԫ�أ����������������Ų����������Ҫ���ã����䵥�ʺͻ������Ӧ���о���Ŀǰ��ѧ�о���ǰ��֮һ����ش��������⣺
��1��CrԪ�أ��˵����Ϊ24���Ļ�̬ԭ�ӵ����Ų�ʽΪ
����һ�Ų���ʽ����
����ԭ��������Ƚ�Fe�� Mn�ĸ��������ܺ��֣���̬Mn
2+��ʧȥһ�����ӱ���̬Fe
2+��ʧȥһ������
����ѡ����ס�������ÿ�����֣���6�֣�
��2������Ԫ������������Ԫ�ز�ͬ�ļ۵��ӹ��ͣ�������Χ���ӹ���Ϊ4f
75d
16s
2��Ԫ�������ڱ��д���
�壬����Ԫ�ع���
�֣�
��3��ij���������������ͼ1������Aԭ��Ϊ�����Ķ��㣬Aλ������Ca��Sr��Ba��Pb����Bλ��V��Cr��Mn��Feʱ�����ֻ��������CMRЧӦ���ŵ���ЧӦ������A��B��O��ʾ�������⾧��Ļ�ѧʽ��
��
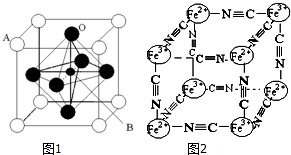
��4����һ����ɫ����ɱ�ʾΪ��[K
xFe
y��CN��
z]���о��������Ľṹ������Fe
2+��Fe
3+�ֱ�ռ��������Ķ��㣬�����������ڣ���CN
һλ������������ϣ�K
+λ�������������ģ���K
+��ȱ��Ϊ50%��������û��K
+��ռ�����ĵİٷֱȣ����侧���е������Ӿ����ṹ��ͼ2��ʾ���þ���Ļ�ѧʽ�ɱ�ʾΪ
��








