
| A、常温常压下,22.4 L乙烯中C-H键数为4 NA |
| B、1 mol羟基中电子数为10 NA |
| C、在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA |
| D、常温下,1 L 0.1 mol/L NH4NO3溶液中NH4+的数目小于6.02×1022 |


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:
| A、火碱液 | B、食盐水 |
| C、牙膏或肥皂水 | D、食醋 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、共价键都是极性的 |
| B、共价键的键能越大,共价键越牢固,含有该键的双原子分子越稳定 |
| C、CF4、CCl4、CBr4、CI4中C-X键的键长、键角均相等 |
| D、H2O分子中2个O-H键夹角为180° |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol NaHSO4固体中含离子总数为3NA |
| B、标准状况下,11.2 L SO3中含有分子的数目为0.5NA |
| C、1 mol FeI2与足量氯气反应时转移的电子数为3NA |
| D、1.6 g由氧气和臭氧组成的混合物中含有分子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
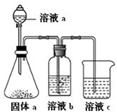 五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:
五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:查看答案和解析>>
科目:高中化学 来源: 题型:
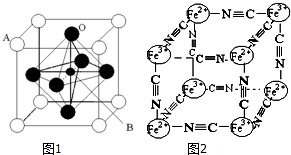
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水中只含Cl2和H2O分子 |
| B、光照氯水有气泡放出,该气体是O2 |
| C、氯水放置一段时间后颜色将变浅 |
| D、新制氯水可使紫色石蕊试液先变红后褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com