
【题目】以下有关同分异构体的说法,错误的是
A.若两种有机物互为同分异构体,则二者的分子式相同
B.分子式为C5H12的的同分异构体有3种
C.1-丁烯、2-丁烯均存在顺反异构
D.同分异构现象的广泛存在是造成有机物种类繁多的重要原因之一
【答案】C
【解析】
A.同分异构体的分子式相同、结构不同,则两种有机物互为同分异构体,分子式一定相同,正确,A不选;
B.C5H12的同分异构体有三种,分别是正戊烷、异戊烷、新戊烷,其结构简式分别是为CH3CH2CH2CH2CH3,(CH3)2CHCH2CH3,C(CH3)3,正确,B不选;
C.若存在顺反异构,则碳碳双键两端的碳原子连有两个不同原子或原子团。1-丁烯的结构式CH2=CHCH2CH3,有个碳碳双键的碳原子连有2个相同的H原子,不存在顺反异构;为2-丁烯,CH3CH=CHCH3,碳碳双键两端的碳原子连接均连接不同的原子或原子团,存在顺反应异构,如果所示: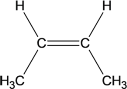 (顺式)、
(顺式)、 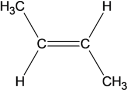 (反式)。错误,C选;
(反式)。错误,C选;
D.碳原子能与多种原子形成四个共价键(碳和碳之间可以形成双键,可以是单键,可以是三键),且碳原子之间相互成键可以成碳链,可以成碳环;此外含碳的有机物存在同分异构现象,也是自然界中有机物种类繁多的主要原因之一,正确,D不选。
答案选C。


科目:高中化学 来源: 题型:
【题目】研究金属与硝酸的反应,实验如下。
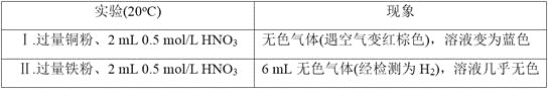
(1)Ⅰ中的无色气体是_________。
(2)Ⅱ中生成H2的离子方程式是______________________________________。
(3)研究Ⅱ中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于NO3-,所以NO3-没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是_______________________________。
②乙同学通过分析,推测出NO3-也能被还原,依据是___________________________,进而他通过实验证实该溶液中含有NH4+,其实验操作是__________________________
(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有_________________________试推测还可能有哪些因素影响_________(列举1条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸工艺的催化氧化反应原理是:2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0,起始以相同的物质的量进行投料,测得SO2在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
2SO3(g)ΔH<0,起始以相同的物质的量进行投料,测得SO2在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
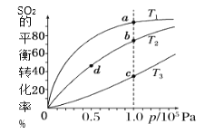
A.温度:T1温度最高
B.正反应速率:υ(a)>υ(b)=υ(d)>υ(c)
C.平均摩尔质量:M(a)<M(b)= M(d)<M(c)
D.平衡常数:K(a)>K(b)=K(d)>K(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题是现代社会发展的三大基本问题之一。
(1)焦炭可用于制取水煤气。实验测得1.2 g 碳与水蒸气完全反应生成水煤气时,吸收了13.16 kJ热量。该反应的热化学方程式为______________;该反应在________条件下能自发进行(选“高温”、“低温”或“任意温度”)。
(2)甲醇(CH3OH)广泛用作燃料电池的燃料,工业上可由CO和H2来合成,化学方程式为CO(g)+2H2(g)![]() CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g)。如图是在不同温度下CO的转化率随时间变化的曲线。
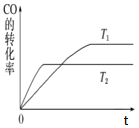
①T1和T2温度下的平衡常数大小关系是K1________(填“>”、“<”或“=”)K2。
②若容器容积不变,下列措施不能增加CO转化率的是________(填字母)。
a.降低温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂
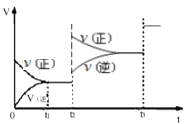
③生成甲醇的化学反应速率(v)与时间(t)的关系如图所示。则图中t2时采取的措施可能是_____;
④若在T1℃时,往一密闭容器通入等物质的量CO和H2测得容器内总压强1MPa,40min达平衡时测得容器内总压强为0.6MPa,计算生成甲醇的压强平衡常数KP=________(MPa)-2(小数点后保留2位小数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)甲醇(CH3OH)燃料电池是以铂为电极,以KOH溶液为电解质溶液,在两极区分别加入CH3OH和O2即可产生电流。请写出负极的电极反应为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H是一种广谱高效食品防腐剂,如图所示是H分子的球棍模型,下列有关说法正确的是
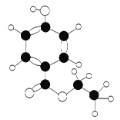
A. 有机物H的分子式为C9H11O3
B. 有机物H的官能团有羟基、羰基和醚键
C. 有机物H能发生加成反应、取代反应和氧化反应
D. 1mol有机物H最多可与1molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是碳和碳的化合物的转化关系:C![]() CO2
CO2![]() H2CO3
H2CO3![]() CaCO3
CaCO3![]() CO2。其各步转化的基本反应类型从左到右依次是( )。
CO2。其各步转化的基本反应类型从左到右依次是( )。
A.化合、分解、置换、复分解B.置换、化合、复分解、分解
C.复分解、化合、分解、置换D.分解、置换、化合、复分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通立德粉(BaSO4·ZnS)广泛用于工业生产中,可利用ZnSO4和BaS共沉淀法制备。以粗氧化锌(含Zn、CuO、FeO等杂质)和BaSO4为原料制备立德粉的流程如下:
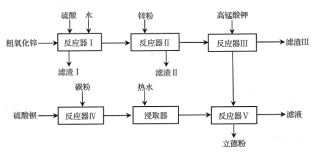
(1)生产ZnSO4的过程中,反应器Ⅰ要保持强制通风,原因是___。
(2)加入锌粉的主要目的是___(用离子方程式表示)。
(3)已知KMnO4在酸性溶液中被还原为Mn2+,在弱酸性、弱碱性溶液中被还原为MnO2,在碱性溶液中被还原为MnO42-。据流程判断,加入KMnO4时溶液的pH应调至___;
a.2.2~2.4 b.5.2~5.4 c.12.2~12.4
滤渣Ⅲ的成分为____。
(4)制备BaS时,按物质的量之比计算,BaSO4和碳粉的投料比要大于1:2,目的是__;生产过程中会有少量氧气进入反应器Ⅳ,反应器Ⅳ中产生的尾气需用碱液吸收,原因是__。
(5)普通立德粉(BaSO4·ZnS)中ZnS含量为29.4%,高品质银印级立德粉中ZnS含量为62.5%。在ZnSO4、BaS、Na2SO4、Na2S中选取三种试剂制备银印级立德粉,所选试剂为___,反应的化学方程式为__(已知BaSO4相对分子质量为233,ZnS相对分子质量为97)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应CCl4+4Na![]() C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是( )
C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是( )
A. C(金刚石)属于原子晶体
B. 该反应利用了Na的强还原性
C. CCl4和C(金刚石)中C的杂化方式相同
D. NaCl晶体中每个Cl-周围有8个Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用12mol·L-1的浓盐酸配制0.10mol·L-1的稀盐酸500 mL。回答下列问题。
(1)关于容量瓶的使用,下列操作正确的是___(填序号)。
a.使用前要检验容量瓶是否漏液
b.用蒸馏水洗涤后必须要将容量瓶烘干
c.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
d.为了使所配溶液浓度均匀,定容结束后,要摇匀
e.用500mL的容量瓶可以直接配制480mL溶液
f.当用容量瓶配制完溶液后,可用容量瓶存放配制的试剂
(2)量取浓盐酸的体积为___mL,应选用的量筒规格为___(填“10mL”“25mL”或“50mL”)。
(3)配制时应选用的容量瓶规格为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com