
【题目】某学生用12mol·L-1的浓盐酸配制0.10mol·L-1的稀盐酸500 mL。回答下列问题。
(1)关于容量瓶的使用,下列操作正确的是___(填序号)。
a.使用前要检验容量瓶是否漏液
b.用蒸馏水洗涤后必须要将容量瓶烘干
c.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
d.为了使所配溶液浓度均匀,定容结束后,要摇匀
e.用500mL的容量瓶可以直接配制480mL溶液
f.当用容量瓶配制完溶液后,可用容量瓶存放配制的试剂
(2)量取浓盐酸的体积为___mL,应选用的量筒规格为___(填“10mL”“25mL”或“50mL”)。
(3)配制时应选用的容量瓶规格为___。
【答案】ad 4.2 10mL 500mL
【解析】
(1)根据容量瓶的构造和使用方法及其注意事项分析判断;
(2)配制500mL稀盐酸,需要选用500mL容量瓶进行配制,根据配制过程中溶质HCl的物质的量不变计算出需要浓盐酸的体积,并判断选用的量筒规格。
(1)a.容量瓶口部有塞子,使用前要先检查容量瓶是否漏液,故a正确;b.容量瓶用蒸馏水洗净后不影响溶液的体积,浓度不变,所以不需要干燥,故b错误;c.容量瓶不能用来稀释和溶解物质,故c错误;d.为了使所配溶液浓度均匀,定容结束后,需要颠倒摇匀,故d正确;e.实验室没有480mL的容量瓶,应该选用500mL的容量瓶,但不能在容量瓶中直接配制溶液,需要将溶质先在烧杯中溶解后再转移到容量瓶中定容,故e错误;f.容量瓶不能存放配制的试剂,故f错误;故答案为:ad;
(2)用12molL-1的浓盐酸配制0.10molL-1的稀盐酸500mL,需要该浓盐酸的体积为![]() ≈0.0042L=4.2mL,要量取4.2mL浓盐酸,应该选用10mL的量筒,故答案为:4.2;10mL;
≈0.0042L=4.2mL,要量取4.2mL浓盐酸,应该选用10mL的量筒,故答案为:4.2;10mL;
(3)配制0.10mol·L-1的稀盐酸500 mL,需要选用500mL容量瓶进行配制,故答案为:500mL。


科目:高中化学 来源: 题型:
【题目】在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)![]() 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是

A. 图中a点的值为0.15 B. 该反应的平衡常数K=0.03
C. 温度升高,平衡常数K值减小 D. 平衡时A2的转化率为62.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向某溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀 | 原溶液中有Fe2+,无Fe3+ |
B | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
C | 向碘水中加入等体积的CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
D | 向某溶液中先加入Ba(NO3)2溶液,有白色沉淀生成;再加入足量盐酸,白色沉淀不消失 | 原溶液中一定含有SO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.铁和硫酸铜溶液的反应:2Fe+Cu2+=2Fe3++Cu
B.在硫酸溶液中加入氢氧化钠溶液:H++OH-=H2O
C.硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓
D.向沸水中滴加氯化铁饱和溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为金属单质,下列物质相互转化如图所示:

试回答:
(1)写出B的化学式_______,D的化学式______。
(2)写出由E转变成F的化学方程式______。
(3)检验G溶液中阳离子的试剂为______,写出发生反应的离子方程式______。
(4)向G溶液加入A的有关离子反应方程式______。
(5)某同学取B的溶液酸化后加入碘化钾淀粉溶液,在空气中放置一会儿变为蓝色,写出与上述变化过程相关的离子方程式______,______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数的值用NA表示,则:
(1)该气体的物质的量为___mol。
(2)该气体所含原子总数为___个。
(3)该气体在标准状况下的体积为___L。
(4)该气体一个分子的质量为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多种短周期非金属元素的气态氧化物常会造成一些环境污染问题,化学工作者设计出将工业废气中污染物再利用的方案,以消除这些不利影响。
(1)以NH3、CO2为原料生产重要的高效氮肥——尿素[CO(NH2)2],两步反应的能量变化示意图如下:
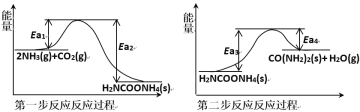
写出以氨气和二氧化碳气体为原料合成尿素的热化学方程式_________,已知两步反应中第二步反应是生产尿素的决速步骤,可判断Ea1_____Ea3(填“>”、“<”或“=”)。
(2)向体积为2 L的恒温恒容容器中通入2 mol CO和2 mol SO2,发生反应2CO(g)+SO2(g)![]() 2CO2(g)+S(s)。若反应进行到10 min时达平衡,测得CO2的体积分数为0.5,则前16 min的平均反应速率v(CO)=____,该温度下反应化学平衡常数K=____。
2CO2(g)+S(s)。若反应进行到10 min时达平衡,测得CO2的体积分数为0.5,则前16 min的平均反应速率v(CO)=____,该温度下反应化学平衡常数K=____。
(3)利用“亚硫酸盐法”吸收工业废气中的SO2。

①室温条件下,将工业废气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示,b点溶液中n(![]() )∶n(
)∶n(![]() )=________。
)=________。
②已知室温条件下,Ka1(H2SO3) =1.5×10-2;Ka2(H2SO3) =1.0×10-7;Kb(NH3H2O) =1.8×10-5。室温下,0.1molL-1的(NH4)2SO3溶液中离子浓度(不考虑OH-)由大到小顺序为________。
(4)利用电解烧碱和食盐的混合液,使工业废气脱氮,原理如图。
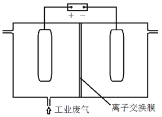
①NO被阳极产生的氧化性物质氧化为![]() 反应的离子方程式:_________________。
反应的离子方程式:_________________。
②为使该电解装置能较长时间正常工作,保持两极电解质溶液导电能力相对稳定,该装置中应使用_______ 离子交换膜(填“阴”或“阳”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关甲、乙、丙、丁四个图示的叙述不正确的是( )
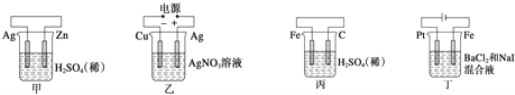
A.甲中负极反应式为![]()
B.乙中阳极反应式为![]()
C.丙中![]() 向碳棒方向移动
向碳棒方向移动
D.丁中电解开始时阳极产生黄绿色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
c(NaOH) | 阴极现象 | 阳极现象 |
1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法不正确的是

A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com