
【题目】绿原酸是金银花的主要抗菌、抗病毒有效药理成分之一,其结构如图所示。下列有关说法正确的是( )
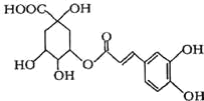
A.分子式为C16H16O9
B.能与碳酸钠溶液反应,但不产生二氧化碳
C.能发生催化氧化反应并生成能发生银镜反应的产物
D.NaOH、H2、溴水分别与1mol绿原酸反应时,消耗反应物的最大物质的量都为4mol
【答案】D
【解析】
该分子中含有醇羟基、羧基、酯基、碳碳双键、苯环、酚羟基,具有醇、羧酸、酯、烯烃、苯和酚的性质,能发生氧化反应、消去反应、酯化反应、水解反应、加成反应、取代反应等。
A.根据结构简式知,分子式为C16H18O9,故A错误;
B.羧基能和碳酸钠反应生成二氧化碳,故B错误;
C.醇羟基能发生催化氧化,但不能生成醛基,所以其氧化产物不能发生银镜反应,故C错误;
D.酚羟基、羧基、酯基水解生成的羧基能和NaOH反应,1mol该物质最多消耗4molNaOH,苯环和碳碳双键能和氢气发生加成反应,所以1mol该物质最多能和4mol氢气发生加成反应,碳碳双键和溴发生加成反应,连接酚羟基的苯环上邻对位氢原子能和溴发生取代反应,则1mol该物质最多能和4mol溴发生反应,故D正确;
故选D。


科目:高中化学 来源: 题型:
【题目】某烷烃主链上有4个碳原子的同分异构体有2种,含有相同碳原子数且主链上也有4个碳原子的单烯烃的同分异构体有( )
A. 2种 B. 4种
C. 5种 D. 7种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列变化进行推断:
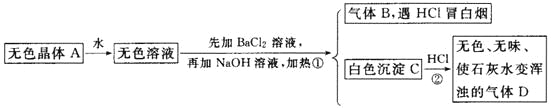
且已知对A加强热产生的气态物质的平均相对分子质量为26.3。
(1)推断A、B、C、D的化学式:A________,B________,C________,D________。
(2)写出①②变化的离子方程式:
①________________________________________________________________;
②________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务。
(1)汽车内燃机工作时发生反应:N2(g)+O2(g)![]() 2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向5L密闭容器中充入6.5molN2和7.5molO2,在5min时反应达到平衡状态,此时容器中NO的物质的量是5mol。
2NO(g),是导致汽车尾气中含有NO的原因之一。T℃时,向5L密闭容器中充入6.5molN2和7.5molO2,在5min时反应达到平衡状态,此时容器中NO的物质的量是5mol。
①5min内该反应的平均速率υ(NO)=___;在T℃时,该反应的平衡常数K=___。
②反应开始至达到平衡的过程中,容器中下列各项发生变化的是___(填序号)。
a.混合气体的密度
b.混合气体的压强
c.正反应速率
d.单位时间内,N2和NO的消耗量之比
(2)H2或CO可以催化还原NO以达到消除污染的目的。
已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镓(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝在元素周期表中的位置是__________________。
(2)GaAs 是一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是___________(填字母)。
a. 碱性:Ga (OH)3> Al (OH)3 b. 非金属性:As>Ga c. 酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释原因_________________。
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式_________。
(3)工业上获取镓的方法之一是从闪锌矿冶锌后的残渣(主要含有 Zn、Pb、Fe、Ga 等元素)中提取,某科研单位设计下述流程提取镓,已知:Ga 在碱性溶液中以[Ga(OH)4]- 形式存在。
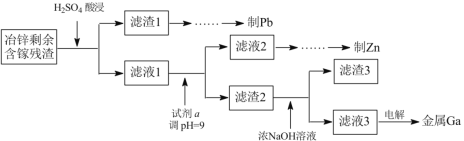
①试剂 a 是_______________。
②写出电解制镓时的阴极电极反应式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钠(NaH)是一种白色的离子化合物,其中钠元素为+1价,NaH与水反应生成氢气,下列叙述正确的是( )
A.NaH在水中显酸性B.NaH中氢离子电子排布与氦原子相同
C.NaH中氢离子半径比锂离子大D.NaH中氢离子可以被还原成氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.(CH3)2C(Cl)CH2CH3的名称为:2-氯-2-甲基丁烷
B.可用新制氢氧化铜浊液鉴别乙醇、乙酸溶液
C.1mol有机物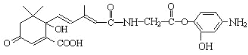 )与NaOH溶液反应,最多消耗5molNaOH
)与NaOH溶液反应,最多消耗5molNaOH
D.1molβ-紫罗兰酮(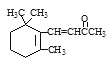 )与1molBr2发生加成反应可得到3种不同产物(不考虑立体异构)
)与1molBr2发生加成反应可得到3种不同产物(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含碳化合物在生产生活中广泛存在,Andren Dasic等提出在M+的作用下以N2O为氧化剂可以氧化乙烯生成乙醛,催化体系氧化还原循环如图所示,请回答下列问题。
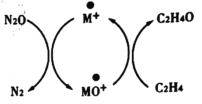
(1)已知N2O(g)+M+(s)=N2(g)+MO+(s) ΔH1=+678kJ·mol-1
MO+(s)+C2H4(g)=C2H4O(g)+M+(s) ΔH2=-283kJ·mol-1
请写出在M+的作用下以N2O为氧化剂氧化乙烯生成乙醛的热化学方程式:_________
(2)已知在含少量的I2溶液中,反应CH3CHO (aq)![]() CH4 (g) +CO (g)分两步进行:第Ⅰ步反应CH3CHO (aq) +I2 (aq) →CH3I (l) +HI (aq) +CO (g) (慢反应),第II步为快反应。
CH4 (g) +CO (g)分两步进行:第Ⅰ步反应CH3CHO (aq) +I2 (aq) →CH3I (l) +HI (aq) +CO (g) (慢反应),第II步为快反应。
①决定此反应快慢的是第______(填“Ⅰ”或“II”)步反应
②请写出第II步反应的化学方程式:_________
(3)若物质与氧原子的结合力用OA表示,氧原子与N2生成N2O的结合力OA(N2) =167.4 kJ·mol-1, 氧原子与乙烯生成乙醛的结合力OA (C2H4) = 473 kJ·mol-1,则可做该反应催化剂的M+与氧原子的的结合力OA (M+)的值应满足________,使用催化剂会使该反应的活化能________ (填“增大”、 “减小”、“不变”)。
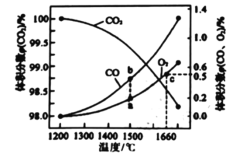
(4)某2L容器中发生: 2CO2(g)![]() 2CO (g)+O2 (g),2molCO2在不同温度下平衡分解的情况如图所示。
2CO (g)+O2 (g),2molCO2在不同温度下平衡分解的情况如图所示。
①恒温恒容条件下,能表示该可逆反应达到平衡状态的是______(填标号)
A.CO体积分数与O2体积分数的比值保持不变
B.容器内混合气体的密度保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.容器内碳元素的质量分数保持不变
②图中a、b、c三点的平衡常数K(a)、K(b)、K(c)的大小关系为_______
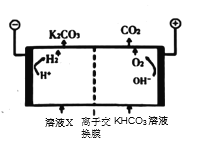
③为实现CO2减排,目前较成熟的方法是用高浓度的K2CO3溶液吸收工业烟气中的CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图,用必要的文字和化学用语简述![]() 在阴极区再生的原理____________。
在阴极区再生的原理____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。回答下列问题:
(1)基态Fe3+的电子排布式为________。
(2)实验室用KSCN溶液、苯酚(![]() )检验Fe3+。N、O、S的第一电离能由大到小的顺序为_______(用元素符号表示),苯酚中碳原子的杂化轨道类型为______。
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为_______(用元素符号表示),苯酚中碳原子的杂化轨道类型为______。
(3)FeCl3的熔点为306℃,沸点为315℃ FeCl3的晶体类型是______。FeSO4常作补铁剂,SO42-的立体构型是_______。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等,1 mol Fe(CO)5分子中含σ键数目为_______,与CO互为等电子体的离子是__________(填化学式,写一种)
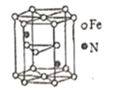
(5)氮化铁晶体的晶体结构示意图如图所示。该晶体中铁、氮的微粒个数之比为______。
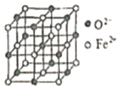
(6)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρg·cm-1,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-的最短间距为_______ pm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com