
| A. | BaSO4属于难溶物,它在水中完全不能溶解 | |
| B. | 沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等 | |
| C. | 沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变 | |
| D. | 沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
分析 A.绝对难溶的物质不存在;
B.沉淀溶解达到平衡是动态平衡;
C.溶质组成不同,离子浓度不一定相同;
D.沉淀溶解达到平衡时,在加入该沉淀沉淀不能继续溶解,固体的浓度为常数,加入难溶的该沉淀物,平衡不发生移动.
解答 解:A.BaSO4属于难溶物,它在水中溶解度小,溶解的全部电离,故A错误;
B.沉淀的速率和溶解的速率相等,沉淀溶解达到平衡,沉淀的速率和溶解的速率相等,故B正确;
C.沉淀溶解达到平衡时,溶液中溶质的离子浓度保持不变,但不一定相等,与难溶二者是否是1:1型有关、与溶解难溶物质的溶液中是否存在难溶物质的离子等有关,故C错误;
D、沉淀溶解达到平衡时,如果再加入难溶的该沉淀物,由于固体的浓度为常数,故平衡不发生移动,故D错误;
故选B.
点评 本题考查难溶物质的溶解平衡,题目难度不大,注意利用平衡移动原理、溶度积常数理解.


科目:高中化学 来源: 题型:解答题
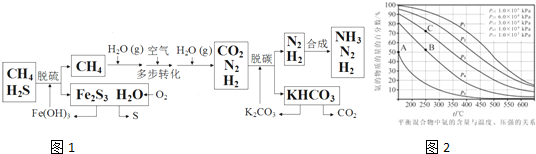
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
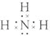
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 112mL | B. | 224mL | C. | 118.72 mL | D. | 201.6 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2>I->Fe2+>Cl- | B. | I->Fe2+>Cl->SO2 | C. | Cl->Fe2+>SO2>I- | D. | Fe2+>I->Cl->SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
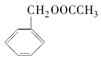 )是其中的一种,它可以从茉莉花中提取,也可以用乙烯和甲苯为原料进行人工合成.其中一种合成路线如图:
)是其中的一种,它可以从茉莉花中提取,也可以用乙烯和甲苯为原料进行人工合成.其中一种合成路线如图: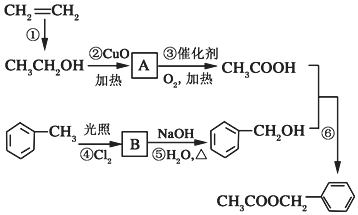
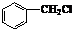 ;
;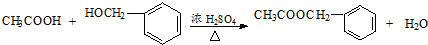 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
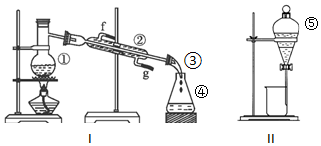
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子的稳定性与分子间作用力的大小无关 | |
| B. | BF3、NCl3、H2O分子中所有原子都满足最外层为8电子结构的是NCl3 | |
| C. | NH4+和CH4属于等电子体,立体构型都是正四面体 | |
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com