
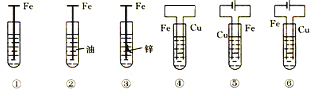
ЁОЬтФПЁПШчЯТЭМЃЌЬњИЏЪДгЩПьЕНТ§ЕФЫГађЮЊЃЈЕчНтжЪШмвКЮЊЫЎЃЉ
A.Ђо>Ђм>Ђл>Ђк>Ђй>ЂнB.Ђн>Ђл>Ђй>Ђк>Ђм>Ђо
C.Ђн>Ђм>Ђй>Ђк>Ђл>ЂоD.Ђн>Ђм>Ђк>Ђй>Ђл>Ђо
ЁОД№АИЁПC
ЁОНтЮіЁП
ИљОнЭМжЊЃЌЂйЂлЂмзАжУЪЧдЕчГиЃЌдкЂмжаЃЌН№ЪєЬњзїИКМЋЃЌЂлжаН№ЪєЬњзїе§МЋЃЌзїИКМЋЕФИЏЪДЫйТЪПьЃЌСНИіЕчМЋН№ЪєЛюЦУадЯрВюдНДѓЃЌИКМЋН№ЪєИЏЪДЫйТЪдНПьЃЌе§МЋБЛБЃЛЄЃЌДЫЭтдЕчГидРэв§Ц№ЕФИЏЪД>ЛЏбЇИЏЪДЃЌЫљвдЂм>Ђл>ЂйЃЌЂнЂозАжУЪЧЕчНтГиЃЌЂнжаН№ЪєЬњЮЊбєМЋЃЌЂожаН№ЪєЬњЮЊвѕМЋЃЌбєМЋН№ЪєБЛИЏЪДЫйТЪПьЃЌвѕМЋБЛБЃЛЄЃЌМДЂн>ЂоЃЌИљОнЕчНтдРэв§Ц№ЕФИЏЪД>дЕчГидРэв§Ц№ЕФИЏЪД>ЛЏбЇИЏЪД>гаЗРЛЄИЏЪДДыЪЉЕФИЏЪДЃЌВЂЧвдЕчГиЕФе§МЋН№ЪєИЏЪДЫйТЪПьгкЕчНтГиЕФвѕМЋН№ЪєИЏЪДЫйТЪЃЌЂкУЛгаЫЎЕФДцдкИЏЪДЫйТЪКмТ§ЃЌМДИЏЪДЫйТЪЂн>Ђм>Ђй>Ђк>Ђл>ЂоЃЛ
ЙЪбЁCЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁППеЦјжаКЌгаЮќШыПХСЃЮяPM2.5ЃЌбЯжигАЯьШЫЕФЩњРэКЭНЁПЕЃЌвђДЫИФЩЦЗЂжЪНсЙЙЁЂЛњЖЏГЕСОДыЪЉФмгааЇМѕЩйPM2.5ЁЂSO2ЁЂNO3ЕШЕФЮлШОЁЃЧыЛиД№ЯТСаЮЪЬтЃК
(1)НЋвЛЖЈСПЕФФГPM2.5бљЦЗгУеєСѓЫЎШмНтжЦГЩД§ВтЪдбљ(КіТдOH-)ЁЃГЃЮТЯТЃЌВтЕУИУЪдбљЕФзщГЩМАЦфХЈЖШШчЯТБэЃК
Рызг | K+ | Na+ | NH4+ | SO42- | NO3Љ | ClЉ |
ХЈЖШ/molЁЄL-1 | 4ЁС10-6 | 6ЁС10-6 | 2ЁС10-5 | 4ЁС10-5 | 3ЁС10-5 | 2ЁС10-5 |
ИљОнБэжаЪ§ОнХаЖЯЃЌИУЪдбљЕФpH = ________ЁЃ
(2)ЦћГЕЮВЦјжаNOxКЭCOЕФЩњГЩЁЃвбжЊЃКЦјИзжаЩњГЩNOЕФЗДгІЮЊN2(g)+O2(g)![]() 2NO(g) ЁїHЃО0ЁЃКуЮТЃЌКуШнУмБеШнЦїжаЃЌЯТСаа№ЪіЃЌФмЫЕУїИУЗДгІДяЕНЛЏбЇЦНКтзДЬЌЕФЪЧ________ (ЬюађКХ)ЁЃ
2NO(g) ЁїHЃО0ЁЃКуЮТЃЌКуШнУмБеШнЦїжаЃЌЯТСаа№ЪіЃЌФмЫЕУїИУЗДгІДяЕНЛЏбЇЦНКтзДЬЌЕФЪЧ________ (ЬюађКХ)ЁЃ
A.ЛьКЯЦјЬхЕФУмЖШВЛдйБфЛЏ B.ЛьКЯЦјЬхЕФЦНОљЗжзгжЪСПВЛдйБфЛЏ
C.N2ЁЂO2ЁЂNOЕФЮяжЪЕФСПжЎБШЮЊ1ЃК1ЃК2 D.бѕЦјЕФзЊЛЏТЪВЛдйБфЛЏ
E.ЩњГЩlmol N2ЕФМфЪБгаlmol O2БЛЯћКФ
(3)ЮЊМѕЩйCO2ЁЂSO2ЕФХХЗХЃЌГЃВЩШЁЕФДыЪЉШчЯТ:
ЂйНЋУКзЊЛЏЮЊ[НрЦјЬхШМСЯЁЃМКжЊЃКH2(g)+1/2O2(g)= H2O(g) ЁїH =-241.8kJ mol-1ЃЛ C(s)+1/2O2(g)=CO(g) ЁїH =-110.5kJ mol-1ЁЃаДГіНЙЬПгыЫЎеєЦјЗДгІЕФШШЛЏбЇЗНГЬЪНЃК_____________________________________ЁЃ
ЂкЯДЕгКЌSO2ЕФбЬЦјЁЃЯТСаЮяжЪЃЌПЩзїЮЊЯДЕгКЌSO2бЬЦјЕФЯДЕгМСЕФЪЧ______(ЬюађКХ)ЁЃ
A.ХЈАБЫЎ B.ЬМЫсЧтФЦБЅКЭШмвК C.FeCl3БЅКЭШмвК D.ЫсадCaCl2БЅКЭШмвК
(4)ФГЪЊЖШЯТЃЌЗДгІ2NO(g)+O2(g) ![]() 2NO2(g)жаЃЌдкБЃжЄO2ХЈЖШВЛБфЕФЧщПіЯТЃЌдіДѓШнЦїЕФЬхЛ§, ЦНКтНЋ_____(ЬюЁАе§ЗДгІЗНЯђЁБ ЁАФцЗДгІЗНЯђЁБЛђЁАВЛЁБ)вЦЖЏЁЃ
2NO2(g)жаЃЌдкБЃжЄO2ХЈЖШВЛБфЕФЧщПіЯТЃЌдіДѓШнЦїЕФЬхЛ§, ЦНКтНЋ_____(ЬюЁАе§ЗДгІЗНЯђЁБ ЁАФцЗДгІЗНЯђЁБЛђЁАВЛЁБ)вЦЖЏЁЃ
ХаЖЯЕФвРОнЪЧ__________________________________ЁЃ
(5)МзДМШМСЯЕчГиПЩФмГЩЮЊЮДРДБуаЏЕчзгВњЦЗгІгУЕФжїСїЁЃФГжжМзДМШМСЯЕчГиЕФЙЄзїдРэШчЭМ14ЫљЪОЃЌдђЭЈШыaЦјЬхЕФЕчМЋЃЌЕчМЋЗДгІЪНЮЊ_________________ЁЃ

(6)ЁЊЖЈЬѕМўЯТЃЌМзДМгывЛбѕЛЏЬМЗДгІПЩвдКЯГЩввЫсЁЃГЃЮТЬѕМўЯТЃЌНЋa mol/LЕФCH3COOHШмвКгыbmol/LBa(OH)2ШмвКЕШЬхЛ§ЛьКЯЃЌЗДгІЦНКтЪБЃЌ2c(Ba2+)=c(CH3COO-)ЃЌгУКЌaКЭbЕФДњЪ§ЪНБэЪОЃЌИУЛьКЯШмвКжаДзЫсЕФЕчРыГЃЪ§ЮЊ___________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌгУ0.1000 mol/LЕФNaOHБъзМШмвКЕЮЖЈ20.00 mL0.1000 mol/LЕФHClШмвКЃЌЕЮЖЈЧњЯпШчЭМЃЌЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ( )
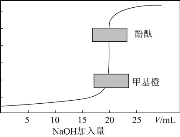
A.жИЪОМСБфЩЋЪБЃЌЫЕУїЗДгІЕФЫсЁЂМюЧЁКУЕШЮяжЪЕФСПЗДгІ
B.ЕБДяЕНЕЮЖЈжеЕуЪБВХДцдкc(Na+)+c(H+)=c(Cl-)+c(OH-)
C.ДяЕНЕЮЖЈжеЕуЪБЃЌгУМзЛљГШзїжИЪОМСЯћКФNaOHШмвКЬхЛ§БШгУЗгЬЊЖр
D.вбжЊH+(aq)+OH-(aq)=H2O(l)ЁїH=-57.3 kJ/molЃЌЩЯЪіЕЮЖЈЧЁКУжаКЭЪБЃЌЗХГі114.6JЕФШШСП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСагаЛњЮяУќУће§ШЗЕФЪЧ
A. 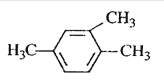 1,3,4-Ш§МзБН
1,3,4-Ш§МзБН
B. 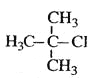 2-МзЛљ-2-ТШБћЭщ
2-МзЛљ-2-ТШБћЭщ
C. 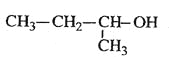 2-МзЛљ-1-БћДМ
2-МзЛљ-1-БћДМ
D. 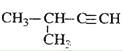 2-МзЛљ-3-ЖЁШВ
2-МзЛљ-3-ЖЁШВ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
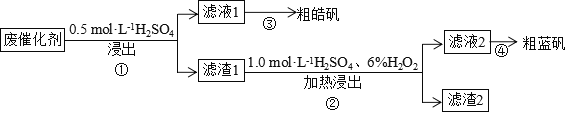
ЁОЬтФПЁПФГЗЯДпЛЏМСКЌ![]() ЁЂZnSЁЂCuSМАЩйСПЕФ
ЁЂZnSЁЂCuSМАЩйСПЕФ![]() ЁЃФГЪЕбщаЁзщвдЗЯДпЛЏМСЮЊдСЯЃЌЛиЪеаПКЭЭЁЃЩшМЦЪЕбщСїГЬШчЯТЃКвбжЊЃКCuSМШВЛШмгкЯЁСђЫсЃЌвВВЛгыЯЁСђЫсЗДгІЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЁЃФГЪЕбщаЁзщвдЗЯДпЛЏМСЮЊдСЯЃЌЛиЪеаПКЭЭЁЃЩшМЦЪЕбщСїГЬШчЯТЃКвбжЊЃКCuSМШВЛШмгкЯЁСђЫсЃЌвВВЛгыЯЁСђЫсЗДгІЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.ТЫвК1жаЪЧЗёКЌга![]() ЃЌПЩвдбЁгУKSCNКЭаТжЦЕФТШЫЎМьбщ
ЃЌПЩвдбЁгУKSCNКЭаТжЦЕФТШЫЎМьбщ
B.ВНжш![]() ВйзїжаЃЌЯШМг
ВйзїжаЃЌЯШМг![]()
![]() ЃЌдкВЛЖЯНСАшЯТЃЌдйМгШы
ЃЌдкВЛЖЯНСАшЯТЃЌдйМгШы![]()
![]()
C.ТЫдќ1ГЩЗжЪЧ![]() КЭCuSЃЌТЫдќ2ГЩЗжвЛЖЈЪЧ
КЭCuSЃЌТЫдќ2ГЩЗжвЛЖЈЪЧ![]()
D.ВНжш![]() ВйзїжаЃЌЩњГЩЕФЦјЬхашгУNaOHШмвКЛђ
ВйзїжаЃЌЩњГЩЕФЦјЬхашгУNaOHШмвКЛђ![]() ШмвКЮќЪе
ШмвКЮќЪе
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЮТЖШЯТЃЌдкШ§ИіШнЛ§ОљЮЊ1 LЕФКуШнУмБеШнЦїжаАДВЛЭЌЗНЪНЭЖШыЗДгІЮяЃЌЗЂЩњЗДгІCO(g)ЃЋ2H2(g)![]() CH3OH(g)(е§ЗДгІЗХШШ)ЃЌВтЕУЗДгІЕФЯрЙиЪ§ОнШчЯТЃК
CH3OH(g)(е§ЗДгІЗХШШ)ЃЌВтЕУЗДгІЕФЯрЙиЪ§ОнШчЯТЃК
ШнЦї | ШнЦї1 | ШнЦї2 | ШнЦї3 |
ЗДгІЮТЖШT/K | 500 | 500 | 600 |
ЗДгІЮяЭЖШыСП | 1 mol COЁЂ 2 mol H2 | 2 mol CH3OH | 1 mol COЁЂ 2 mol H2 |
ЦНКтvе§(H2)/(molЁЄLЃ1ЁЄsЃ1) | v1 | v2 | v3 |
ЦНКтc(CH3OH)/(molЁЄLЃ1) | c1 | c2 | c3 |
ЦНКтЬхЯЕзмбЙЧПp/Pa | p1 | p2 | p3 |
ЮяжЪЕФзЊЛЏТЪІС | ІС1(CO) | ІС2(CH3OH) | ІС3(CO) |
ЦНКтГЃЪ§K | K1 | K2 | K3 |
ЯТСаа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
A. v1<v2ЃЌ2c1>c2B. ІС1(CO)>ІС3(CO)ЃЌv1<v3
C. p2>2p3ЃЌK1<K3D. c2>2c3ЃЌІС2(CH3OH)ЃЋІС3(CO)<1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМйЩшЭМжадЕчГиВњЩњЕФЕчбЙЁЂЕчСїЧПЖШОљФмТњзуЕчНтЁЂЕчЖЦвЊЧѓЃЌМДЮЊРэЯыЛЏЁЃЂй~ЂрЮЊИїзАжУжаЕФЕчМЋБрКХЁЃЕБKБеКЯКѓЃЌЯТСаЫЕЗЈе§ШЗЕФгаЃЈ ЃЉ
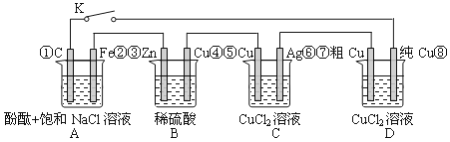
ЂйDзАжУжаДПCuЕчМЋЗДгІЮЊЃКCu2++2e-=Cu
ЂкећИіЕчТЗжаЕчзгЕФСїЖЏЗНЯђЮЊЃКЂлЁњЂк;ЂйЁњЂр;ЂпЁњЂо;ЂнЁњЂм;
ЂлCзАжУдРэЩЯЪЧвЛИіЕчЖЦГи(AgБэУцЖЦCu),ЦкжаCuзївѕМЋЃЌAgзїбєМЋ
ЂмAзАжУжаCЕчМЋЗДгІЮЊЃКO2+4e-+2H2O=4OH-
A. ЂлЂм B. ЂйЂк C. ЂкЂлЂм D. ЂйЂкЂм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖдгкПЩФцЗДгІЃК2A(g)ЃЋB(g)![]() 2C(g) ЁїHЃМ0ЃЌЯТСаИїЭМжае§ШЗЕФЪЧ
2C(g) ЁїHЃМ0ЃЌЯТСаИїЭМжае§ШЗЕФЪЧ
A.
B.
C.
D.
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌгУ0.1000mol/LNaOHШмвКЗжБ№ЕЮЖЈ20.00mL0.1000mol/LHClШмвККЭ20.00mL0.1000mol/LCH3COOHШмвКЃЌЕУЕН2ЬѕЕЮЖЈЧњЯпЃЌШчЯТЭМЫљЪО:
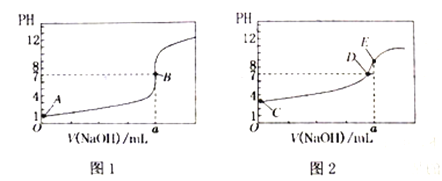
ЃЈ1ЃЉгЩAЁЂCЕуХаЖЯЃЌЕЮЖЈHClШмвКЕФЧњЯпЪЧ__(ЬюЁАЭМ1ЁБЛђЁАЭМ2ЁБ)ЁЃ
ЃЈ2ЃЉa=___mLЁЃ
ЃЈ3ЃЉc(Na+)=c(CH3COO-)ЕФЕуЪЧ_______ЁЃ
ЃЈ4ЃЉEЕуЖдгІРызгХЈЖШгЩДѓЕНаЁЕФЫГађЮЊ________ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com