
【题目】合成氨是人类科技发展史上的一项重大突破。已知25℃时,合成氨反应的热化学方程式为N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4 kJ/mol。请回答下列问题:
2NH3(g) △H=-92.4 kJ/mol。请回答下列问题:
(1)保持容器温度不变,缩小容器体积,化学反应速率_______(填“增大”或“减小”)。
(2)25℃时,取一定量的N2和H2于2 L的密闭容器中在催化剂存在下进行反应达到平衡,若增大N2的浓度,则H2的转化率____(填“增大”或“减小”);若反应达到平衡时放出的热量是92.4 kJ,则生成的NH3为______________mol。
(3)恒温恒容条件下,上述反应达到化学平衡状态的标志是________(填字母代号)。
A. N2、H2、NH3的浓度相等
B.容器内压强不再变化
C.单位时间内消耗a mol N2,同时生成2a mol NH3
(4)上述反应平衡常数的表达式为K=________。
【答案】增大 增大 2 B ![]()
【解析】
(1)气体浓度越大,化学反应速率越快;
(2)根据浓度对平衡状态的影响分析;根据热化学方程式计算;
(3)可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量、物质的量浓度、百分含量以及由此引起的一系列物理量不变;
(4)化学平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比值。
(1)恒温条件下,缩小容器体积,反应物和生成物浓度都增大,增大单位体积内活化分子个数,化学反应速率增大;
(2)增大氮气浓度,平衡正向移动,消耗的氢气量增多,所以氢气转化率增大;根据方程式知,生成2mol氨气放出92.4kJ热量,则反应达到平衡时放出的热量是92.4kJ,因此生成的NH3为2mol;
(3)A.N2、H2、NH3的浓度相等时,该反应不一定达到平衡状态,与反应物初始浓度及转化率有关,故A错误;
B.反应前后气体的物质的量改变,则反应前后气体压强改变,当容器内压强不再变化时,各物质的物质的量不变,反应达到平衡状态,故B正确;
C.无论反应是否达到平衡状态都存在“单位时间内消耗a mol N2,同时生成2a mol NH3”,所以不能据此判断平衡状态,故C错误;
故答案选B;
(4)根据反应的化学方程式可知化学平衡常数的表达式为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】关于如图中四个图像的说法正确的是


注:图中,E表示能量,p表示压强,t表示时间,V表示体积。
A. ①表示化学反应H2(g)+Cl2(g)===2HCl(g)的能量变化,则该反应的反应热ΔH=+183 kJ/mol
B. ②表示其他条件不变时,反应4A(g)+3B(g)![]() 2C(g)+6D在不同压强下B的体积分数随时间的变化,则D一定是气体
2C(g)+6D在不同压强下B的体积分数随时间的变化,则D一定是气体
C. ③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液
D. ④表示10 mL 0.1 mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.1 mol/L盐酸,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类共同关注的重要问题,甲烷是一种洁净的能源。
(1)甲烷不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)=CO(g)+3H2(g)△H1。已知某些化学键的键能数据如下表:
化学键 | C—H | H—H | C≡O | O—H |
键能/kJ·mol-1 | 413 | 436 | 1076 | 463 |
则△H1=___________kJ·mol-1
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g)△H2,在2L恒容密闭容器中,按物质的量之比1:2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,
CH3OH(g)△H2,在2L恒容密闭容器中,按物质的量之比1:2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,
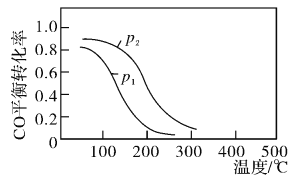
200℃时n(H2)随时间的变化如下表所示
t/min | 0 | 1 | 2 | 3 |
n(H2)/mol | 6.0 | 3.4 | 2.0 | 2.0 |
①△H2___________0(填“>”“<”或“=”)
②下列说法正确的是___________(填字母序号)。
a.达平衡后往容器中充入稀有气体,压强增大,平衡向正反应方向移动
b.降低温度,该反应的平衡常数变大
C.容器内气体密度不变,反应达到最大限度
d.图中压强p1>p2
③200℃时,该反应的平衡常数K=___________。
(3)甲烷、氧气和KOH溶液可组成燃料电池。则此燃料电池工作时,通入甲烷的电极为___________极,其电极反应式为______________________,通入氧气的电极反应式为:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_______。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是________。“滤液”中的溶质主要是_______。“调pH”中发生反应的化学方程式为__________。
(3)KIO3也可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式______。
②电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有______________(写出一点)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表中的W、X、Y、Z均为短周期元素,其原子最外层电子数之和为22。下列说法不正确的是( )
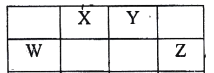
A.以上元素都可以与H元素形成18电子的分子
B.X的氧化物都不是酸性氧化物
C.Y与金属钠形成的化合物可能含有非极性共价键
D.1mol W的单质与足量的Z的单质反应,转移电子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温时CuSO4的水溶液呈____(填“酸”“中”或“碱”)性,原因是(用离子方程式表示_________。
(2)在实验室配制FeCl3溶液时,常将FeCl3固体先溶于较浓的______(填物成名称)中,然后用蒸馏水稀释到所需的浓度,以_________(填“促进”或“抑制”)其水解。
(3)把A1C13溶液蒸干、灼烧,最后得到的主要固体产物是____(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298 K、101kPa时,N2与H2反应过程中能量变化的曲线图,下列叙述错误的是( )
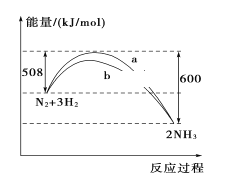
A. 加入催化剂,不能改变该化学反应的反应热
B. b曲线是加入催化剂时的能量变化曲线
C. 该反应的热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92 kJ/mol
2NH3(g) ΔH=-92 kJ/mol
D. 在常温、体积一定的条件下,通入1 mol N2和3 mol H2,反应后放出的热量为92 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的短周期主族元素X、Y、Z、W、R,其中X、Y两种元素的核电荷数之差等于它们的原子最外层电子数之和;Y、Z位于相邻主族;Z是地壳中含量最高的元素;X、W是同主族元素。上述五种元素两两间能形成四种常见的化合物甲、乙、丙、丁,这四种化合物中原子个数比如下表:
甲 | 乙 | 丙 | 丁 | |
化合物中各元素原子个数比 |
|
|
|
|
(1)写出下列元素符号:Y_____________,Z_______________,W_____________,R________________。
(2)写出下列化合物的电子式:乙_______________,丙__________________。
(3)向甲的水溶液中加入丁,有淡黄色沉淀生成,请写出反应的化学方程式:__________________。
(4)甲和乙反应能放出大量的热,同时生成两种无污染的物质,请写出该反应的化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和限度的说法中,正确的是( )
A.铁与硝酸反应时,其他条件一定时,硝酸越浓,反应速率越快
B.在金属钠与足量水反应中,增加水的量能加快反应速率
C.在2SO2+O2![]() 2SO3反应中加入18O2,达到平衡后SO2中不可能含有18O2
2SO3反应中加入18O2,达到平衡后SO2中不可能含有18O2
D.无论是吸热还是放热反应,加热都能加快化学反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com