
�������������ɫ�ͳ����µ�Ksp���±���ʾ��
|
|
Cu(OH)2 |
CuOH |
CuCl |
Cu2O |
|
��ɫ |
��ɫ |
��ɫ |
��ɫ |
ש��ɫ |
|
Ksp(25 ��) |
1��6��10��19 |
1��0��10��14 |
1��2��10��6 |
�� |

ij�о���ѧϰС��Ե��ʳ��ˮ����������̽����
ʵ���װ����ͼ��ʾ����ͨ��Դ����a��b�缫�Ͼ������ݲ�����
��1���������е������ӷ�Ӧ����ʽΪ_________________________________________��
��2��Ϊ��ȷ����Դ���������������в���һ����֮��Ч�������� ������
A���۲����������������ɫ
B����U�ι����˷ֱ�������η�̪��Һ
C����ȼ�ŵ�ľ������U�ιܿ�
D����U�ιܿ���һ��ʪ��ĵ���KI��ֽ
ʵ�����������װ�õ�ʯī������ͭ������ֱ����Դ���е�⣬װ����ͼ��ʾ��

�۲쵽������������ʾ��
�ٿ�ʼ�������������Һ�����µ�ͭ�������䰵��
��5 min��b��������ʼ���ְ�ɫ�������������࣬����a����ɢ��
��10 min�����a���İ�ɫ������ʼ��ɺ�ɫ��
��12 min��b�������İ�ɫ������ʼ��ɻ�ɫ��Ȼ����ɳȻ�ɫ��
��a��һֱ�д������ݲ�����
��ֹͣ��⣬��U�ι�������Һ����һ��ʱ����ϲ���Һ����ɫ��û�г�����ɫ���²����ȫ����ש��ɫ��
��3�� a�������ĵ缫��Ӧ����ʽΪ________________________________________________________��
��4�� ���5 min��b�������ĵ缫��Ӧ����ʽΪ___________________________________________��
��5��12 min��b���������ֵijȻ�ɫ�����ijɷ���������������ԭ����___________________________________________________________________________________��
��1��2Cl����2H2O 2OH����H2����Cl2��
2OH����H2����Cl2��
��2��BD
��3��2H+��2e��= H2�� ����2H2O��2e��=2OH����H2����
��4��Cu��Cl����e��=CuCl��
��5��CuOH��Cu2O ��Ksp(CuOH)<Ksp(CuCl)��CuClת��Ϊ��ɫ��CuOH������CuOH���ȶ��ֽ�����Cu2O�����ԳȻ�ɫ�����ijɷ�ΪCuOH��Cu2O�Ļ���
��������
�����������1�� a��b�缫�Ͼ������ݲ�����˵�����NaCl������H2��Cl2�����������ӷ�Ӧ����ʽΪ2Cl����2H2O 2OH����H2����Cl2��
2OH����H2����Cl2��
��2����U�ι����˷ֱ�������η�̪��Һ��������ɫ��һ�������������ӵ�Դ�ĸ�������һ�������������ӵ�Դ����������U�ιܿ���һ��ʪ��ĵ���KI��ֽ��ʪ��ĵ���KI��ֽ������һ�������������ӵ�Դ������������BD���ԡ�
��ѵ��װ�õ�ʯī������ͭ������ֱ����Դ���е�⡣��5 min��b��������ʼ���ְ�ɫ��������ɫ����ΪCuCl����10 min�����a���İ�ɫ������ʼ��ɺ�ɫ����ɫ����ΪCu2O��12 min��b�������İ�ɫ������ʼ��ɻ�ɫ��Ȼ����ɳȻ�ɫ����ɫ����ΪCuOH��a��һֱ�д������ݲ���������ΪH2����ֹͣ��⣬��U�ι�������Һ����һ��ʱ����ϲ���Һ����ɫ��û�г�����ɫ���²����ȫ��ΪCu2O������a�������ĵ缫��Ӧ����ʽΪ2H+��2e��= H2�� ����2H2O��2e��=2OH����H2���������5 min��b�������ĵ缫��Ӧ����ʽΪCu��Cl����e��=CuCl������ΪKsp(CuOH)<Ksp(CuCl)��CuClת��Ϊ��ɫ��CuOH������CuOH���ȶ��ֽ�����Cu2O�����ԳȻ�ɫ�����ijɷ�ΪCuOH��Cu2O�Ļ�������2 min��b���������ֵijȻ�ɫ�����ijɷ���CuOH��Cu2O��
���㣺ԭ��ء������ۺϿ��顣


 �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| b |
| a-b |
| b |
| a-b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
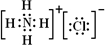
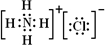
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
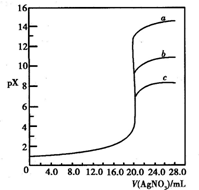 ��0.1mol?L-1?AgNO3��Һ�ֱ�ζ�20.00mL��Cl-��Br-��I-Ũ�Ⱦ�Ϊ0.1mol?L-1����Һ���Ե����AgNO3��Һ�����Ϊ�����꣬pXΪ������[pX=-lg c��X����X=Cl-��Br-��I-]���ɵ���ͼ��ʾ�ĵζ����ߣ���֪25��ʱ�����������ε�Ksp����ɫ�����ʾ�� ��0.1mol?L-1?AgNO3��Һ�ֱ�ζ�20.00mL��Cl-��Br-��I-Ũ�Ⱦ�Ϊ0.1mol?L-1����Һ���Ե����AgNO3��Һ�����Ϊ�����꣬pXΪ������[pX=-lg c��X����X=Cl-��Br-��I-]���ɵ���ͼ��ʾ�ĵζ����ߣ���֪25��ʱ�����������ε�Ksp����ɫ�����ʾ��
|
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com