
����Ŀ�����Ȼ����Ǻϳɲ���������Ҫԭ�ϡ�
��1�����ù�ҵFeCl3��ȡ�����IJ���������[Fe2(C2O4)3��5H2O]��ʵ����������ͼ��ʾ��
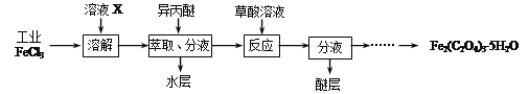
��Ϊ����FeCl3ˮ�⣬��ҺXΪ ��
������������FeCl3�ܱ��������ȡ����ԭ���� ��������ȡ����Һ������ˮ�����Ƿ���Fe3���ķ����� ��
������Fe2(C2O4)3��5H2O���ñ�ˮϴ�ӣ���Ŀ���� ��
��Ϊ�ⶨ���ò���������Ĵ��ȣ�ʵ���ҳ�ȡa g��Ʒ���������ữ����KMnO4����Һ�ζ����ɵ�H2C2O4��KMnO4����ҺӦ������ͼ��ʾ���� ���������������������С�������������ʵ����Fe2(C2O4)3��5H2O����ƫ�͵��� ��

a��ʢ��KMnO4�ĵζ���ˮϴ��δ�ñ�Һ��ϴ
b���ζ��ܵζ�ǰ���첿�������ݣ��ζ�����ʧ
c���ζ�ǰ���Ӷ������ζ����Ӷ���
��2��ij�о���ѧϰС������ʴ�̶�ͭ��·�����÷�Һ������ΪFeCl2��CuCl2��FeCl3���������Ʊ�����ͭ����ˮFeCl3������FeCl3�ϳ�Fe2(C2O4)3��5H2O���벹��������ʴ�̷�Һ�Ʊ�����ͭ����ˮFeCl3��ʵ�鲽�裨��ѡ�õ��Լ������ۡ����ᡢNaOH��Һ��H2O2��Һ�������Һ�м����������ۣ���ַ�Ӧ����ˣ�__________��___________��������ҺpH������Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�Ӹ����FeCl3��6H2O�� ___________���õ���ˮFeCl3��
���𰸡���1������Ũ�����
��FeCl3��������е��ܽ�ȴ�������ˮ�е��ܽ�ȣ�ȡ������Һ�������еμ�����KSCN��Һ������Һ��죬����Fe3+��
����ȥ���ʡ����ٲ�����������ܽ���ģ����ף�c��
��2���������м�������HCl����ַ�Ӧ����ˡ�ϴ�ӡ������ͭ�ۣ������ι���������Һ�ϲ��������м�������H2O2��Һ��Fe2+ȫ������Fe3+����FeCl3��6H2O��HCl�������м�����ˮ��
��������
�����������1�����Ȼ���ˮ������������������ᣬ����Ϊ�������Ȼ���ˮ�⣬Ҫ����Һ�м����ᣬΪ�˲������µ��������ӣ��ữFeCl3 �������ữ�����������ʣ������������ӵ�ˮ�⣻����ȡ�������������������ܵ��ܼ��е��ܽ�Ȳ��������ȡ���ʵ�һ�ַ���������ȡ˵��FeCl3 ��������е��ܽ�ȴ�������ˮ�е��ܽ�ȣ�����Fe3+ ��KSCN��Һ����Һ��ΪѪ��ɫ��������ȡ������Һ�������еμ�����KSCN��Һ������Һ��죬����Fe3+ ����ϴ���dz�ȥ�����������ʣ���ˮ�����¶Ƚ��ͣ����ʵ��ܽ�ȼ�С����˿������ٳ����ܽ���ʧ����KMnO4 ����Һ����ǿ�����ԣ�����ʴ�ܣ����Ӧ������ʽ�ζ�������Ӧ��ʹ�ü���a��û����ϴ���¸������Ũ�ȵ���������࣬ʹ�ⶨ��Fe2(C2O4)3��5H2O����ƫ���������� b������ʹ�����������࣬���²ⶨ��Fe2(C2O4)3��5H2O����ƫ�ߣ����� c���������ƫС�����²ⶨ��Fe2(C2O4)3��5H2O����ƫ�ͣ���ȷ����2����ʴ�̷�Һ�Ʊ�����ͭ����ˮFeCl3��ʵ�鲽�������Һ�м����������ۣ�������Ӧ��Fe+ 2FeCl3=3FeCl2��Fe+CuCl2=FeCl2+Cu����ַ�Ӧ����ˣ����ܷ�Ӧͭ��ʣ�����Ļ�������������ȥͭ�е�����Fe�����ᷴӦ����FeCl2����������Cu���ܷ�Ӧ�����ѷ�Ӧ��Һ��ǰ�κϲ��������м�������H2 O2 ��Һֱ������Һ��Fe2+ ȫ������Fe3+ ��������ҺpH������Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�Ӹ����FeCl3��6H2O����ֱ�Ӽ���FeCl3 6H2 O��ˮ�������ܵõ���ˮFeCl3��Ϊ����ˮ������HCl��Χ�½������ȣ����ɵõ���ˮFeCl3��


 �ο�������ϵ�д�
�ο�������ϵ�д� ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и�������һ������ָ����Һ�д����������
A. pH=l ����Һ�У�Ba2+��Fe3+ ��Cl-��SCN-
B. ��ʹ��̪������Һ��Ca2+��K+��HCO3-��CO32-
C.  =10-12����Һ�У�NH4+��Cu2+��NO3-��SO42-
=10-12����Һ�У�NH4+��Cu2+��NO3-��SO42-
D. ��ˮ�����c(H+)=10-12mol��L-1����Һ�У�Na+��Al3+��Cl-��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A. ǿ����ʶ�������ˮ������BaSO4���������
B. ������ˮ��Һ���Ե��磬���������ڷǵ����
C. ʹ�ô��������ò��Է��Ļ�ѧ��Ӧ�Է�����
D. �������Һ�ĵ���������������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����þ��Ͷ�뵽ʢ������ij������������H2�����ʿ�����ͼ��ʾ�������������У��������Ũ�ȣ���þ���ı����������Һ���¶ȣ���Cl-��Ũ����Ӱ�췴Ӧ���ʵ�������

A�� �٢� B�� �ۢ� C�� �٢ڢ� D�� �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ƿ�������������ʵ���Ũ�ȵ���Һ�Ķ������������ϱ��У����¶ȡ���Ũ�ȡ�����������ѹǿ�����̶����������еģ� ��
A. �ڢ� B. �ۢ� C. �٢ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ײ��ϡ���ָ����ֱ���ڼ�������ʮ���IJ��ϣ��罫�����ײ��ϡ���ɢ��Һ���ɢ���У����÷�ɢϵ���й�˵����ȷ���ǣ� ��
A.�Ǵ�����
B.��������һ��Ϊ����Һ������Һ
C.��ͨ�����˵ķ����õ����ײ���
D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ȫ�����ڴ��������( )
A. �������֡��ơ��� B. ���������ȷ¡��Ҵ���
C. �������͡���ˮ�ƾ� D. ���͡������ᡢú
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ������ȥ��Ӧ����
A. �Ҵ���Ũ���Ṳ�ȵ�140�� B. �Ҵ��������ᣨHBr����Ӧ
C. �Ҵ���������Ӧ������ȩ D. �Ҵ���Ũ���Ṳ����170��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl3 ���о�ˮ���ã�����ʴ�豸�����ۺ��Ȼ�����һ�����͵���������������ˮ��FeCl3 ��Ч���Ҹ�ʴ��С��(��֪25����Ksp[Fe(OH)3]=4.0��10��38��lg2=0.3)
��ش��������⣺
(1)FeCl3��ˮ��ԭ���� ��(�����ӷ���ʽ��ʾ)��Fe3��ˮ�����ɵ�Fe(OH)3��������������ˮ�е��������ʣ������´˷�Ӧ��ƽ�ⳣ��Ϊ (��д��ֵ)��
(2)��FeCl3 ��Һ��NaHCO3 ��Һ��ϣ������ӷ���ʽΪ ��
(3)25��ʱpH=3����Һ�У�c(Fe3��)= molL��1��
(4)FeCl3 ����Һ�з�����ˮ�⣺
Fe3����H2O![]() Fe(OH)2����H�� K1
Fe(OH)2����H�� K1
Fe(OH)2����H2O![]() Fe(OH)2����H�� K2
Fe(OH)2����H�� K2
Fe(OH)����H2O![]() Fe(OH)3��H�� K3
Fe(OH)3��H�� K3
����ˮ�ⷴӦ��ƽ�ⳣ��K1��K2��K3�ɴ�С��˳���� ��
ͨ����������������ˮ�����ۺϣ����ɾۺ������������ӷ���ʽΪ��xFe3����yH2O![]() Fex��yH������ʹƽ�������ƶ��ɲ��õķ�����(�����) ��
Fex��yH������ʹƽ�������ƶ��ɲ��õķ�����(�����) ��
a.���� b.��ˮϡ�� c.����NH4Cl d.����NaHCO3
(5) FeCl3��Һ�ɸ�ʴӡˢ��·�壬�䷴ӦΪCu ��2FeCl3 =CuCl2��2FeCl2 Ҫ���˷�Ӧ�����ԭ����н��У���������ӦʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com