
【题目】在反应KClO3+6HCl(浓)===3Cl2↑+KCl+3H2O中,被还原的氯原子和被氧化的氯原子的个数之比为
A.1:6 B.5:1 C.1:5 D.6:1
科目:高中化学 来源: 题型:
【题目】(Ⅰ)在下列化合物中:H2O 、Na2O 、I2 、NaCl、KOH、CO2、NH4Cl、Na2O2,请填空:
(1)只由非金属组成的离子化合物是________________,
(2)含有极性共价键的离子化合物是________________,
(3)只含有非极性共价键的是______________________,
(4)既有离子键又有非极性键的化合物是___________________。
(Ⅱ)有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如右图所示。E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同。

请回答下列问题:
(1)写出B元素的原子结构示意图_______________________;
(2)A与氢元素能形成原子物质的量之比为1:1的化合物,其电子式为______________;
(3)向D与E形成的化合物的水溶液中滴入NaOH溶液直至过量,观察到的现象是:_______________,最后阶段反应的离子方程式为___________________;
(4)B、C、D、E的最高价氧化物的水化物的酸性从强到弱的顺序为(物质用化学式表示):___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是( )
A. 对2HI(g)![]() H2(g)+I2(g)平衡体系增加压强使颜色变深
H2(g)+I2(g)平衡体系增加压强使颜色变深
B. 反应CO(g)+NO2(g)![]() CO2(g)+NO(g)△H<0升高温度使平衡向逆方向移动[
CO2(g)+NO(g)△H<0升高温度使平衡向逆方向移动[
C. 合成氨反应:N2(g)+3H2(g)![]() 2NH3(g)△H<0,为使氨的产率提高,理论上应采取低温高压的措施
2NH3(g)△H<0,为使氨的产率提高,理论上应采取低温高压的措施
D. 在溴水中存在如下平衡:Br2(g)+H2O(l)![]() HBr(aq)+HBrO(aq),当加入NaOH溶液后颜色变浅]
HBr(aq)+HBrO(aq),当加入NaOH溶液后颜色变浅]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水溶液一定呈中性的是
A.c(NH4+)=c(C1-)的NH4Cl 溶液
B.c(H+)=1×10-7mol·L-1的溶液
C.pH=7的溶液
D.室温下将pH=3的酸与pH= 11的碱等体积混合后的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程没有发生化学反应的是
A. 用消毒液杀灭游泳池中的藻类 B. 用CaCl2融化路面的积雪
C. 用石灰修复被酸雨侵蚀的土壤 D. 用醋酸浸泡热水壶以除去水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示,下列叙述不正确的是( )
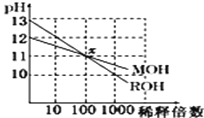
A. MOH是一种弱碱
B. 在x点,c(M+)=c(R+)
C. 稀释前,c(ROH)="10" c(MOH)
D. 稀释前MOH溶液和ROH溶液中由水电离出的c(OH﹣)后者是前者的 10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷和其化合物在科研及生产中均有着重要的作用。
(1)红磷P(s)和Cl2(g)发生反应生成PCl3(g)PCl5(g),反应过程如下:
2P(s) + 3Cl2(g) = 2PCl3(g) △H=-612kJ/mol
2P(s) + 5Cl2(g) = 2PCl5(g) △H=-798kJ/mol
气态 PCl5生成气态PCl3和Cl2的热化学方程式为________。
(2)一定温度下,在三个恒容体积均为2.0L的容器中发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
编号 | 温度(℃) | 起始/mol | 平衡/mol | 达到平衡所需时间/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
I | 320 | 0.40 | 0.10 | 0.10 | t1 |
II | 320 | 0.80 | t2 | ||
III | 410 | 0.40 | 0.15 | 0.15 | t3 |
①平衡常数K:溶液II____溶液III(填“>”或“=”或“<”)
②反应达到平衡时,PCl3的转化率:容器II_____容器I(填“>”或“=”或“<”)
(3)亚磷酸(H2PO5)与足量的NaOH溶液反应生成Na2HPO3。电解Na2HPO3溶液也可得到亚鱗酸,装置示意图如图:

阴极的电极反应式为_______;产品室中反应的离子方程式为__________。
(4)一定温度下,Ksp[Mg3(PO4)2]=6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26向浓度均为0.20 mol·L-1的MgCl2和CaCl2混合溶液中逐滴加入Na3PO3,先生成________沉淀(填化学式);当测得溶液其中一种金属阳离子沉淀完全(浓度小于105mol/L)时,溶液中的另一种金属阳离子的物质的量浓度c= ______mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是中学化学常见物质,A、D为单质,G是含A元素的酸性气体。已知:A(s)+B(g)=C(g)+D(g) ΔH= +131.4 kJmol-1,某同学实验测知,4 g A发生上述反应吸收43.8 kJ的热量。
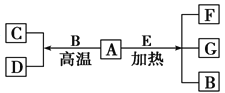
(1)写出A元素的名称________。
(2)另外知:
A(s)+O2(g)=G(g)ΔH= -393.6 kJmol-1
C(g)+ O2(g)=G(g)ΔH=-283 kJmol-1
D(g)+ O2(g)=B(g)ΔH=-242 kJmol-1由此判断“因为283 kJmol-1+242 kJmol-1>393.6 kJmol-1,所以A燃烧时加少量B可以放出更多的热量”这种说法是否正确?___________,理由是_____________________;
(3)写出A+O2→C的热化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电负性的大小也可以作为判断金属性和非金属性强弱的尺度,下列关于电负性的变化规律正确的是
A. 周期表中同周期元素从左到右,元素的电负性逐渐增大
B. 周期表中同主族元素从上到下,元素的电负性逐渐增大
C. 电负性越大,金属性越强
D. 电负性越小,非金属性越强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com