
����Ŀ����ͼ��һ���绯ѧ���̵�ʾ��ͼ���밴Ҫ����գ�
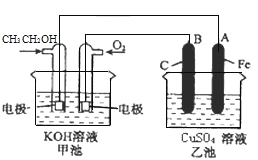
(1)ͨ��CH3CH2OH�ĵ缫������______________��B�缫��������_____________��
(2)ͨ��CH3CH2OHһ���ĵ缫��ӦʽΪ_____________________________________��
(3)�ҳ����ܷ�Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
(4)���ҳ���A(Fe)������������12.8gʱ���׳�������O2 _______ mL(�����)
(5)�������ʱ������(N2H4)Ϊȼ�ϣ��Զ������������������������Ӧ���ɵ�����ˮ������
��д���ڼ��������¸�����ӦʽΪ��___________________________________________��
����֪��N2(g)��2O2(g)=2NO2(g)����H����67.7 kJ��mol��1��N2H4(g)��O2(g)=N2(g)��2H2O(g)����H����534 kJ��mol��1����N2H4��NO2��Ӧ���Ȼ�ѧ����ʽ__________________________________________��
���𰸡����� ���� C2H5OH-12e-+16OH-=2CO![]() +11H2O 2CuSO4+2H2O
+11H2O 2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4 2240 N2H4-4e-+ 4OH��=N2+4H2O 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)��H=-1135.7kJmol-1
2Cu+O2��+2H2SO4 2240 N2H4-4e-+ 4OH��=N2+4H2O 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)��H=-1135.7kJmol-1
��������
�׳�Ϊ�Ҵ�ȼ�ϵ�أ��ŵ�������Ҵ������������������ڵ������Һ�Լ��ԣ���������CO![]() ��ˮ����������ԭ�����������Ե������Һ������OH�����ҳ�Ϊ����װ�ã�B�缫��ԭ�����������Ϊ������ʧ���ӷ���������Ӧ��A�缫��ԭ��ظ�������Ϊ�������õ��ӷ�����ԭ��Ӧ��
��ˮ����������ԭ�����������Ե������Һ������OH�����ҳ�Ϊ����װ�ã�B�缫��ԭ�����������Ϊ������ʧ���ӷ���������Ӧ��A�缫��ԭ��ظ�������Ϊ�������õ��ӷ�����ԭ��Ӧ��
(1)ͨ���Ҵ��ĵ缫ʧ���ӷ���������Ӧ��Ϊԭ��صĸ�����B�缫��ԭ�����������Ϊ������
(2)�Ҵ������������������ڵ������Һ�Լ��ԣ���������CO![]() ��ˮ���缫����ʽΪC2H5OH-12e-+16OH��=2CO
��ˮ���缫����ʽΪC2H5OH-12e-+16OH��=2CO![]() +11H2O��
+11H2O��
(3)�ҳ���������ˮ��������������ŵ�����������ͬʱ���������ӣ�������ͭ���ӷŵ�����ͭ���ʣ����Ե���ܷ�Ӧ�Ļ�ѧ����ʽΪ2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4��
2Cu+O2��+2H2SO4��
(4)�ҳ���A�缫Ϊ�������缫��ӦΪCu2++2e-=Cu������ͭ�����ʵ���Ϊ![]() =0.2mol������ת�Ƶĵ���Ϊ0.4mol���׳���ͨ��������һ���ĵ缫��ӦΪO2+2H2O+4e-=4OH��������ת��0.4mol����ʱ����0.1mol��������������Ϊ0.1mol��22.4L/mol=2.24L=2240mL��
=0.2mol������ת�Ƶĵ���Ϊ0.4mol���׳���ͨ��������һ���ĵ缫��ӦΪO2+2H2O+4e-=4OH��������ת��0.4mol����ʱ����0.1mol��������������Ϊ0.1mol��22.4L/mol=2.24L=2240mL��
(5)��ԭ����и���ʧ���ӷ���������Ӧ���õ����N2H4��NO2����������N2H4Ϊ����ԭ�ϣ��������Һ�Լ��ԣ����Ե缫����ʽΪN2H4-4e-+ 4OH��=N2+4H2O��
����֪i��N2(g)+2O2(g)=2NO2(g)����H=+67.7kJmol-1��
ii��N2H4(g)+O2(g)=N2(g)+2H2O(g)����H=-534kJmol-1
���ݸ�˹���ɣ�2����-�ٿɵ�2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ��H=2(-534kJmol-1)-(+67.7kJmol-1)=-1135.7kJmol-1��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���������
A. �����̻������ȼ�������ڱ�������
B. ���Ȼ�̼�ͱ�������ˮ�е����ȡ��
C. ���ۡ������ʾ���ˮ�⣬��ˮ�����ղ����Ϊ������
D. �ȼҵ����Cl2��NaOH��Һ��ʹ�õ��������ӽ���Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС����ʵ�������Ҵ���Ũ������廯�ƺ�ˮ��Ϸ�Ӧ���Ʊ������飬��̽������������ʡ��й����ݼ��±���
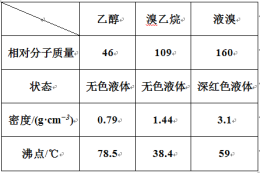
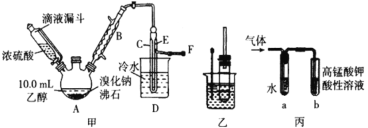
I. ��������Ʊ�
��Ӧԭ�����£�ʵ��װ������ͼ������װ�á��г�װ�þ�ʡ�ԣ���
H2SO4+NaBr ![]() NaHSO4+HBr�� CH3CH2OH+HBr
NaHSO4+HBr�� CH3CH2OH+HBr ![]() CH3CH2Br+H2O
CH3CH2Br+H2O
��1�� ͼ����A ����������_____��ͼ��B �����ܵ�����Ϊ_____��
��2�� ��ͼ����A �����¶ȹ���Ũ�����Ũ�ȹ�����ʹ C ���ռ����Ĵֲ�Ʒ�ʳ�ɫ��ԭ����A �з����˸���Ӧ������_____��F ���ӵ���ͨ��ϡNaOH ��Һ�У���Ŀ����Ҫ������_____��β����ֹ��Ⱦ����
II. ���������ʵ�̽��
����ͼʵ��װ����֤����������ʣ�
��3�� �������Թ��ڼ��� 10mL6mol��L ��1NaOH ��Һ�� 2mL �����飬�����ã�Һ��ֲ㣬ˮԡ���ȡ��ù����еĻ�ѧ����ʽΪ_______��
��4�� ���������Թ���� NaOH ��Һ����NaOH �Ҵ���Һ��Ϊ֤������Ϊ��ϩ�������ɵ�����ͨ����ͼ��װ�á�a �Թ��е�ˮ��������_______������ a �Թܣ������ɵ�����ֱ��ͨ�� b �Թ��У��� b�е��Լ�����Ϊ _____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ƾ�����ǿɰ���ִ���������Լ�ʻԱ���ƵĶ��٣��乤��ԭ��ʾ��ͼ��ͼ��ʾ����Ӧԭ��Ϊ��CH3CH2OH+O2=CH3COOH+H2O�������ߺ��������������ľƾ������͵�����з�Ӧ����С�������õ��������ӷŴ����Ŵ����Һ����ʾ������ʾ��ƾ�����������˵����ȷ����

A. bΪ�������缫��ӦʽΪ��O2+4H++4e-=2H2O
B. �������Һ�е�H+����a�缫
C. ����0.4mol����ת�ƣ����ڱ�״��������4.48L����
D. ���������оƾ�����Խ�ߣ���������ͨ���ĵ���ԽС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ŵ������ѧ�������ʩ�˵��˷��ֽ�����Ŀ��������������Ϊ�dz���Ч��ϩ�����ֽ������������ҵ��ұ����Ļ�ѧ��Ӧ����Ϊ��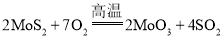 ����
����![]() ����
����![]() ����
����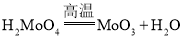 �����û�ԭ����
�����û�ԭ����![]() ��ԭ�ɽ����⡣����˵����ȷ���ǣ� ��
��ԭ�ɽ����⡣����˵����ȷ���ǣ� ��
A.![]() ���ղ�����β����ֱ���ŷ�
���ղ�����β����ֱ���ŷ�
B.![]() �ǽ��������Ҳ�Ǽ���������
�ǽ��������Ҳ�Ǽ���������
C.![]() ��һ��ǿ��
��һ��ǿ��
D.����![]() ��
��![]() ��
��![]() �ֱ�ԭ������
�ֱ�ԭ������![]() �������Ļ�ԭ�������ʵ���֮��Ϊ
�������Ļ�ԭ�������ʵ���֮��Ϊ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ӵ��㾫�Ķ����D�Լ���������ȫ�����в�ĸ߷��ӻ�����PVB�ĺϳ�·�����£�
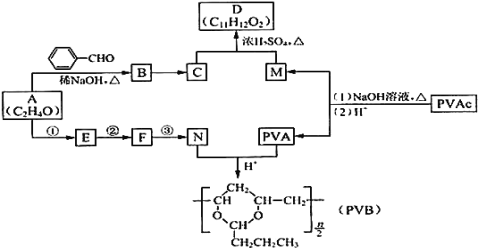
��֪����.RCHO+R��CH2CHO![]()
![]() +H2O(R��R����ʾ��������)
+H2O(R��R����ʾ��������)
��.ȩ���Ԫ��![]() �磺�Ҷ���
�磺�Ҷ���![]() �����ɻ�״��ȩ��RCHO+HOCH2CH2OH
�����ɻ�״��ȩ��RCHO+HOCH2CH2OH![]()
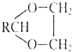 +H2O
+H2O
��A�ĺ˴Ź������������ַ壮A�������� ______
�����й���B��˵����ȷ���� ______
a.����ʽΪC9H8O b.����ԭ�Ӿ�����ͬһƽ����
c.��������5molH2������Ӧ d.����ʹ��ˮ��ɫ
��CΪ��ʽ�ṹ����B��ԭ�õ���C�Ľṹ��ʽ�� ______
��G��D������ͬ�Ĺ����ţ���Է�������DС28����G�Ľṹ�� ______ ��![]() �����������칹
�����������칹![]()
��E��ʹBr2��CCl4��Һ��ɫ��N��A����Ӧ���ۺϳɡ�
a.�ڵķ�Ӧ������ ______
b.�۵Ļ�ѧ����ʽ�� ______
��PVAc��һ�ֵ��徭�Ӿ۷�Ӧ�õ����õ���Ľṹ��ʽ�� ______
�˼��������£�PVAc��ȫˮ��Ļ�ѧ����ʽ�� ______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.100mol/L��NaOH��Һ�ֱ�ζ�20.00mL0.100mol/L�������0.100mol/L�Ĵ��ᣬ�õ������ζ����ߣ���ͼ��ʾ��
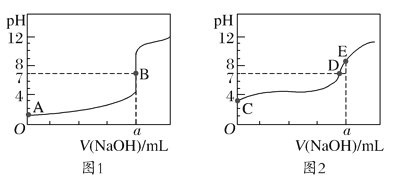
����˵����ȷ����( )
A.�ζ������������ͼ2
B.���εζ�����ѡ����Ȼ��̪��ָʾ��
C.�ﵽB��E��ʱ����Ӧ���ĵ�n(CH3COOH)=n(HCl)
D.��HA��ʾ�ᣬ��0mL<V(NaOH)<20.00mLʱ��ͼ2��Ӧ���Һ�и�����Ũ���ɴ�С��˳��һ����c(A-)>c(Na+)>c(H+)>c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɡ�
��һ��ҽҩ�м��壬�������Ʊ�����Ѫҩ����ͨ������·�ߺϳɡ�
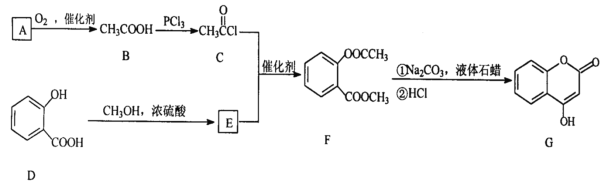
��ش��������⣺
(1)A��������Һ��Ӧ���������ɣ���A�Ľṹ��ʽ��__________________
(2)B��C�ķ�Ӧ������______________
(3)д��F����NaOH��Һ����ʱ��Ӧ�Ļ�ѧ����_______________________________
(4)���й���G��˵����ȷ����______________
a.�����嵥�ʷ�Ӧ
b.��������Ʒ�Ӧ
c.1molG����ܺ�3mol������Ӧ
d.����ʽ��C9H7O3
(5)��D��Ϊͬ���칹���Һ��з��ǻ�����������_____________��
(6)������ѧ֪ʶ�ͻ�ȡ����Ϣ��д����CH3COOH,![]() Ϊԭ�Ϻϳ���Ҫ�Ļ�����Ʒ
Ϊԭ�Ϻϳ���Ҫ�Ļ�����Ʒ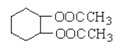 ��·������ͼ__________________________(���Լ���ѡ)�ϳ�·������ͼʾ�����£�CH3CH2OH
��·������ͼ__________________________(���Լ���ѡ)�ϳ�·������ͼʾ�����£�CH3CH2OH![]() CH2=CH2
CH2=CH2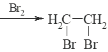
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��������������Z��Һ�й�����ͼ��װ�ã�ʵ���е�����ָ�뷢��ƫת��ͬʱX����֣�Y����ϸ����X��Y��Z������( )
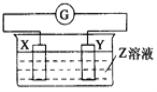
ѡ�� | X | Y | Z |
A | Zn | Cu | ϡ���� |
B | Cu | Zn | ϡ���� |
C | Cu | Ag | ����ͭ��Һ |
D | Ag | Zn | ��������Һ |
A.AB. BC. CD. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com