
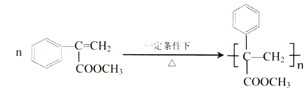
【题目】下图是以芳香烃A为原料合成有机高分子化合物甲和乙的路线图。
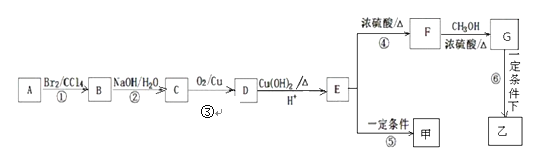
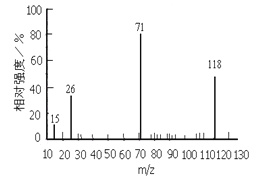
已知:①下图是A通过检测所得的质谱图,A分子中有5种不同化学环境的氢原子,它们的个数比为1:2:2:2:3;②甲乙均为有机高分子化合物;③A的分子结构中苯环上只有一个取代基。
请根据信息,回答下列问题:
(1)A的化学式为______;
(2)C中所含官能团的名称是_____;
(3)反应④的反应类型为_____;
(4)甲的结构简式为______;
(5)写出有关反应的化学方程式:③的反应方程式__________,⑥的反应方程式__________;
(6)含有苯环、与F具体相同官能团的F的同分异构体有____种(不考虑立体异构、不含F),其中核磁共振氢谱为5组峰,面积比为2:2:2:1:1的为_____(写结构简式)。
【答案】C9H10 羟基 消去反应 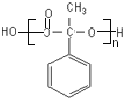
 4
4 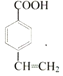
【解析】
试题 (1)通过质谱图测得芳香烃A的相对分子质量是118;A的分子结构中苯环上只有一个取代基;A分子中有5种不同化学环境的氢原子,它们的个数比为1:2:2:2:3;A的结构只能是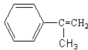 ,A与Br2的CCl4溶液反应生成B,则B是
,A与Br2的CCl4溶液反应生成B,则B是 ;氯代物在氢氧化钠的水溶液中发生水解反应生成C,则C是
;氯代物在氢氧化钠的水溶液中发生水解反应生成C,则C是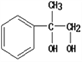 ;醇在铜作催化剂的条件下与氧气发生氧化反应生成醛D,则D是
;醇在铜作催化剂的条件下与氧气发生氧化反应生成醛D,则D是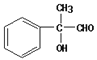 ;醛被新制氢氧化铜悬浊液氧化为酸E,则E是
;醛被新制氢氧化铜悬浊液氧化为酸E,则E是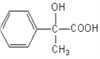 ;
; 在浓硫酸作用下可发生消去反应生成F,则F是
在浓硫酸作用下可发生消去反应生成F,则F是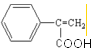 ;F在浓硫酸作用下与甲醇发生酯化反应生成酯G,G是
;F在浓硫酸作用下与甲醇发生酯化反应生成酯G,G是![]() ;G在一定条件下发生加聚反应生成高聚物乙,则乙是
;G在一定条件下发生加聚反应生成高聚物乙,则乙是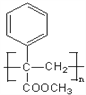 ;化合物
;化合物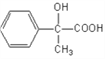 含有羟基、羧基,可以发生缩聚反应生成甲,则甲是
含有羟基、羧基,可以发生缩聚反应生成甲,则甲是 。
。
解析:根据以上分析,(1)A的结构式是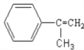 ,化学式为C9H10;
,化学式为C9H10;
(2)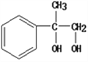 中所含官能团的名称是羟基;
中所含官能团的名称是羟基;
(3)反应④是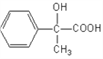 在浓硫酸作用下生成
在浓硫酸作用下生成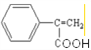 ,反应类型为消去反应;
,反应类型为消去反应;
(4)甲是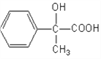 在一定条件下发生缩聚反应的产物,甲是的结构简式为
在一定条件下发生缩聚反应的产物,甲是的结构简式为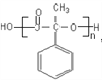 ;
;
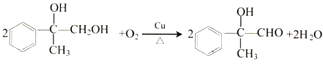
(5)反应③是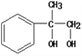 在铜作催化剂的条件下与氧气发生氧化反应生成
在铜作催化剂的条件下与氧气发生氧化反应生成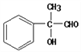 ,反应方程式img src="http://thumb.zyjl.cn/questionBank/Upload/2019/05/01/08/8c46d943/SYS201905010832494221135440_DA/SYS201905010832494221135440_DA.024.png" width="343" height="59" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />;
,反应方程式img src="http://thumb.zyjl.cn/questionBank/Upload/2019/05/01/08/8c46d943/SYS201905010832494221135440_DA/SYS201905010832494221135440_DA.024.png" width="343" height="59" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />;
反应⑥是![]() 在一定条件下发生加聚反应,反应方程式是
在一定条件下发生加聚反应,反应方程式是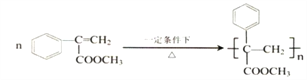 ;
;
(6)含有苯环、与F具体相同官能团的F的同分异构体,若存在![]() 和
和![]() 有邻间对三种结构;若存在
有邻间对三种结构;若存在![]() 只有一种结构,所以共有4种同分异构体,其中核磁共振氢谱为5组峰,面积比为2:2:2:1:1的为
只有一种结构,所以共有4种同分异构体,其中核磁共振氢谱为5组峰,面积比为2:2:2:1:1的为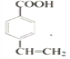 。
。


科目:高中化学 来源: 题型:
【题目】“结晶玫瑰”具有强烈的玫瑰香气,是一种很好的定香剂,其化学名称为“乙酸三氯甲基苯甲酯”,通常以三氯甲基苯基甲醇和醋酸酐为原料制备:
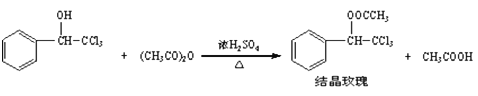
已知:

操作步骤如下:
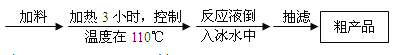
请根据以上信息,回答下列问题:
(1)加料时,应先加入三氯甲基苯基甲醇和酷酸酐,然后慢慢加入浓硫酸并______,待混合均匀后,最适宜的加热方式为______(填“水浴加热”或“油浴加热”)。
(2)粗产品的成分是结晶攻瑰与少量_______(填名称)的混合物,设计了如下方案进行提纯和检验。请完成表中内容:
序号 | 实验方案 | 实验现象 | 结论 |
① | 将粗产品溶解在中,按粗产品、溶剂的质量比为1:__混合,用水浴加热到70℃回流溶剂使粗产品充分溶解 | 得到无色溶液 | |
② | 将步骤1所得溶液____________抽滤 | 得到白色晶体 | |
③ | 干燥步骤2所得白色晶体,____________ | _____________ | 白色晶体是结晶玫瑰 |
(3)4.51g三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰4.68g,则产率是________(小数点后保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于下图所示电化学装置的分析正确的是

A. 若X为直流电源,Y为铜棒接正极,则Fe棒上镀铜
B. 若X为直流电源,Y为碳棒接负极,则Fe棒被保护
C. 若X为电流计,Y为锌棒,则SO42-移向Fe棒
D. 若X为导线,Y为铜棒,则Fe棒发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的用途说法不正确的是
A.碳酸氢钠可被用于治疗胃酸过多B.Cl2可被用于工业制漂粉精
C.明矾可用于自来水的杀菌消毒D.Fe2O3俗称铁红,常用作红色涂料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二氯化二硫(S2Cl2)是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为193K,沸点为411K,遇水水解产生的气体能使品红褪色。下列有关说法正确的是
A. S2Cl2晶体中存在离子键
B. S2Cl2在熔融状态下能导电
C. S2Cl2分子中各原子均达到8电子稳定结构
D. S2Cl2与水反应后生成的气体难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为研究电化学原理,设计如图装置。请回答下列问题:
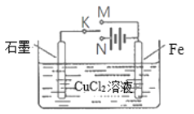
(1)若K与M、N均断开,发生的离子反应为____________________。
(2)若K与M相连、与N断开,石墨为_________(填电极名称)。
(3)若K与N相连、与M断开,石墨电极处的现象为____________________。
(4)若将CuCl2溶液换成精制饱和食盐水,仍保持K与N相连、与M断开,此时装置中发生的离子反应方程式为_______________________________。若此反应过程中转移1mol电子,理论上共产生标准状况下气体__________________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组测定某Fe2(SO4)3样品(只含少量FeCl2杂质)中铁元素的质量分数,按以下实验步骤进行操作:
①称取a g样品,置于烧杯中;
②加入50 mL 1.0 mol/L稀硫酸和一定量的蒸馏水,使样品溶解,然后准确配制成250.0 mL溶液;
③量取25.0 mL步骤②中配得的溶液,置于烧杯中,加入适量氯水,使反应完全;
④加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤,洗涤沉淀;将沉淀转移到某容器内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;
⑥……
请根据上面叙述,回答:
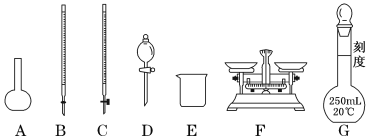
(1)上图所示仪器中,步骤①②③中必须用到的仪器有E和___________(填字母)。
(2)步骤②中:配制50 mL 1.0 mol/L稀H2SO4,需要用量筒量取98%(密度1.84 g/cm3)的浓H2SO4体积为________ mL。
(3)样品中的杂质Fe2+有较强的还原性,完成并配平下列反应的离子方程式
____Fe2++ ClO2+ === Fe3++ Cl-+ H2O
从理论上分析,上述实验中若将氯水改为ClO2时,对实验结果的影响是__________(填“偏大”“偏小”或“不影响”),等物质的量ClO2与Cl2的氧化效率之比为__________。
(4)若步骤⑤不在干燥器中冷却,则测定的铁元素的质量分数会________(填“偏大”“偏小”或“不影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的说法正确的是( )
A. 钠是银白色金属、密度比水略大 B. 钠着火时,可用水灭火
C. 金属钠在空气中燃烧,生成氧化钠 D. 通常情况下,钠的熔点略低于水的沸点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com