
【题目】下列物质的转化在给定条件下能实现的是( )
A.NaCl(aq)![]() NaHCO3(s)
NaHCO3(s) ![]() Na2CO3(s)
Na2CO3(s)
B.CuCl2![]() Cu(OH)2
Cu(OH)2![]() Cu
Cu
C.Al ![]() NaAlO2(aq)
NaAlO2(aq) ![]() NaAlO2(s)
NaAlO2(s)
D.MgO(s)![]() Mg(NO3)2(aq)
Mg(NO3)2(aq) ![]() Mg(s)
Mg(s)
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】右图是a、b两种固体物质的溶解度曲线。下列说法中正确的是
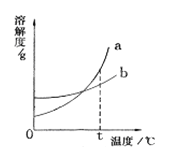
A. a物质的溶解度受温度变化的影响较小,b物质的溶解度受温度变化的影响较大。
B. t℃时,等质量的a、b饱和溶液中含有相同质量的溶质
C. 当温度大于t℃时,a溶液一定比b溶液浓
D. a中含有少量b时,用冷却热饱和溶液的方法提纯a。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用离子方程式OH+H+ = H2O表示的反应是
A.稀盐酸和稀氨水反应
B.稀硫酸和烧碱溶液反应
C.稀硫酸和氢氧化铜反应
D.稀硫酸和氢氧化钡溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的酸性溶液中,能共存的离子组是( )
A. Na+ 、K+、SO42-、HCO3 B. Cu2+、K+、SO42-、NO3
C. Na+、 K+、Cl、 NO3 D. Ba2+、K+、SO42-、Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,1 mol/L的NH4Cl、CH3COONH4、NH4HSO4、NH3·H2O四种溶液中,测得c(NH![]() )分别为a、b、c、d(单位为mol/L),下列判断正确的是( )
)分别为a、b、c、d(单位为mol/L),下列判断正确的是( )
A.a=b=c=d B.a>b>d>c
C.d >a>c>b D.c>a>b>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】丁二酮肟![]() 是检验Ni2+的灵敏试剂。
是检验Ni2+的灵敏试剂。
(1)Ni2+基态核外电子排布式为___________ 。丁二酮肟分子中C原子轨道杂类型为 ____________,1mol丁二酮肟分子所含![]() 键的数目为 ____________,分子中各原子的电负性由大到小的顺序为______________。
键的数目为 ____________,分子中各原子的电负性由大到小的顺序为______________。
(2)Ni能与CO形成四羰基镍[Ni(CO)4],四羰基镍熔点-19.3℃,沸点42.1℃,易溶于有机溶剂。
①Ni(CO)4固态时属于 __________晶体(填晶体类型)。
②与CO互为等电子体的阴离子为 ________________(填化学式)。
(3)Ni2+与Mg2+、O2—形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为 ____________。
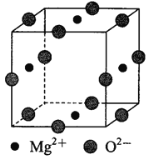
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一份含有FeCl3和FeCl2固体的混合物,为测定FeCl2的含量,进行如下实验:
①称取混合物样品的质量7.06g,将样品溶解
②向溶解后的溶液中,加入足量的双氧水
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀
④将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4.00g
根据实验回答下列问题:
(1)样品溶解过程中需加入 ,以防止 ;
(2)写出溶解后的溶液与双氧水反应的离子方程式 ;
(3)过滤操作中除用漏斗外,还需要的玻璃仪器有 ;
(4)简述检验实验步骤④中沉淀已经洗涤干净的方法 ;
(5)通过实验所得数据,计算固体样品中FeCl2的质量分数: ;
(6)实验室采用如图装置制取少量无水FeCl3固体.(已知FeCl3固体易潮解,部分夹持仪器已略去.)
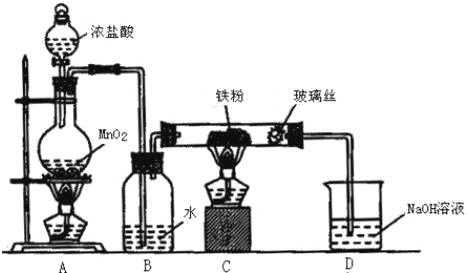
该装置存在明显缺陷,得不到无水FeCl3固体,请你对该装置进行合理的改进: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com