
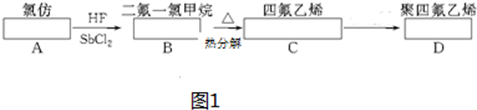


分析 Ⅰ.氯仿为CHCl3,二氟一氯甲烷的结构简式为CHClF2,二氟一氯甲烷在加热条件下生成四氟乙烯,其结构简式为CF2═CF2,据元素守恒可知需2mol二氟一氯甲烷制取1mol四氟乙烯,同时又得到HCl.四氟乙烯发生加聚反应得到聚四氟乙烯,其结构简式构为 ;
;
Ⅱ.二氧化硫是否存在可用品红溶液检验,检验乙烯可以用溴水或高锰酸钾酸性溶液,乙烯和二氧化硫都能使溴水或高锰酸钾酸性溶液褪色;
乙烯与溴水发生加成反应使溴水褪色:CH2=CH2+Br2→CH2Br-CH2Br,乙烯被酸性高锰酸钾氧化使其褪色.二氧化硫与溴水、酸性高锰酸钾发生氧化还原反应,5SO2+2KMnO4+2H2O═K2SO4+2MnSO4+2H2SO4,SO2+Br2+H2O═H2SO4+2HBr;乙烯不与NaOH溶液反应,但二氧化硫能与碱反应(SO2+2NaOH=Na2SO3+H2O),故乙烯的检验应放在排除SO2的干扰后进行,选通过品红溶液褪色检验SO2的存在;再通过NaOH溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净.最后用高锰酸钾酸性溶液褪色实验检验乙烯.
解答 解:Ⅰ.二氟一氯甲烷在加热条件下生成四氟乙烯,据元素守恒可知需2mol二氟一氯甲烷制取1mol四氟乙烯,同时又得到HCl,反应方程式为:2CHClF2$\stackrel{△}{→}$CF2=CF2+2HCl,CF2═CF2在催化剂条件下发生加聚反应生成聚四氟乙烯,方程式为nCF2═CF2$\stackrel{催化剂}{→}$ ,
,
故答案为:2CHClF2$\stackrel{△}{→}$CF2=CF2+2HCl;nCF2═CF2$\stackrel{催化剂}{→}$ ;
;
Ⅱ.(1)乙烯不与NaOH溶液反应,但二氧化硫能与碱反应(SO2+2NaOH=Na2SO3+H2O),二氧化硫是否存在可用品红溶液检验,乙烯的检验应放在排除SO2的干扰后进行,选通过品红溶液褪色检验SO2的存在;再通过NaOH溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净.最后用高锰酸钾酸性溶液褪色实验检验乙烯,
故答案为:④;⑥;④;①;
(2)乙烯和二氧化硫都能使溴水或高锰酸钾酸性溶液褪色,二氧化硫的存在影响乙烯的检验,故检验乙烯时应先除去二氧化硫,所以装置B的作用是除去二氧化硫气体,以免干扰乙烯的实验,通过NaOH溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,所以装置C的作用是检查二氧化硫是否除尽,
故答案为:除去二氧化硫气体,以免干扰乙烯的实验;检查二氧化硫是否除尽;
(3)二氧化硫是否存在可用品红溶液检验,所以能说明混合气体中含SO2的实验现象是装置A中品红溶液褪色,最后用高锰酸钾酸性溶液褪色实验检验乙烯,装置D中的酸性高锰酸钾溶液褪色,说明含有乙烯,
故答案为:装置A中品红溶液褪色;装置D中的酸性高锰酸钾褪色.
点评 本题考查有机物的合成,题目难度不大,注意根据物质的名称能正确写出有机物的结构简式,本题考查乙烯的化学性质、制备以及常见气体的检验,题目难度不大,注意实验的先后顺序


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
| A的用量 | B的用量 | A2B的质量 | |
| 甲 | 7.0 g | 1.0 g | 5.0 g |
| 乙 | 4.0 g | 4.0 g | 5.0 g |
| 丙 | a g | b g | 3.0 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酚遇FeCl3溶液时立即显紫色,而醇不能 | |
| B. | 分子内有苯环和羟基的化合物一定是酚 | |
| C. | 含有羟基的化合物一定是醇 | |
| D. | 酚和醇具有相同的官能团,因而具有相同的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 天气情况 | 平均风速(m/s) | 空气中SO2的平均含量(mg/L) |
| 雨前 | ||
| 雨后 | ||
| 晴 | ||
| 晴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Iˉ只有还原性,IO32-只有氧化性 | |
| B. | 由①②可知氧化性的强弱顺序为Cl2>I2>IO32- | |
| C. | ①中发生反应的离子方程式为:3Cl2+Iˉ+3OHˉ=IO32-+6Clˉ+3H+ | |
| D. | 反应②中若有5mol电子转移,则生成3mol单质I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采取低碳、节俭的生活方式 | |
| B. | 经常使用一次性筷子、纸杯、塑料袋等 | |
| C. | 深入农村和社区宣传环保知识 | |
| D. | 按照规定对生活废弃物进行分类放置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com