
【题目】下列属于碱性氧化物的是
A. SO2 B. CaO C. CO D. Cu2(OH)2CO3
科目:高中化学 来源: 题型:
【题目】下面是一些晶体的结构示意图。
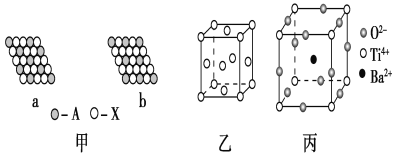
(1)下列关于晶体的说法正确的是________(填字母)。
A.晶体的形成与晶体的自范性有关
B.可以用X射线衍射仪区分晶体和非晶体
C.石蜡是非晶体,但有固定的熔点
D.晶胞就是晶体
(2)图甲表示的是晶体的二维平面示意图,a、b中可表示化学式为AX3的化合物的是________。(填“a”或“b”)
(3)图乙表示的是金属铜的晶胞,请完成以下各题:
①该晶胞“实际”拥有的铜原子数是________,铜原子的配位数为________。
②该晶胞称为________(填字母)。
A.六方晶胞
B.体心立方晶胞
C.面心立方晶胞
(4)图丙为钛酸钡晶体的晶胞结构,该晶体经X射线分析得出,重复单位为立方体,顶点位置被Ti4+所占据,体心位置被Ba2+所占据,棱心位置被O2-所占据。
①写出该晶体的化学式:_____________________________。
②若将Ti4+置于晶胞的体心,Ba2+置于晶胞顶点,则O2-处于立方体的________位置。
③Ti4+的氧配位数和Ba2+的氧配位数分别为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,2.24L SO3中含有的氧原子数目为0.3NA
B. 18gH218O和2H2O的混合物中,所含中子数为10NA
C. 一定条件下,2.3g的金属钠完全与氧气反应时生成3.6g产物时失去的电子数为0.1NA
D. 物质的量浓度为0.1molL﹣1的MgCl2溶液中,含有Cl﹣个数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列各化合物:
A.CH3CH2CH2CHO与CH3COCH2CH3
B.CH3CH(NH2)COOH与H2NCH2COOH
C. ![]() 与
与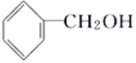
D.CH3CH2C≡CH与CH2=CH-CH=CH2
E.HOOCCH2CH2COOH与HOOC-COOH
F.戊烯与环戊烷
已知:![]()
 。
。
(1)上述各组化合物中属于同系物的是________,属于同分异构体的是________(填字母)。
(2)上述化合物中的含氧官能团是_____________________(写名称)。根据官能团的特点可将C中两种化合物划分为________类和________类。
(3)若将A中两化合物看作是某单烯烃被酸性高锰酸钾溶液氧化生成的,则单烯烃的结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯是海水中含量最丰富的元素,氯的单质及其化合物在生成、生活领域应用广泛。
(1)自来水厂常用液氯进行杀菌消毒。氯气溶于水发生的可逆反应为______________(用离子方程式表示)。
(2)用液氯消毒会产生微量有机氯代物,危害人体健康,可以使用二氧化氯(ClO2)代替液氯。工业上以黄铁矿(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯气体。已知黄铁矿中的硫元素(-1价)最终氧化成SO42-,写出制备二氧化氯的离子方程式_____________________________________。
(3)生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,如图为生产流程示意图。
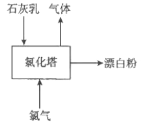
生产漂白粉反应的化学方程式为_____________________。实际生产中,将石灰乳(含有3%-6%水分的熟石灰)从塔顶喷洒而下,氯气从塔的最底层通入。这样加料的目的是_____________________________。
(4)用莫尔法可以测定溶液中Cl-的含量。莫尔法是一种沉淀滴定法,用标准AgNO3溶液滴定待测液,以K2CrO4为指示剂,滴定终点的现象是溶液中出现砖红色沉淀(Ag2CrO4)。已知平衡Cr2O72-+H2O![]() 2CrO42-+2H+,该滴定过程需要控制pH范围在6.5~10.5,若pH小于6.5会使测定结果偏高。结合平衡移动原理解释偏高的原因:_______________________________ 。
2CrO42-+2H+,该滴定过程需要控制pH范围在6.5~10.5,若pH小于6.5会使测定结果偏高。结合平衡移动原理解释偏高的原因:_______________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业是最基本的化学工业之一,其产品用途广泛。
(1)写出氯碱工业电解食盐水的离子方程式____________。
(2)①图1是氯碱工业中阳离子交换膜电解槽示意图(“阳离子交换膜”特性是只允许阳离子通过而阻止阴离子和气体通过)。
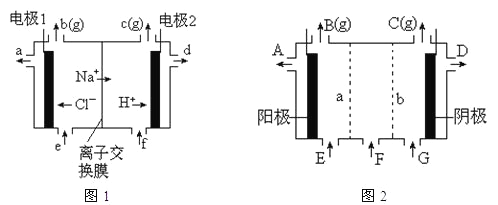
图1中电极1应连接电源的__极(填“正”或“负”极);理论上讲,从f口加入纯水即可,但实际生产中,纯水中要加入一定量的NaOH溶液,其原因是_____。
②图2是根据氯碱工业中离子交换膜技术原理,设计的电解Na2SO4溶液生产NaOH和H2SO4溶液的装置。其中a、b处均设有离子交换膜,则a处为__(填“阳”、“阴”)离子交换膜。阳极的电极反应式是___。从D口流出的物质为____。
(3)某同学采用如下装置对氯碱工业中电解食盐水的条件进行探究,记录如下:
装置 | 编号 | 条件控制 | 测定结果 | ||||
电极材料 | 溶液浓度 | 温度/℃ | *电解电压/V | 气体V阴:V阳 | |||
阴极 | 阳极 | ||||||
| I | C | C | 1 mol/L | 25 | 8 | >1:1 |
II | 饱和 | 25 | 5 | ≈1:1 | |||
III | 饱和 | 50 | 4 | ≈1:1 | |||
IV | Fe | C | 饱和 | 50 | 3.5 | ≈1:1 | |
电解电压:开始发生电解反应时的电压
①对比实验I和Ⅱ阴、阳极气体体积比,推测实验I阳极可能有其它气体生成,其它气体的化学式为_____。
②资料显示:“较低的电解电压有利于节能降耗……”。结合上表中Ⅲ和Ⅳ的数据,解释Ⅳ更有利于节能降耗的原因_______________。
(4)资料显示“氯碱工业中采用金属阳极材料,可以降低电解电压,实现节能降耗”,该同学用50℃的饱和NaCl溶液进行实验验证,结果如下:
装置 | 编号 | 电极材料 | 电解 电压/V | 现象 | |
阴极 | 阳极 | ||||
| V | Fe | Fe | 1.5 | 阴极:产生无色气体 U形管底部:有白色沉淀生成 |
VI | Fe | Cu | 2 | 阴极:产生无色气体 阳极:有白色胶状沉淀生成且逐渐增多 U形管底部:靠近阴极区白色胶状沉淀逐渐转化为淡黄色,最后变成砖红色 | |
实验V中,通过检验阴、阳极附近溶液所含离子,推断产生白色沉淀为Fe(OH)2 。该同学经查阅资料分析认为:“实验VI中白色沉淀是CuCl,淡黄色沉淀是CuOH。
i.阳极生成CuCl的电极反应式为_________。
ii.用化学用语和必要文字解释阴极区白色胶状沉淀转化为淡黄色的原因___________。
该同学通过以上探究认为,氯碱工业中不能采用Fe、Cu作阳极材料。
(5)综合以上探究,你对氯碱工业中电解食盐水条件控制的建议有 _____(至少写出两条)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com