
����Ŀ����Ҫ����գ�
��1��32 g CH4����Ħ������Ϊ_______��Լ����____Ħ���ӣ��ڱ�״������ռ�����ԼΪ____L��
��2������������ʵ���Ũ�ȵ�Ca(OH)2��Һ��NaHCO3��Һ��ϣ����ӷ���ʽΪ��______��
��3��H++HCO3-��H2O+CO2����Ӧ��һ����ѧ����ʽ________________________��
��4���Ʊ�����������������ӷ���ʽ________________��
�������������ʣ�
��NaCl���� ��Һ̬SO3 ��Һ̬�Ĵ��� �ܹ� ��BaSO4���� ������(C12H22O11) �߾ƾ�(C2H5OH) ���ۻ���KNO3 �����ᡣ��ش���������(�����)��
��1�������������ܵ������__________________��
��2�������������ڵ���ʵ���_________________��
��3���������������ڷǵ���ʵ���______________��
���𰸡�16g/mol 20 44.8 Ca2++OH��+HCO3����CaCO3��+H2O HCl+NaHCO3��NaCl+CO2��+H2O Fe3++3H2O![]() Fe(OH)3(����)+3H+ �ܢ�� �٢ۢݢ� �ڢޢ�
Fe(OH)3(����)+3H+ �ܢ�� �٢ۢݢ� �ڢޢ�
��������
��1���������Է���������16��������Ħ��������16g/mol��32 g CH4�����ʵ�����32g��16g/mol��2mol��1���Ӽ��麬��10�����ӣ���˺���20mol���ӡ�����V=nVm��֪�ڱ�״������ռ�����ԼΪ2mol��22.4L/mol��44.8L��
��2������������ʵ���Ũ�ȵ�Ca(OH)2��Һ��NaHCO3��Һ��Ϸ�Ӧ����̼��ơ��������ƺ�ˮ����Ӧ�����ӷ���ʽΪCa2++OH��+HCO3����CaCO3��+H2O��
��3��H++HCO3-��H2O+CO2����Ӧ��һ����ѧ����ʽ������HCl+NaHCO3��NaCl+CO2��+H2O��
��4�������Ȼ�����Һ�����ˮ�м�������һ��ʱ��ɵõ������������壬���Ʊ�����������������ӷ���ʽΪFe3++3H2O![]() Fe(OH)3(����)+3H+��
Fe(OH)3(����)+3H+��
������ˮ������״̬���ܹ�����Ļ������ǵ���ʣ�����ˮ��������״̬�¾����ܵ���Ļ������Ƿǵ���ʣ����������ƶ����ӻ����ӵ����ʿ��Ե��硣
��NaCl���岻���磬�ǵ���ʣ�
��Һ̬SO3�����磬�Ƿǵ���ʣ�
��Һ̬�Ĵ�����磬�ǵ���ʣ�
�ܹ��ǽ������ܵ��磬���ǵ����Ҳ���Ƿǵ���ʣ�
��BaSO4���岻���磬�ǵ���ʣ�
������(C12H22O11)�����磬�Ƿǵ���ʣ�
�߾ƾ�(C2H5OH)�����磬�Ƿǵ���ʣ�
���ۻ���KNO3�ܵ��磬�ǵ���ʣ�
�������ܵ��磬���ڻ������ǵ����Ҳ���Ƿǵ���ʡ���
��1�������������ܵ�����Ǣܢ�ᡣ
��2�������������ڵ���ʵ��Ǣ٢ۢݢࡣ
��3���������������ڷǵ���ʵ��Ǣڢޢߡ�


 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǹ�ҵ���Ʊ�Na2S2O3�ķ���֮һ����Ӧԭ��Ϊ��2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2���÷�Ӧ��H��0����ij�о�С����ʵ��������Ʊ�Na2S2O3��5H2O�������¡�

��1������װ����ͼ��ʾ��

��װ��B�������Ǽ���װ��A��SO2������Ч�ʣ�B���Լ���_____________������SO2����Ч�ʵ͵�ʵ��������B����Һ______________��
��Ϊ��ʹSO2������������ȫ���ڲ��ı�A����ҺŨ�ȡ�����������£����˼�ʱ���跴Ӧ���⣬���ɲ�ȡ�ĺ�����ʩ��______________������дһ����
��2�����豾ʵ�����õ�Na2CO3������NaCl��NaOH�����ʵ�鷽�����м��顣������ʱCaCO3������Һ��pH��10.2������ѡ�Լ���������ϡ���ᡢAgNO3��Һ��CaCl2��Һ����̪��Һ������ˮ��pH�ơ��ձ����Թܡ��ι�
��� | ʵ����� | Ԥ������ | ���� |
�� | ȡ������Ʒ���Թ��У�������������ˮ��������ܽ⣬____________ �� | �а�ɫ�������� | ��Ʒ��NaCl |
�� | ��ȡ������Ʒ���ձ��У�������������ˮ����ֽ����ܽ⣬_______�� | ���ɫ�������ɣ��ϲ���ҺpH>10.2 | ��Ʒ��NaOH |
��3��Na2S2O3��Һ�Ƕ���ʵ���еij����Լ����ⶨ��Ũ�ȵĹ������£�
��һ����ȷ��ȡa g KIO3(��Է���������214)���������Һ��
�ڶ������������KI�����H2SO4��Һ���μ�ָʾ����
����������Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��Һ�����Ϊv mL����c(Na2S2O3)��______mol��L-1����ֻ�г���ʽ���������㣩
��֪��IO3-+I-+6H+=3I2+3H2O 2S2O32-+I2=S4O62-+2I-����ͬѧʢװNa2S2O3��Һ֮ǰδ��ϴ��������õ�Na2S2O3��Ũ�ȿ���________��������Ӱ��������ƫ��������ƫ����)����ͬѧ��һ���͵ڶ����IJ������ܹ淶������������̫����������õ�Na2S2O3��Ũ�ȿ���________(������Ӱ�������� ƫ��������ƫ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H����Ҫ���л������E��F��һ�������ºϳɣ�(���ַ�Ӧ������ʡ�ԣ�����ע���ͷ��ָ����)
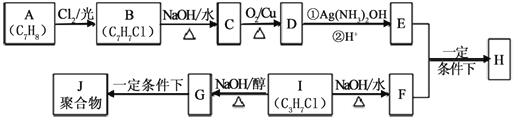
��֪������Ϣ��
i.A���ڷ�������H����������
ii.I�ĺ˴Ź�������Ϊ����壬�ҷ�������Ϊ6:1��
�ش��������⣺
(1)E�ĺ�������������________��B�Ľṹ��ʽ_____________��
(2)G �� J�ķ�Ӧ����________________��
(3)�� E + F �� H�Ļ�ѧ����ʽ___________________��
�� I �� G �Ļ�ѧ����ʽ_____________________________��
(4)H��ͬϵ��K��H��Է�������С28��K�ж���ͬ���칹�塣
��K��һ��ͬ���칹���ܷ���������Ӧ��Ҳ��ʹFeCl3��Һ����ɫ��������������֧���������ϵ���ĺ˴Ź�������Ϊ����壬�ҷ������Ϊ1:1��д��K������ͬ���칹��Ľṹ��ʽ_________________��
����K��ͬ���칹������ڷ����廯������ܺͱ���NaHCO3��Һ��Ӧ�ų�CO2���������������ͬ���칹�干��__________��(�����������칹)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ͷ���������ͳһ������Ϊ
A. ����ϸ���ĸ��ֻ������ڷ������ж�����
B. �����ͷ�����綼�����³´�л
C. ����ϸ���������ڷ�������Ƕ�����
D. ����ϸ���ĸ��ֻ�ѧԪ��������Ȼ���ж����ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���Ũ����ͬ��������NaX��NaY��NaZ����Һ����PH����Ϊ8��9��10����HX��HY��HZ��������ǿ������˳����( )
A. HX��HZ��HY B. HX��HY��HZ C. HZ��HY��HX D. HY��HZ��HX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������;������������ȷ����
A.Һ�������������B.Ũ��������������
C.�����ƿ������Ʊ��轺D.���ʹ���������ά
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ����Ҫ�Ĺ�ҵԭ�ϣ���Ũ��һֱΪ��������ע������˵����ȷ����
����Ҫ�Ĺ�ҵԭ�ϣ���Ũ��һֱΪ��������ע������˵����ȷ����
A. ![]() ԭ�Ӻ��к���92������ B.
ԭ�Ӻ��к���92������ B. ![]() ԭ�Ӻ�����143������
ԭ�Ӻ�����143������
C. ![]() ��
��![]() ��Ϊͬλ�� D.
��Ϊͬλ�� D. ![]() ��
��![]() Ϊͬһ����
Ϊͬһ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��4 ���£�������A gĦ������ΪM g��mol��1�Ŀ�������RCln �ܽ���V mLˮ�У�ǡ���γɸ��¶��µı�����Һ���ܶ�Ϊ�� g��cm��3�����й�ϵʽ�������
A. ���ʵ����������أ�A/(A��V)��100%
B. ���ʵ����ʵ���Ũ��c��1 000�� A/(MA��MV) mol��L��1
C. ���¶��´��ε��ܽ��S��100A/V g
D. 1 mL����Һ��n(Cl��)��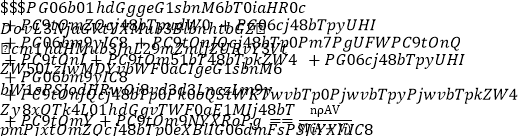 mol
mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����4��̼ԭ�ӽ�ϳɵ�6���л���(��ԭ��û�л���)
![]()
(1) д���л���(a)��ϵͳ������������___________________��
(2) �л���(a)��һ��ͬ���칹�壬��д����ṹ��ʽ__________________��
(3) �����л�������(c)��Ϊͬ���칹�����________(�����)��
(4) ��дһ����(e)��Ϊͬϵ����л���Ľṹ��ʽ____________��
(5) �����л����в������巴Ӧ��ʹ����ɫ����________(�����)��
(6) (a)(b)(c)(d)���������У�4��̼ԭ��һ������ͬһƽ�����________(�����)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com