
【题目】下列说法中正确的是
A. 电子云通常是用小黑点来表示电子的多少
B. 在同一能级上运动的电子,其运动状态是相同的
C. 能层序数越大,s电子云的半径越大
D. 电子仅在激发态跃迁到基态时才会产生原子光谱
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】吲哚昔酚 (idoxifene)可用于治疗骨质疏松症,它的合成路线如图。
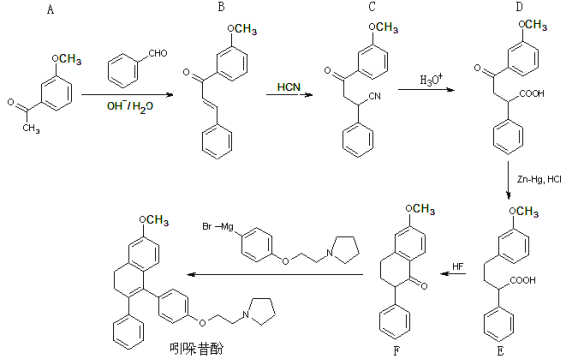
(1)反应类型:B→C ;D→E
(2)D中的含氧官能团为 (写名称)
(3)满足下列四个条件的A的同分异构体数目有 种。
①苯的衍生物,且苯环上只有两个互为对位的取代基;②能发生银镜反应;③与FeCl3溶液作用不显色;④不与氢氧化钠水溶液反应
(4)E→F中还有一种副产物G生成,G与F互为同分异构体,且含有三个六元环,G结构简式为
(5)2,2-二甲基戊酸[CH3CH2CH2C(CH3)2COOH]是有机合成中间体,请设计合理的方案以丙酮(CH3COCH3)为唯一有机原料合成2,2-二甲基戊酸异丙酯(用合成路线流程图表示,并注明反应条件)
提示:①合成过程中无机试剂任选;②丙酮分子间能发生上图合成路线中A→B的类似反应;③合成路线流程图示例:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() CH2Br-CH2Br
CH2Br-CH2Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对一些实验事实的解释正确的是
选项 | 实验事实 | 解释 |
A | 水加热到较高温度都难以分解 | 水分子间存在氢键 |
B | 白磷为正四面体分子 | 白磷分子中P-P键间的键角是109°28′ |
C | 用苯萃取碘水中的I2 | 苯和I2均为非极性分子,且苯与水互不相溶 |
D | H2O的沸点高于H2S | H-O键的键长比H-S键的键长短 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是
A. 在标准状况下,11.2 L H2O中含有的分子数为0.5 NA
B. 32 g O2所含的原子数为2 NA
C. 1 mol/L NaCl溶液中含有的Na+的数为NA
D. 1 mol Na2O2中离子总数为4 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖的结构简式为:CH2OH—CHOH—CHOH—CHOH—CHOH—CHO其对应的性质中不正确的是( )
A.1mol葡萄糖最多可以与5mol金属钠反应放出氢气
B.1mol葡萄糖最多可以与5mol乙酸发生取代反应
C.能发生银镜反应
D.可与小苏打溶液反应冒出气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机合成在制药工业上有着极其重要的地位。现用硝基苯制取苯胺,再用苯胺制得无 色晶体乙酰苯胺(具有退热镇痛作用的药物)。
①化学反应原理为:
![]()
②相关物质的物理常数
物质 | 相对分子质量 | 熔点(℃) | 沸点(℃) | 溶解度(g) | |
水 | 乙醇 | ||||
苯胺 | 93 | -6 | 184 | 3.42(20℃) | 任意比混溶 |
乙酸 | 60 | 17 | 117.9 | 任意比混溶 | 任意比混溶 |
乙酰苯胺 | 135 | 114 | 304 | 0.56(20℃) 3.45(50℃) 5.20(100℃) | 36.9(20℃) |
③制备乙酰苯胺的装置及过程如下图所示:
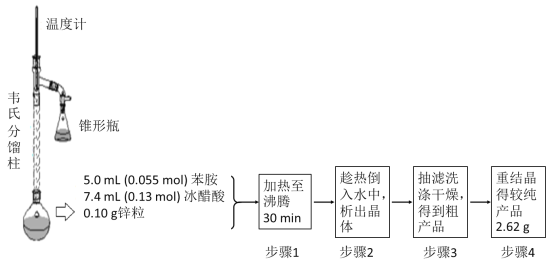
已知:Ⅰ苯胺易被氧化;Ⅱ韦氏分馏柱作用与原理类似于冷凝管
请回答以下问题:
(1)加入锌粒的目的是___________;韦氏分馏柱作用的是_________;
(2)步骤1中保持柱顶温度约为105℃,则锥形瓶中收集到的馏分主要是_____________;
(3)步骤2中将反应液倒入水中的目的是___________;
(4)步骤3中洗涤剂最好选择______________;
A.冷水 B.热水 C.15%的乙醇溶液 D.NaOH溶液
(5)步骤4重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→________→__________→抽滤→洗涤→干燥;
(6)上述制备过程的产率是____________。(结果保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铜、硝酸银溶液和银组成的原电池装置中,当导线中有0.02mol电子通过时,理论上银片的质量变化了多少?
(2)将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) =xC(g)+2D(g),经过5分钟后,测得D的浓度为0.5mol/L,C的平均反应速率是0.1mol/(L·min),且c(A):c(B)=3:5。求:(1)x的值和反应开始前放入容器中A、B的物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量的氧化铁杂质。具体实验流程如下:
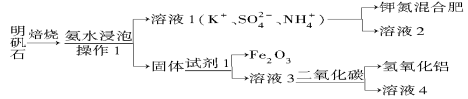
(1)操作1所用到的玻璃仪器的名称是 。
(2)由溶液3制取氢氧化铝的离子方程式为 。
(3)明矾石焙烧时产生SO2,请你写出能验证SO2具有还原性且实验现象明显的化学方程式: 。
(4)请你写出验证溶液1中有NH4+的实验过程: 。
(5)实验室用Fe2O3与CO反应来制取单质Fe。
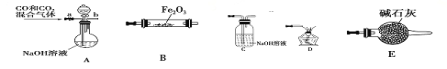
①请按气流由左到右的方向连接下列各装置,顺序为A→________。
②在点燃B处的酒精灯前,应进行的操作是____________。
③装置C的作用是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com