
【题目】(1)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式_______
(2)某炔烃和氢气充分加成生成2,5﹣二甲基己烷,该炔烃的结构简式是_______
(3)某芳香烃结构为![]() 。它一氯代物有_______种。
。它一氯代物有_______种。
(4)分子式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为_______,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为_______。
(5) 分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,该芳香烃的结构简式是_______。
【答案】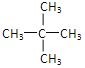 (CH3)2CHC≡CCH(CH3)2 4
(CH3)2CHC≡CCH(CH3)2 4 ![]() CH3C≡CCH3
CH3C≡CCH3 ![]()
【解析】
(1)戊烷的某种同分异构体只有一种一氯代物,说明该有机物分子中只含1种类型的氢原子;
(2)饱和烃与炔烃分子中碳的骨架完全相同,饱和烃相邻碳原子上必须均含有两个或两个以上的氢原子时才可出现碳碳叁键,根据2,5-二甲基己烷确定炔烃的结构简式;
(3)芳香烃的结构简式是![]() ,分子中有4种氢原子;
,分子中有4种氢原子;
(4)根据乙烯是平面型分子,乙炔是直线型分子,分析判断;
(5)分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,说明结构具有对称性,据此分析判断。
(1)戊烷的某种同分异构体只有一种一氯代物,说明该有机物分子中只含1种类型的氢原子,该烃的结构简式为 ,故答案为:
,故答案为: ;
;
(2)饱和烃与炔烃的碳的骨架完全相同,倒推可得,饱和烃相邻碳原子上必须均含有两个或两个以上的氢原子时才可出现碳碳叁键,所以某炔烃和氢气充分加成生成2,5-二甲基己烷,该炔烃的结构简式是(CH3)2CHC≡CCH(CH3)2,故答案为:(CH3)2CHC≡CCH(CH3)2;
(3)芳香烃的结构简式是![]() ,分子中有4种氢原子(
,分子中有4种氢原子(![]() ),所以一氯代物有4种,故答案为:4;
),所以一氯代物有4种,故答案为:4;
(4)乙烯是平面型分子,![]() 可看做乙烯中的四个氢原子被甲基取代,所以分子式为C6H12且所有碳原子都在同一平面上的烃的结构简式为
可看做乙烯中的四个氢原子被甲基取代,所以分子式为C6H12且所有碳原子都在同一平面上的烃的结构简式为![]() ;乙炔是直线型分子,CH3C≡CCH3可看做是甲基取代乙炔分子上的氢原子,所以分子式为C4H6的烃中所有的碳原子都在同一条直线上的结构简式是CH3C≡CCH3,故答案为:
;乙炔是直线型分子,CH3C≡CCH3可看做是甲基取代乙炔分子上的氢原子,所以分子式为C4H6的烃中所有的碳原子都在同一条直线上的结构简式是CH3C≡CCH3,故答案为:![]() ;CH3C≡CCH3;
;CH3C≡CCH3;
(5)分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,说明结构对称,所以结构简式是![]() ,故答案为:
,故答案为:![]() 。
。


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列关于 的说法,正确的是( )
的说法,正确的是( )
A.该物质可由n个单体分子通过缩聚反应生成
B.![]() 该物质完全燃烧,生成33.6 L(标准状况)的
该物质完全燃烧,生成33.6 L(标准状况)的![]()
C.该物质在酸性条件下水解产物之一可作汽车发动机的抗冻剂
D.![]() 该物质与足量
该物质与足量![]() 溶液反应,最多可消耗
溶液反应,最多可消耗![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯的分子式为C2H4,是一种重要的化工原料和清洁能源,研究乙烯的制备和综合利用具有重要意义。
请回答下列问题:
(1)乙烯的制备:工业上常利用反应C2H6(g)![]() C2H4(g)+H2(g) △H制备乙烯。
C2H4(g)+H2(g) △H制备乙烯。
已知:Ⅰ.C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) △H1=-1556.8kJ·mol-1;
Ⅱ.H2(g)+![]() O2(g)=H2O(1) △H2=-285.5kJ·mol-1;
O2(g)=H2O(1) △H2=-285.5kJ·mol-1;
Ⅲ.C2H6(g)+![]() O2(g)=2CO2(g)+3H2O(l) △H3=-1559.9kJ·mol-1。
O2(g)=2CO2(g)+3H2O(l) △H3=-1559.9kJ·mol-1。
则△H=___kJ·mol-1。
(2)乙烯可用于制备乙醇:C2H4(g)+H2O(g)![]() C2H5OH(g)。向某恒容密闭容器中充入a mol C2H4(g)和 a mol H2O(g),测得C2H4(g)的平衡转化率与温度的关系如图所示:
C2H5OH(g)。向某恒容密闭容器中充入a mol C2H4(g)和 a mol H2O(g),测得C2H4(g)的平衡转化率与温度的关系如图所示:
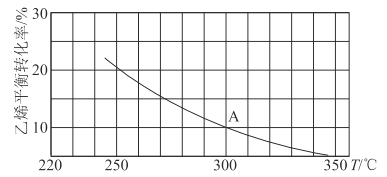
①该反应为____热反应(填“吸”或“放”),理由为____。
②A点时容器中气体的总物质的量为____。已知分压=总压×气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数(KP),测得300℃时,反应达到平衡时该容器内的压强为b MPa,则A点对应温度下的KP=____MPa-1(用含b的分数表示)。
③已知:C2H4(g)+H2O(g)![]() C2H5OH(g)的反应速率表达式为v正=k正c(C2H4)·c(H2O),v逆=k逆c(C2H5OH),其中,k正、k逆为速率常数,只与温度有关。则在温度从250℃升高到340℃的过程中,下列推断合理的是___(填选项字母)。
C2H5OH(g)的反应速率表达式为v正=k正c(C2H4)·c(H2O),v逆=k逆c(C2H5OH),其中,k正、k逆为速率常数,只与温度有关。则在温度从250℃升高到340℃的过程中,下列推断合理的是___(填选项字母)。
A.k正增大,k逆减小 B.k正减小,k逆增大
C.k正增大的倍数大于k逆 D.k正增大的倍数小于k逆
④若保持其他条件不变,将容器改为恒压密闭容器,则300℃时,C2H4(g)的平衡转化率__10%(填“>”“<”或“=”)。
(3)乙烯可以被氧化为乙醛(CH3CHO),电解乙醛的酸性水溶液可以制备出乙醇和乙酸,则生成乙酸的电极为_____极(填“阴”或“阳”),对应的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.红外光谱及![]() 核磁共振谱均可以给出有机物分子结构的信息
核磁共振谱均可以给出有机物分子结构的信息
B.钛可制成飞船的“外衣”,高温时可用金属钠还原四氯化钛来制取金属钛
C.蚕丝被轻薄透气,蚕丝的主要成分是纤维素,属于天然高分子化合物
D.从原子利用率的角度来看,加成反应符合绿色化学思想
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.90g某有机物完全燃烧只生成1.32g CO2和0.54g H2O,下列有关该有机物的说法正确的是( )
A.一定只含C、H、O三种元素
B.一定含有C、H两种元素,一定不含O元素
C.该有机物的分子式为C3H6O2
D.不能确定是否含有除C、H、O之外的其他元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是( )
A.标准状况下0.5mol![]() N3
N3![]() T分子中所含中子数为6.5NA
T分子中所含中子数为6.5NA
B.0.1molFe与0.1molCl2完全反应后,转移的电子数为0.2NA
C.13.35gAlCl3水解形成的Al(OH)3胶体粒子数小于0.1NA
D.一定条件下的密闭容器中,2molSO2和1molO2催化反应充分发生后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向![]() 盐酸中滴加
盐酸中滴加![]() 溶液,溶液的pH随
溶液,溶液的pH随![]() 溶液体积的变化如图。已知
溶液体积的变化如图。已知![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
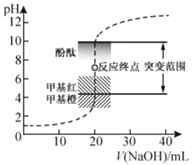
A.![]() 与盐酸恰好完全反应时,
与盐酸恰好完全反应时,![]()
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.![]() 时,
时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】均三甲苯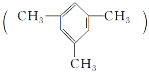 是一种易燃、不溶于水、比水密度小的有毒液体,是重要的有机化工原料,用于制备合成树脂、抗氧化剂等。
是一种易燃、不溶于水、比水密度小的有毒液体,是重要的有机化工原料,用于制备合成树脂、抗氧化剂等。
(1)均三甲苯属于苯的同系物,选用一种试剂区别苯和均三甲苯:________________。
(2)均三甲苯分子中的一个H原子被Cl原子取代,所得产物有________种。
(3)下列属于苯的同系物的是________(填字母)。
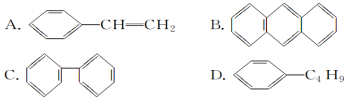
(4)下列物质中,能发生加成反应,也能发生取代反应,同时能使溴水因加成反应而褪色,还能使酸性高锰酸钾溶液褪色的是________(填字母)。
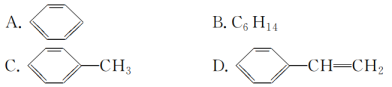
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许______离子通过,氯气的逸出口是_______(填标号)。
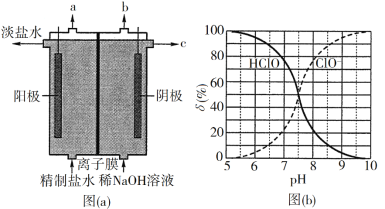
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ[δ(X)=![]() ,X为HClO或ClO]与pH的关系如图(b)所示。HClO的电离常数Ka值为______。
,X为HClO或ClO]与pH的关系如图(b)所示。HClO的电离常数Ka值为______。
(3)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为______。
(4)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为_____mol;产生“气泡”的化学方程式为____________。
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是______(用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000 kg该溶液需消耗氯气的质量为____kg(保留整数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com